早教吧作业答案频道 -->化学-->
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.(1)基态
题目详情
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
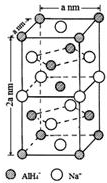
(1)基态Ti原子的价电子轨道表示式为___.
(2)NaH的熔点为800℃,不溶于有机溶剂.NaH属于___晶体,其电子式为___.
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为___(标明配位键).
(4)AlH4-中,Al的轨道杂化方式为___;例举与AlH4-空间构型相同的两种离子___(填化学式).
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有___个;NaAlH4晶体的密度为___g•cm-3(用含a的代数式表示).若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为___(填化学式).
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构.这种结构变化由表面层扩展到整个晶体,从而释放出氢气.该释氢过程可用化学方程式表示为___.

(1)基态Ti原子的价电子轨道表示式为___.
(2)NaH的熔点为800℃,不溶于有机溶剂.NaH属于___晶体,其电子式为___.
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为___(标明配位键).
(4)AlH4-中,Al的轨道杂化方式为___;例举与AlH4-空间构型相同的两种离子___(填化学式).
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有___个;NaAlH4晶体的密度为___g•cm-3(用含a的代数式表示).若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为___(填化学式).
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构.这种结构变化由表面层扩展到整个晶体,从而释放出氢气.该释氢过程可用化学方程式表示为___.
▼优质解答
答案和解析
(1)Ti原子核外电子数为22,价电子排布式为3d24s2,价电子轨道表示式为,故答案为:;(2)NaH的熔点为800℃,不溶于有机溶剂,应属于离子晶体,由钠离子与氢负离子构成,电子式为,故答案为:离子;;(3)氯化铝...
看了 氢化铝钠(NaAlH4)是一...的网友还看了以下:
1.a≠0,b≠0,则a/|a|+b/|b|的不同取值的个数为()A.3B.2C.1D.02.若|x 2020-03-31 …
基本不等式超费解130已知a>b>0,求a2+1/(a*b)+1/[a*(a-b)]的最小值.a2 2020-05-13 …
设集合A={1,a,b},B={a,a^2,ab}且A=B,求实数A,B的值因为集合需要满足互异性 2020-05-15 …
数列a[n+1]=k+(2k+1)a[n]+(k(k+1)a[n]a[n+1])^1/2 已知a1 2020-05-16 …
假设集合A满足以下条件:诺a∈A,a不等于1,则1-a分之1属于A若a属于A,则1-a分之一属于A 2020-07-03 …
立方差公式的推广证明过程(1)a^n-b^n=(a-b)[a^(n-1)+a^(n-2)*b+.. 2020-07-11 …
用a^n-b^n=(a-b)(a^(n-1)+a^(n-2)*b+...+ab^(n-2)+b^( 2020-07-14 …
第一题:设集合M={2,-2a,a²-3},N={a²+a-4,2a+1,-1},且2∈M∩N,求实 2020-11-03 …
递回关系式的运算公式(数列)以下是推导一个公式"a=a+r(1-p^n)/(1-p)"的过程a=p* 2021-01-13 …
在资金时间价值计算时,i和n给定,下列等式中正确的有().A.(F/A,i,n)=[(P/F,i,n 2021-01-14 …