早教吧作业答案频道 -->化学-->
Na2O2与水的反应实际可以分解为两个阶段:Na2O2+2H2O=2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分2H2O2=2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固
题目详情
Na2O2与水的反应实际可以分解为两个阶段:Na2O2+2H2O=2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分 2H2O2=2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:
①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mL KMnO4溶液(此时锰全部以Mn2+存在)
(1)有500mL、250mL、150mL的量筒备用,应选用量程为___的量筒.
(2)该实验应选用___(填“酸式”或“碱式”)滴定管.
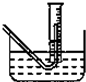
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面(如图),立即读数会使Na2O2的纯度___(填“偏高”“偏低”或“不变”).
(4)在步骤④中还要用到的玻璃仪器有___.
(5)该过氧化钠的纯度为___(用百分数表示,保留一位小数;实验中得到的气体体积均看作为标准状况下).
①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mL KMnO4溶液(此时锰全部以Mn2+存在)

(1)有500mL、250mL、150mL的量筒备用,应选用量程为___的量筒.
(2)该实验应选用___(填“酸式”或“碱式”)滴定管.
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面(如图),立即读数会使Na2O2的纯度___(填“偏高”“偏低”或“不变”).
(4)在步骤④中还要用到的玻璃仪器有___.
(5)该过氧化钠的纯度为___(用百分数表示,保留一位小数;实验中得到的气体体积均看作为标准状况下).
▼优质解答
答案和解析
(1)用量筒时应选择体积接近的量筒,以减少误差,所以收集112mL气体应选择150mL的量筒,故答案为:150mL;
(2)高锰酸钾是强氧化性的物质,应选择酸式滴定管,故答案为:酸式;
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面,立即读数会使收集到的气体体积偏高,结果偏高,应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平,
故答案为:偏高;
(4)配制一定物质的量浓度的溶液需要的玻璃仪器:玻璃棒、胶头滴管,以及一定规格的容量瓶,故答案为:玻璃棒、胶头滴管;
(5)双氧水分解掉的量,据2H2O2═2H2O+O2↑,当生成112mL氧气时,分解掉双氧水
=0.01(mol),根据反应2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O求的剩余双氧水的量
≈0.006mol,所以双氧水的总量=0.01mol+0.006mol=0.016mol,根据反应Na2O2+2H2O═2NaOH+H2O2,可知过氧化钠的量为0.0016mol,纯度=
×100%=62.4%,
故答案为:62.4%.
(2)高锰酸钾是强氧化性的物质,应选择酸式滴定管,故答案为:酸式;
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面,立即读数会使收集到的气体体积偏高,结果偏高,应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平,
故答案为:偏高;
(4)配制一定物质的量浓度的溶液需要的玻璃仪器:玻璃棒、胶头滴管,以及一定规格的容量瓶,故答案为:玻璃棒、胶头滴管;
(5)双氧水分解掉的量,据2H2O2═2H2O+O2↑,当生成112mL氧气时,分解掉双氧水
| 0.112L |
| 22.4L/mol |
| 5×24.4×0.01×10-3×10 |
| 2 |
| 0.0016mol×78g/mol |
| 2.0g |
故答案为:62.4%.
看了Na2O2与水的反应实际可以分...的网友还看了以下:
(1)操作、观察:任意画⊙O,在⊙O内任取一点P(不为圆心),过点P直线l,交⊙O于点A、B.若直 2020-05-13 …
如图,三角形ABC中角B=30度角C=60度AC=6,O为AB上一动点,以O为圆心,OA长为半径画 2020-05-16 …
如图,Rt△ABC中,∠C=90°、∠A=30°,在AC边上取点O画圆,使⊙O经过A、B两点,下列 2020-06-29 …
如图,在Rt△ABC中,∠C=90°,∠A=30°,O为AB上一点,BO=x,⊙O的半径为2.(1 2020-07-21 …
如图,已知⊙O是以数轴的原点O为圆心,半径为1的圆,∠AOB=45°,点P在数轴上运动,若过点P且 2020-07-22 …
如图,以O为圆,AB长为直径作圆,在O上取一点,延长AB至点D,连接DC,过点A作O的切线交DC的 2020-07-31 …
图中a为一固定放置的半径为R的均匀带电球体,O为其球心.己知取无限远处的电势为零时,球表面处的电势 2020-07-31 …
已知关于x的不等式组5-2x≥-1x-a大于0无解,a的取值范围是≥3若只将不等式组中X-a>o改 2020-07-31 …
如图,已知P为O外一点,连结OP交O于点A,且OA=2OP,求作直线PB,使PB与O相切.以下是甲 2020-08-01 …
以O为顶点的角上取一点A,作三角形OAB的外角形OAC的旁切圆O2.若O1A=O2A,求证三角形A 2020-08-03 …