早教吧作业答案频道 -->化学-->
常温下在20mL0.1mol/L碳酸钠溶液中逐滴加入0.1mol/L盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的百分含量也发生变化(二氧化碳因为逸出未画出).据此回答下列问题:(1)用离
题目详情
常温下在20mL0.1mol/L碳酸钠溶液中逐滴加入0.1mol/L盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的百分含量也发生变化(二氧化碳因为逸出未画出).据此回答下列问题:
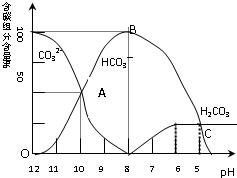
(1)用离子方程式表示碳酸钠溶液呈碱性的原因:___
(2)当加入盐酸使溶液pH为10时,混合液中含碳元素的离子的物质的量之比为___
(3)用等式表示碳酸钠溶液中所有离子浓度之间的关系:___
(4)请写出OAB段的离子方程式:___
(5)当混合溶液的pH=___时,开始放出二氧化碳气体.

(1)用离子方程式表示碳酸钠溶液呈碱性的原因:___
(2)当加入盐酸使溶液pH为10时,混合液中含碳元素的离子的物质的量之比为___
(3)用等式表示碳酸钠溶液中所有离子浓度之间的关系:___
(4)请写出OAB段的离子方程式:___
(5)当混合溶液的pH=___时,开始放出二氧化碳气体.
▼优质解答
答案和解析
(1)碳酸钠溶液中碳酸根离子存在水解平衡:CO32-+H2O⇌HCO3-+OH-,所以溶液显示碱性,故答案为:CO32-+H2O⇌HCO3-+OH-;
(2)根据图中的信息可以知道,当pH=10时,碳酸根离子和碳酸氢根离子的百分含量是相等的,所以n(CO32-):n(HCO3-)=1:1;故答案为:n(CO32-):n(HCO3-)=1:1;
(3)碳酸钠溶液中碳酸根离子水解,溶液显示碱性,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故答案为:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-);
(4)OAB段是溶液中的碳酸根离子和氢离子反应生成碳酸氢根离子的过程,发生反应的离子方程式为:CO32-+H+=HCO3-;
故答案为:CO32-+H+=HCO3-;
(5)碳酸氢根离子和氢离子反应生成二氧化碳,当二氧化碳得到溶解平衡便有二氧化碳放出,即碳酸的百分含量保持不变时,此时pH=6.
故答案为:6.
(2)根据图中的信息可以知道,当pH=10时,碳酸根离子和碳酸氢根离子的百分含量是相等的,所以n(CO32-):n(HCO3-)=1:1;故答案为:n(CO32-):n(HCO3-)=1:1;
(3)碳酸钠溶液中碳酸根离子水解,溶液显示碱性,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故答案为:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-);
(4)OAB段是溶液中的碳酸根离子和氢离子反应生成碳酸氢根离子的过程,发生反应的离子方程式为:CO32-+H+=HCO3-;
故答案为:CO32-+H+=HCO3-;
(5)碳酸氢根离子和氢离子反应生成二氧化碳,当二氧化碳得到溶解平衡便有二氧化碳放出,即碳酸的百分含量保持不变时,此时pH=6.
故答案为:6.
看了 常温下在20mL0.1mol...的网友还看了以下:
已知函数f(x)=a^x,g(x)=(a^2x)+m,其中m>0,a>0且a≠0.当x€[-1,1 2020-06-11 …
已知向量a=(m,2),b=(4,n),其中m>0,n>0,若a*b=6,则2/m+1/n的最小值 2020-06-12 …
如图,在平面直角坐标系xOy中,已知椭圆=1的左、右顶点为A、B,右焦点为F.设过点T(t,m)的 2020-06-14 …
已知从北京到上海通话m分钟的电话费f(m)=1.06(0.5×[m]+1)元,其中m>0.[m]是 2020-06-27 …
已知从北京到上海通话m分钟的电话费f(m)=1.06(0.5×[m]+1)元,其中m>0.[m]是 2020-06-27 …
已知y1=a1(x-m)2+5,点(m,25)在抛物线y2=a2x2+b2x+c2上,其中m>0. 2020-07-09 …
如图,已知:在平面直角坐标系中,直线l与y轴相交于点A(0,m)其中m<0,与x轴相交于点B(4, 2020-07-21 …
已知函数f(x)=|x|,x≤mx2-2mx+4m,x>m,其中m>0,若存在实数b,使得关于x的 2020-07-21 …
一道函数题二次函数f(x)=px^2+qx+r中,实数p,q,r满足p/(m+2)+q/(m+1) 2020-07-26 …
已知函数f(x)=emx(x≥0)1mln(-x)(x<0)(其中m>0,e为自然对数的底数)的图 2020-08-02 …