早教吧作业答案频道 -->化学-->
F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易与水反应.其中6XeF4+12H2O=2XeO3+4Xe↑+24HF+3O2↑,下列推测正确的是(
题目详情
F 2 和Xe在一定条件下可生成XeF 2 、XeF 4 和 XeF 6 三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易与水反应.其中6XeF 4 +12H 2 O=2XeO 3 +4Xe↑+24HF+3O 2 ↑,下列推测正确的是( )
| A、XeF 2 分子中各原子均达到八电子的稳定结构 |
B、 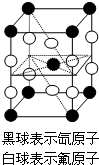 某种氟化氙的晶体结构单元如图所示,可推知其化学式为XeF 6 |
| C、XeF 4 按已知方式水解,每生成2mol Xe转移8 mol电子 |
| D、XeF 2 加入水中,在水分子的作用下,生成Xe和F 2 |
▼优质解答
答案和解析
考点:氧化还原反应 原子核外电子排布 晶胞的计算 专题: 分析:A.根据原子的最外层电子数结合成键电子数判断;B.根据原子在晶胞中的位置利用均摊法计算;C.6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑反应中,Xe元素化合价升高生成XeO3,降低生成Xe,O元素化合价升高,根据化合价降低的计算;D.F2和水剧烈反应,不可能生成F2. A.XeF2分子中Xe最外层电子数为8+2=10,故A错误;B.晶胞中Xe原子个数为:8×18+1=2,F原子个数为:8×14+2=4,故原子个数比Xe:F=1:2,其化学式为XeF2,故B错误;C.6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑反应中,Xe元素化合价升高生成XeO3,降低生成Xe,O元素化合价升高,则生成4molXe,转移电子4mol×(4-0)=16mol,故C正确;D.F2和水剧烈反应,不可能生成F2,故D错误.故选C. 点评:本题考查较为综合,涉及晶胞的计算、氧化还原反应等知识,侧重于学生的分析能力的考查,注意把握晶胞的计算方法,结合元素化合价的变化解答该题,难度不大.
看了F2和Xe在一定条件下可生成X...的网友还看了以下:
在直角坐标系xOy中,圆C的方程为(x-1)2+y2=1.以O为极点,x轴的非负半轴为极轴建立极坐 2020-07-08 …
在直角坐标xoy中,以O为极点,x轴正半轴为极轴建立极坐标系,曲线C的极坐标方程为ρ=2cosθ, 2020-07-08 …
曲线C1的参数方程为x=2+2cosαy=2sinα(α为参数),以坐标原点O为极点,x轴正半轴为 2020-07-09 …
在直角坐标系xOy中,圆C的参数方程为x=2+2cosαy=2sinα(其中α为参数),以坐标原点 2020-07-30 …
在直角坐标系xOy中,椭圆C的参数方程为x=acosθy=bsinθ(φ为参数,a>b>0).在极 2020-07-31 …
以坐标原点O为极点,x轴的正半轴为极轴建立极坐标系,已知曲线C的极坐标方程为ρ=4cosθ,曲线M 2020-07-31 …
在直角坐标系xOy中,圆C的参数方程为(其中为参数).以坐标原点O为极点,x轴的正半轴为极轴建立极 2020-07-31 …
选修4-4:坐标系与参数方程选讲.在极坐标系中,O为极点,半径为2的圆C的圆心的极坐标为(2,π3 2020-07-31 …
在直角坐标系xOy中,直线l的方程是y=6,圆C的参数方程是x=cosφy=1+sinφ(φ为参数 2020-07-31 …
图h是一台发电机定子o的磁场分布图,其oN、S是永久磁铁的两个磁极,它们的表面呈半圆柱面形状.M是圆 2020-12-22 …