早教吧作业答案频道 -->化学-->
白云石粉是生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某兴趣小组进行探究.查阅资料]白云石属于碳酸盐矿物,主要成分的化学式可表示为:xMgCO3•yCaCO3.(杂质是二氧化硅,其不
题目详情
白云石粉是生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某兴趣小组进行探究.
查阅资料]白云石属于碳酸盐矿物,主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
Ⅰ定性探究:白云石粉的成分
[实验分析]
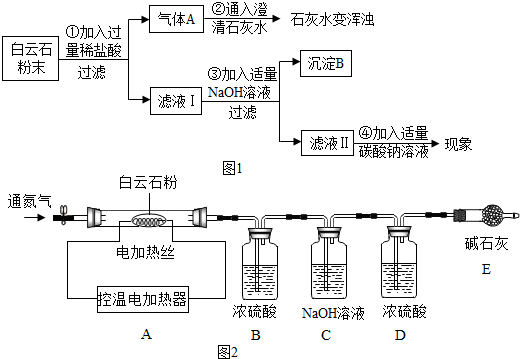
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、___.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是___(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是___.步骤④的反应现象是___.
[结 论]白云石由碳酸钙、碳酸镁组成.
[实验质疑]因氢氧化钙微溶于水,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
Ⅱ定量探究:白云石的组成
[查阅资料]碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
[实验设计]为测定白云石中的含钙量及x:y的值,该小组设计了如图2装置并进行实验:
[实验步骤]
①组装仪器,检查装置的气密性;
②准确称取30.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量;
③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;
④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量;
⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量.
实验数据记录如表:
[实验分析和数据处理]
(4)装置D的作用是___;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是___.
(6)计算白云石中钙元素的质量分数.(写出计算过程,3分):
(7)设计实验证明白云石粉已完全分解的实验方法是___(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=___(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值___ (填偏大、偏小或不变).
查阅资料]白云石属于碳酸盐矿物,主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
Ⅰ定性探究:白云石粉的成分
[实验分析]

(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、___.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是___(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是___.步骤④的反应现象是___.
[结 论]白云石由碳酸钙、碳酸镁组成.
[实验质疑]因氢氧化钙微溶于水,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
Ⅱ定量探究:白云石的组成
[查阅资料]碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
[实验设计]为测定白云石中的含钙量及x:y的值,该小组设计了如图2装置并进行实验:
[实验步骤]
①组装仪器,检查装置的气密性;
②准确称取30.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量;
③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;
④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量;
⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量.
实验数据记录如表:
| 装置 | B/g | C/g | D/g | E/g |
| 反应前 | 150.0 | 200.0 | 150.0 | 120.5 |
| 700℃ | 150.0 | 208.4 | 150.4 | 120.5 |
| 1000℃ | 150.0 | 212.6 | 150.6 | 120.5 |
(4)装置D的作用是___;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是___.
(6)计算白云石中钙元素的质量分数.(写出计算过程,3分):
(7)设计实验证明白云石粉已完全分解的实验方法是___(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=___(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值___ (填偏大、偏小或不变).
▼优质解答
答案和解析
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、漏斗.
故填:漏斗.
(2)碳酸根离子能和氢离子结合成水和二氧化碳,因此由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-.
故填:CO32-.
(3)步骤③中,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,实验现象是产生白色沉淀.
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;产生白色沉淀.
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小.
故填:吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小.
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
故填:使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)设碳酸钙的质量为x,
碳酸钙分解生成二氧化碳质量是4.4g,
CaCO3
CaO+CO2↑,
100 44
x 4.4g
=
,
x=10g,
ω(Ca)═(10g×40%)/30g═13.3%
答:白云石中钙元素的质量分数为13.3%.
(7)实验证明白云石粉已完全分解的实验方法是:取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解.
故填:取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解.
(8)设碳酸镁质量为y,
碳酸镁分解生成二氧化碳的质量是2.2g,
MgCO3
MgO+CO2↑,
84 44
y 2.2g
=
,
y=4.2g,
根据题意有:
=
,
=
,
若加热前没有鼓入一段时间的氮气,或导致碳酸镁分解生成的二氧化碳质量偏大,从而会导致x:y的值偏大.
故填:1:2;偏大.
故填:漏斗.
(2)碳酸根离子能和氢离子结合成水和二氧化碳,因此由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-.
故填:CO32-.
(3)步骤③中,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,实验现象是产生白色沉淀.
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;产生白色沉淀.
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小.
故填:吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小.
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
故填:使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)设碳酸钙的质量为x,
碳酸钙分解生成二氧化碳质量是4.4g,
CaCO3
| ||
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g,
ω(Ca)═(10g×40%)/30g═13.3%
答:白云石中钙元素的质量分数为13.3%.
(7)实验证明白云石粉已完全分解的实验方法是:取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解.
故填:取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解.
(8)设碳酸镁质量为y,
碳酸镁分解生成二氧化碳的质量是2.2g,
MgCO3
| ||
84 44
y 2.2g
| 84 |
| y |
| 44 |
| 2.2g |
y=4.2g,
根据题意有:
| 84x |
| 100y |
| 4.2g |
| 10g |
| x |
| y |
| 1 |
| 2 |
若加热前没有鼓入一段时间的氮气,或导致碳酸镁分解生成的二氧化碳质量偏大,从而会导致x:y的值偏大.
故填:1:2;偏大.
看了白云石粉是生产高级玻璃器皿、医...的网友还看了以下:
已知球O的球面有四点S,A,B,C,其中O,A,B,C,四点共面,△ABC是边长为2的已知球O的球 2020-04-26 …
第二次 makefile 提示 make:`myapp' is up to date,myapp 2020-05-16 …
已知平面上有四点O,A,B,C,其中O是正三角形ABC的外心,且满足OC乘以OA=-1,则△ABC 2020-06-02 …
已知:以点C(t,t/2)(t属于R且不等于O)为圆心的圆与x轴交与O,A,与y轴相交与点O,B, 2020-06-06 …
已知椭圆(a>b>0)经过点,其离心率为.(Ⅰ)求椭圆C的方程;(Ⅱ)设直线l与椭圆C相交于A、B 2020-06-18 …
[2014·江门模拟]如图,矩形O′A′B′C′是水平放置的一个平面图形的直观图,其中O′A′=6 2020-06-19 …
(2013•奉贤区二模)如图,已知AB是⊙O的直径,AB=8,点C在半径OA上(点C与点O、A不重 2020-07-29 …
(2013•南京二模)如图,某广场中间有一块扇形绿地OAB,其中O为扇形所在圆的圆心,∠AOB=6 2020-07-31 …
已知以点C(t,2/t)),(t>0)为圆心的圆与与X轴交与O,A,与Y轴交与点O,B其中O为坐标 2020-08-02 …
如图,己知AB是O的直径,且AB=4,点C在半径OA上(点C与点O、点A不重合),过点C作AB的垂线 2021-01-12 …