早教吧作业答案频道 -->化学-->
将一定体积的CO2通入到一定浓度的NaOH溶液中,为了测定其溶液的成分,向该溶液中逐滴加入1mol•L-1盐酸.所加入盐酸的体积与产生CO2气体体积(标准状况)的关系如图所示.(1)写出OA段
题目详情
将一定体积的CO2通入到一定浓度的NaOH溶液中,为了测定其溶液的成分,向该溶液中逐滴加入1mol•L-1盐酸.所加入盐酸的体积与产生CO2气体体积(标准状况)的关系如图所示.
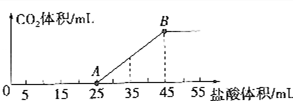
(1)写出OA段所发生反应的离子方程式:___.
(2)当加入35mL盐酸时,所产生的CO2的体积是___mL(标准状况).
(3)溶液中所含的物质有___,其物质的量之比为___.

(1)写出OA段所发生反应的离子方程式:___.
(2)当加入35mL盐酸时,所产生的CO2的体积是___mL(标准状况).
(3)溶液中所含的物质有___,其物质的量之比为___.
▼优质解答
答案和解析
(1)在溶液中碳酸氢钠与氢氧化钠反应生成碳酸钠,结合图象可知,开始没有二氧化碳气体生成,则制成的稀溶液中的溶质为碳酸钠和氢氧化钠,则OA段0~5mL先发生酸碱中和,其离子反应方程式为H++OH-═H2O,再发生碳酸钠与盐酸反应生成碳酸氢钠与氯化钠,其离子反应方程式为CO32-+H+═HCO3-,
故答案为:H++OH-═H2O;CO32-+H+═HCO3-;
(2)结合图象可知,当加入35mL盐酸时,25~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体,设生成二氧化碳的物质的量为n,生成气体时消耗的酸的物质的量为(35-25)×10-3L×1mol•L-1=0.01mol,则
HCO3-+H+═CO2↑+H2O
1 1
0.01mol n
,所以n=0.01mol,标准状况下其体积为0.01mol×22.4L/mol=0.224L=224mL,故答案为:224;
(3)溶液中所含的物质有碳酸钠和氢氧化钠,由图可知氢氧化钠消耗盐酸的体积为5ml,而碳酸钠生成碳酸氢钠消耗盐酸为:20ml,碳酸钠和氢氧化钠与盐酸都是1:1反应,所以其物质的量之比等于消耗盐酸的体积之比,则物质的量之比为5:20=1:4,故答案为:氢氧化钠和碳酸钠;1:4.
故答案为:H++OH-═H2O;CO32-+H+═HCO3-;
(2)结合图象可知,当加入35mL盐酸时,25~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体,设生成二氧化碳的物质的量为n,生成气体时消耗的酸的物质的量为(35-25)×10-3L×1mol•L-1=0.01mol,则
HCO3-+H+═CO2↑+H2O
1 1
0.01mol n
,所以n=0.01mol,标准状况下其体积为0.01mol×22.4L/mol=0.224L=224mL,故答案为:224;
(3)溶液中所含的物质有碳酸钠和氢氧化钠,由图可知氢氧化钠消耗盐酸的体积为5ml,而碳酸钠生成碳酸氢钠消耗盐酸为:20ml,碳酸钠和氢氧化钠与盐酸都是1:1反应,所以其物质的量之比等于消耗盐酸的体积之比,则物质的量之比为5:20=1:4,故答案为:氢氧化钠和碳酸钠;1:4.
看了 将一定体积的CO2通入到一定...的网友还看了以下:
已知数列{An}满足A(n+1)=an+2*(3^n)+1,a1=3,求{An}原式得:An=A( 2020-05-13 …
已知函数f(x)=x/(2*x+1),数列{an}满足a[1]=1/2,a[n+1]=f(a[n] 2020-05-13 …
(1)在等差数列{an}中,是否有an=(a(n-1)+a(n+1))/2(n≥2)?(2)在数列 2020-05-14 …
(1)在等差数列{an}中,是否有an=(a(n-1)+a(n+1))/2(n≥2)?(2)在数列 2020-05-14 …
立方差公式的推广证明过程(1)a^n-b^n=(a-b)[a^(n-1)+a^(n-2)*b+.. 2020-07-11 …
基本不等式设数列a(n),b(n),且a(1)>b(1)>0,a(n)=(a(n-1)+b(n-1 2020-08-03 …
lim[cos(u/4n)+cos(3u/4n)+.+cos(2n-1)u/4n]/n这里n趋于无穷 2020-11-01 …
已知数列{an}满足a1=1,(a(n-1)+1)/an=(a(n-1)+1)/(1-an),(n∈ 2020-11-19 …
定义运算#:a#1=aa#n=2×a#(n-1)+a,n>1已知m#4=30,(1)m=————(2 2020-11-24 …
已知数列{a(n)}的前n项和为S(n),且满足a(1)=1,a(n+1)=S(n)+1(n∈N(+ 2021-02-09 …