将Na2O2与NaHCO3的均匀混合物粉末分成等质量的两份,其中一份加入100mL盐酸使其充分反应,溶液呈中性,放出气体2.24L(标准状况);将生成的气体通入另一份混合物中充分反应后
(1)混合物中Na 2 O 2 和NaHCO 3 的物质的量之比。
(2)加入盐酸的物质的量浓度。
(1)2:9或8:1
(2)1.3 mol·L -1 或3.4 mol·L -1
解析:(1)若Na 2 O 2 在反应中未完全消耗完,设混合物中含NaHCO 3 的物质的量为x,消耗的CO 2 物质的量为y
2Na 2 O 2 +2CO 2 ![]() 2Na 2 CO 3 +O 2 Δn
2Na 2 CO 3 +O 2 Δn
2 mol 1 mol 1 mol
Y ![]() =0.01 mol
=0.01 mol
则y=0.02 mol
NaHCO 3 +HCl![]() NaCl+CO 2 ↑+H 2 O
NaCl+CO 2 ↑+H 2 O
1 mol 1 mol
x 0.02 mol
则x=0.02 mol
Na 2 O 2 的物质的量为(![]() -0.02 mol)×2=(0.1 mol-0.02 mol)×2=0.16 mol
-0.02 mol)×2=(0.1 mol-0.02 mol)×2=0.16 mol
Na 2 O 2 与NaHCO 3 的物质的量之比为0.16 mol:0.02 mol=8:1
因为溶液里正负电荷守恒,n(Na + )=n(Cl - ),所以加入盐酸的物质的量浓度为:
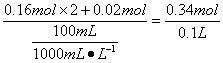 =3.4 mol·L -1
=3.4 mol·L -1
(2)若Na 2 O 2 全部消耗完,设Na 2 O 2 的物质的量为x′,O 2 的物质的量为y′
2Na 2 O 2 +2CO 2 ![]() 2Na 2 CO 3 +O 2 Δn
2Na 2 CO 3 +O 2 Δn
2 mol 2 mol 1 mol 1 mol
x′ y′ ![]() =0.01 mol
=0.01 mol
则x′=0.02 mol y′=0.01 mol
CO 2 的物质的量为:![]() -0.01 mol=0.1 mol-0.01 mol=0.09 mol
-0.01 mol=0.1 mol-0.01 mol=0.09 mol
n(NaHCO 3 )=n(CO 2 )=0.09 mol
Na 2 O 2 与NaHCO 3 的物质的量之比为0.02 mol:0.09 mol=2:9
加入盐酸的物质的量浓度为:
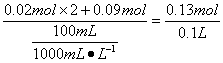 =1.3 mol·L -1 .
=1.3 mol·L -1 .
长为8m宽为6m高为5m的仓库在其内壁的点A有一只壁虎,在点B一只蚊子.则壁虎到蚊子最短距离为如图是 2020-03-31 …
如图是一个长为8m,宽为6m,高为5m的仓库,在其内壁的点A(长的四等分点)处有一只壁虎.在点B(宽 2020-03-31 …
数学中的“三等分线”用英语怎么说?我知道二等分线是bisector像三等分线、四等分线、五等分线… 2020-06-05 …
如图,线段AB和CD垂直且相等.点E、F、G是线段AB的四等分点,点E、H是线段CD的三等分点.从 2020-06-12 …
AB是圆O的直径,其长为1,它的三等分点分别为C与D,在AB的两侧以AC、AD、CB、DB为直径分 2020-06-13 …
急!地理问题求中国地理的的各种等分线,和其等分线等分什么如秦岭-淮河等分线等分. 2020-06-14 …
一根粗细均匀的电阻丝,阻值为25Ω,将其等分成五段,然后并联使用,则其等效电阻是()A.1/25Ω 2020-06-17 …
1、在一段绳子的二等分点、三等分点、四等分点、五等分点、六等分点处都做上记号,然后在所有记号处剪开 2020-06-19 …
CAXA2013怎样绘制角等分线CAXA2013怎样绘制大角度等分线,大于180度角的角等分线怎样 2020-06-27 …
有一个无盖的立方体水箱,其侧面一条高上的三等分除开两个排水孔A和B,已知两空的排水速度相同,现在从 2020-07-08 …