工业上生产4J29合金(铁、钴、镍合金)废物中提取钴和镍,一般是用H2SO4溶解合金使其成为Fe2+、Co2+和Ni2+,再将Fe2+氧化成Fe3+,从而使Fe3+转化为某种沉淀析出,从而达
| | | 工业上生产4J29合金(铁、钴、镍合金)废物中提取钴和镍,一般是用H 2 SO 4 溶解合金使其成为Fe 2+ 、Co 2+ 和Ni 2+ ,再将Fe 2+ 氧化成Fe 3+ ,从而使Fe 3+ 转化为某种沉淀析出,从而达到与Co 2+ 和Ni 2+ 分离的目的,生产上要实现上述氧化过程,可采用加入NaClO或NaClO 3 溶液(均含有少量的H 2 SO 4 ). 阅读材料:生产上除去溶液中Fe 3+ 的一般方法是:控制溶液的pH=1 . 6~1 . 8,温度在85℃~95℃时,使Fe 3+ 在热的溶液中发生水解,最终生成沉淀除去. | | (1) | | 上述反应可用以下化学反应式表示: NaClO+FeSO 4 +H 2 SO 4 NaCl+Fe 2 (SO 4 ) 3 +H 2 O NaClO 3 +FeSO 4 +H 2 SO 4 NaCl+Fe 2 (SO 4 ) 3 +H 2 O(均未配平) 请问:若从化学反应的反应物计量关系上看,应选择何种氧化剂?并说明理由:________ | | | (2) | | 通过阅读材料,若利用离子水解使Fe 3+ 与Co 2+ 和Ni 2+ 分离还需要知道什么信息? ________ | | | (3) | | 配平下列离子方程式,并回答下列有关问题: 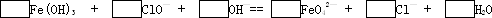 若已知有3 . 21gFe(OH) 3 参加反应,则电子转移了 ________ 个. | | |
答案和解析
答案:解析:(1) NaClO3,因为与相同量的Fe2+反应,NaClO3用量少; (2) 应知道此温度下,溶液中Co2+和Ni2+能完全水解的pH值; (3) 2Fe(OH)3+3ClO?/SUP>+4OH?/SUP>====2FeO42?/SUP>+3Cl?/SUP>+5H2O,0.09NA或5.418×1022
A、D、E、F为氧化物,B、C为单质,C不能与稀硫酸反应.F与A的组成元素相同,F的相对分子质量为 2020-05-15 …
求助高一数学:两个事件E,F,P(F|E)=0.45,比较P(非F|E)与0.55的大小1.两个事 2020-06-10 …
若f(u)可导,且y=f(e^x),则有(),为什么A.dy=f'(e^x)dxB.dy=f'(e 2020-06-12 …
f(x)是可微的,则df(e^x)=()A.f'(x)e^xdxB.f'(e^x)dxC.f'(e 2020-06-13 …
函数f(e^x-1)=x^2+1,则f(x)的定义域为e的x次方再减去1 2020-06-25 …
问一道数学题,科大上p175我这样做的:(1)将等式两边求导:1=f`*e^f+f*e^f*f`= 2020-07-18 …
EXCEL循环或计算问题。F=A+B+C+D+E。(A.B.C.D.E.F.均要大于零)E=A*10 2020-11-01 …
函数题,最短路径已知点A(0,3)和点B(0,1),若一个动点P从点B出发,先到达x轴上的某点(设为 2020-11-26 …
检验电荷的电荷量为什么要足够小E不是等于F/q的么?F=KQq/RRF再除以一个q得到E也就是说E的 2020-12-09 …
英语向高人求教!写几句话.每句开头的第一个字母分别是“L,i,U,F,E,i,F,E,i,w,o,a 2020-12-15 …