早教吧作业答案频道 -->化学-->
电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:①第一段:NaCN+NaClO→NaOCN+NaCl②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)完成下列填空:(1)上述反应涉及的元素中,氮原子核
题目详情
电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外未成对电子数是___个;O2-、Na+、Cl-中半径最小的是___.
(2)NaCN晶体中含有的化学键类型为___.
(3)第二段过程中,产物属于共价化合物的电子式是___,其属于___(填“极
性”或“非极性”)分子.
(4)已知:NaOCN中N元素为-3价.配平第二段过程的化学方程式并标出电子转移的方向和数目.___
(5)综合两段反应,处理含有0.01mol NaCN的废水,至少需NaClO___mol.
(6)请用一个方程式证明氮的非金属性大于碳:___.
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外未成对电子数是___个;O2-、Na+、Cl-中半径最小的是___.
(2)NaCN晶体中含有的化学键类型为___.
(3)第二段过程中,产物属于共价化合物的电子式是___,其属于___(填“极
性”或“非极性”)分子.
(4)已知:NaOCN中N元素为-3价.配平第二段过程的化学方程式并标出电子转移的方向和数目.___
(5)综合两段反应,处理含有0.01mol NaCN的废水,至少需NaClO___mol.
(6)请用一个方程式证明氮的非金属性大于碳:___.
▼优质解答
答案和解析
(1)N原子的2p轨道上有3个单电子,所以氮原子核外未成对电子数是3;电子层数越多半径越大,电子层数相同时,原子序数越大,半径越小,则O2-、Na+、Cl-中半径关系为:Cl->O2->Na+,即Na+的半径最小;
故答案为:3;Na+;
(2)NaCN晶体中钠离子与CN-之间存在离子键,C与N之间存在共价键;
故答案为:离子键、共价键;
(3)第二段过程中,产物属于共价化合物的是CO2,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为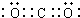 ,分子构型为直线型,结构对称为非极性分子;
,分子构型为直线型,结构对称为非极性分子;
故答案为: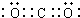 ;非极性;
;非极性;
(4)NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑反应中NaClO中Cl元素的化合价降低2价,NaOCN中N元素的化合价升高3价,配平方程式为:2NaOCN+3NaClO=Na2CO3+CO2↑+3NaCl+N2↑,反应中转移电子数为6,则标出电子转移的方向和数目为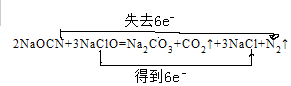 ;
;
故答案为: ;
;
(5)已知反应方程式为①NaCN+NaClO=NaOCN+NaCl,②第二段:2NaOCN+3NaClO=Na2CO3+CO2↑+3NaCl+N2↑,
0.01mol NaCN发生①消耗0.01molNaClO,生成0.01molNaOCN,发生②消耗0.015molNaClO,所以处理含有0.01mol NaCN的废水,至少需NaClO为0.025mol;
故答案为:0.025;
(6)元素的非金属性越强,其最高价含氧酸的酸性越强,证明氮的非金属性大于碳,则证明硝酸的酸性大于碳酸即可,由方程式Na2CO3+2HNO3=NaNO3+H2O+CO2↑可知,硝酸的酸性大于碳酸;
故答案为:Na2CO3+2HNO3=NaNO3+H2O+CO2↑.
故答案为:3;Na+;
(2)NaCN晶体中钠离子与CN-之间存在离子键,C与N之间存在共价键;
故答案为:离子键、共价键;
(3)第二段过程中,产物属于共价化合物的是CO2,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为
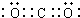 ,分子构型为直线型,结构对称为非极性分子;
,分子构型为直线型,结构对称为非极性分子;故答案为:
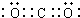 ;非极性;
;非极性;(4)NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑反应中NaClO中Cl元素的化合价降低2价,NaOCN中N元素的化合价升高3价,配平方程式为:2NaOCN+3NaClO=Na2CO3+CO2↑+3NaCl+N2↑,反应中转移电子数为6,则标出电子转移的方向和数目为
 ;
;故答案为:
 ;
;(5)已知反应方程式为①NaCN+NaClO=NaOCN+NaCl,②第二段:2NaOCN+3NaClO=Na2CO3+CO2↑+3NaCl+N2↑,
0.01mol NaCN发生①消耗0.01molNaClO,生成0.01molNaOCN,发生②消耗0.015molNaClO,所以处理含有0.01mol NaCN的废水,至少需NaClO为0.025mol;
故答案为:0.025;
(6)元素的非金属性越强,其最高价含氧酸的酸性越强,证明氮的非金属性大于碳,则证明硝酸的酸性大于碳酸即可,由方程式Na2CO3+2HNO3=NaNO3+H2O+CO2↑可知,硝酸的酸性大于碳酸;
故答案为:Na2CO3+2HNO3=NaNO3+H2O+CO2↑.
看了 电镀废水中常含有剧毒的NaC...的网友还看了以下:
已知平面上的直线l及点p,在l上任取一点Q,线段PQ长度最小值称为点p到直线l的距离,记作d(p, 2020-05-17 …
已知线段AB和直线l,过A、B两点作圆,并使圆心在l上当L与AB斜交时,可以作几个这样的圆?当l垂 2020-06-04 …
在Rt△ABC中,BC=AC,∠ACB=90°,点D为射线AB上一点,连接CD,过点C作线段CD的 2020-07-21 …
如图所示,内径均匀的L形玻璃管,A端封闭,D端开口,AC段水平,CD段竖直.AB段长L1=30cm 2020-07-31 …
L为x轴上从(0,0)到(1,0)点的一段有向线段,则∫L(x+3y^2)dx,初学,求详解,公式 2020-08-02 …
截取一段长为l(L的小写)的吸管,找一直径为D的钢珠,把钢珠放在吸管上方,再测出管底到球顶部的高度L 2020-11-05 …
(2013•乐山)如图,已知线段AB.(1)用尺规作图的方法作出线段AB的垂直平分线l(保留作图痕迹 2020-11-06 …
如图,已知线段AB。(1)用尺规作图的方法作出线段AB的垂直平分线l(保留作图痕迹,不要求写出作法) 2020-11-06 …
1.求带电线段(L,)延长线上距离端点a处的电场强度2.求带电线段(2L,)中垂线上任意一点电场 2020-11-24 …
1过点P(-1,2)的直线l与x轴和y轴分别交与A,B两点.若点P恰为线段AB的中点,求直线l的斜率 2021-01-10 …