常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数〔分布系数)随PH变化的关系如图所示.下列表述不正确的是()A.HC2O4-⇌H++C2O42-,K=1×10-4.3B.将等物质的量的NaH
常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数〔分布系数)随PH变化的关系如图所示.下列表述不正确的是( )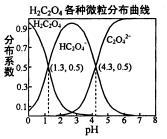
A. HC2O4-⇌H++C2O42-,K=1×10-4.3
B. 将等物质的量的NaHC2O4、NAa2C2O4溶于水中,所得溶液PH恰好为4.3
C. 常温下HF的KB=1×10--3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
D. 在0.1mol/LNaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-)
| c(H+)×c(C2O42-) |
| c(HC2O4-) |
| c(H+)×c(C2O42-) |
| c(HC2O4-) |
B.将等物质的量的NaHC2O4、Na2C2O4溶于水中,HC2O4-电离程度大于C2O42-的水解程度,所以溶液中c(C2O42-)>c(HC2O4-),则溶液PH大于4.3,故B错误;
C.常温下H2C2O4的K1=10-1.3,K2=10-4.3,HF的KB=1×10-3.45,则酸性:H2C2O4>HF>HC2O4-,所以将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为H2C2O4+F-=HF+HC2O4-;故C正确;
D.NaHC2O4溶液显酸性,以HC2O4-的电离为主,在溶液中部分电离HC2O4-,则各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-),故D正确.
故选B.
已知t℃时,盐M(不含结晶水,相对分子质量为126)的溶解度为S克.在一定量的M的水溶液中加入ag 2020-04-13 …
热敏电阻的阻值会随温度的改变而改变.小明同学用甲图所示的电路来探究热敏电阻RT的阻值与温度的关系. 2020-05-14 …
密度分别为p1和p2的两种液体,已知p1>p2,分别以等体积和等质量混合成体积相等的甲、乙两瓶混合 2020-05-20 …
浮力计算题及答案将质量为300克物体M放在盛满某种液体的容器中,无块M有一半体积浮出页面.先将无块 2020-06-07 …
有三种不同的液体,它们密度分别为p1=1.7*10³kg/m³,p2=1.3*10³kg/m³,p 2020-06-07 …
向盛有10mLlmol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质 2020-07-21 …
如图为某固体溶解度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的 2020-07-29 …
一种药在病人血液中的含量不低于2克时,它才能起到有效治疗的作用,已知每服用m(1≤m≤4且m∈R)个 2020-11-15 …
一容器中装有某种液体,测得液体的体积为V,液体与容器的总质量为m,改变液体的体积,重复上述实验,得到 2020-12-07 …
请问0.5M的蔗糖溶液中的M是什么意思是mol/L吗? 2021-02-05 …