早教吧作业答案频道 -->化学-->
FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们
题目详情
FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
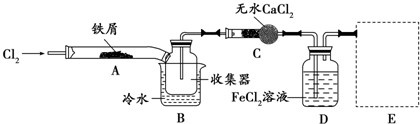
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为___.
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端.要使沉积的FeCl3进入收集器,第④步操作是___.
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)___.
(4)装置B中冷水浴的作用为___;装置C的名称为___;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:___.
(5)在虚线框中画出尾气吸收装置E并注明试剂.
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液.
(6)FeCl3与H2S反应的离子方程式为___.
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为___.
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;
②___.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为___.
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端.要使沉积的FeCl3进入收集器,第④步操作是___.
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)___.
(4)装置B中冷水浴的作用为___;装置C的名称为___;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:___.
(5)在虚线框中画出尾气吸收装置E并注明试剂.
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液.
(6)FeCl3与H2S反应的离子方程式为___.
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为___.
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;
②___.
▼优质解答
答案和解析
Ⅰ.(1)氯气具有强氧化性,将有变价的铁元素氧化成高价铁,生成氯化铁,所以装置A中铁与氯气反应生成氯化铁,反应为2Fe+3Cl2
2FeCl3,
故答案为:2Fe+3Cl2
2FeCl3;
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,第④步操作是对FeCl3加热发生升华使沉积的FeCl3进入收集器,
故答案为:在沉积的FeCl3固体下方加热;
(3)为防止FeCl3潮解所采取的措施有②通入干燥的Cl2⑤用干燥的N2赶尽Cl2,
故选:②⑤;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品,装置C的名称为干燥管;Fe2+的检验可通过与赤铁盐(K3)生成蓝色沉淀(腾化盐)的方法来完成,
故答案为:冷却,使FeCl3沉积,便于收集产品;干燥管;K3溶液;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可以用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,尾气吸收装置E为: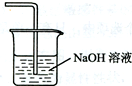 ,
,
故答案为: .
.
Ⅱ.(6)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应:2FeCl3+3H2S=2FeCl2+6HCl+3S↓,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
(7)电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应:Fe2+-e-=Fe3+,
故答案为:Fe2+-e-=Fe3+;
(8)电解池中最终得到的FeCl3可重新用来吸收H2S,得到循环利用,
故答案为:FeCl3可以循环利用.
| ||
故答案为:2Fe+3Cl2
| ||
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,第④步操作是对FeCl3加热发生升华使沉积的FeCl3进入收集器,
故答案为:在沉积的FeCl3固体下方加热;
(3)为防止FeCl3潮解所采取的措施有②通入干燥的Cl2⑤用干燥的N2赶尽Cl2,
故选:②⑤;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品,装置C的名称为干燥管;Fe2+的检验可通过与赤铁盐(K3)生成蓝色沉淀(腾化盐)的方法来完成,
故答案为:冷却,使FeCl3沉积,便于收集产品;干燥管;K3溶液;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可以用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,尾气吸收装置E为:
 ,
,故答案为:
 .
.Ⅱ.(6)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应:2FeCl3+3H2S=2FeCl2+6HCl+3S↓,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
(7)电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应:Fe2+-e-=Fe3+,
故答案为:Fe2+-e-=Fe3+;
(8)电解池中最终得到的FeCl3可重新用来吸收H2S,得到循环利用,
故答案为:FeCl3可以循环利用.
看了 FeCl3在现代工业生产中应...的网友还看了以下:
“定义在R上的奇函数f(x)一定满足关系式()”,请求详解(A)f(x)-f(-x)>0(B)f( 2020-04-26 …
设关系模式R(A,B,C),F是R上成立的FD集,F={B→C),则分解P={AB,BC}相对于F( 2020-05-24 …
关于C是f(x)的重根的条件当且仅当C是f(x)与f‘(x)的公共根时,证明C是f(x)的重根. 2020-06-16 …
求三道函数题目.职高难度.1、已知函数f(x)=ax+c,f(1)=1,f(2)=4.求a与c的值 2020-06-26 …
三角形三个点(a,f(a))(b,f(b))(c,f(c))面积=1/2*行列式,行列式的第一排为 2020-07-25 …
第1题A、f(x)是比g(x)高阶的无穷小B、f(x)是比g(x)低阶的无穷小C、f(x)与g(x 2020-07-30 …
二阶导数问题f(x)在c点导数为f'(c),若f'(c)=0,f''(c)≠0,则c点为f(x)极 2020-07-31 …
对定义在区间I上的函数f(x),若存在开区间(a,b)⊊I和常数C,使得对任意的x∈(a,b)都有 2020-08-01 …
若偶函数f(x)在x≤-1上是增函数,则下列关系中成立的是a.f(2)<f(-3/2)<f(-1) 2020-08-01 …
1)设f(x)在[a,b]上可微,且f(a)=f(b)=0,证明:在(a,b)内存在一点ξ,使f'( 2020-12-28 …