早教吧作业答案频道 -->化学-->
甲同学进行了FeCl2溶液的配制、浓度的测定以及Fe2+还原性的实验,并针对异常现象进行探究.步骤一:甲同学准备用两种方案制取FeCl2.方案1:按如图装置用H2还原无水FeCl3制取.(1)E中盛
题目详情
甲同学进行了FeCl2溶液的配制、浓度的测定以及Fe2+还原性的实验,并针对异常现象进行探究.
步骤一:甲同学准备用两种方案制取FeCl2.
方案1:按如图装置用H2还原无水FeCl3制取.
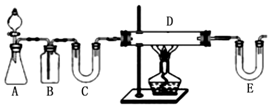
(1)E中盛放的试剂是___;D中反应的化学方程式为___.
方案2:由0.1mol•L-1 FeCl3溶液制取FeCl2溶液,
(2)写出完成上述操作所涉及的离子方程式___.
步骤二:用重铬酸钾法测定方案2所配FeCl2溶液的物质的量浓度.
(3)①若需配制浓度为0.01000mol•L-1的K2Cr2O7标准溶液480mL,实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少___,___.
②本实验滴定过程中操作滴定管的图示正确的是___(填编号).
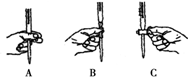
③下列错误的操作使测定的FeCl2溶液浓度偏小的是___
a.若在配制K2Cr2O7标准溶液定容时采取俯视姿势
b.若滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失.
c.锥形瓶洗净后未干燥
步骤三:向2mL FeCl2溶液中滴加2滴0.1mol•L-1KSCN溶液,无现象;再滴加5滴5% H2O2溶液(pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2).
(4)甲同学探究“步骤三”中溶液褪色的原因:
实验I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
实验II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀,并测得生成了两种可直接排放到空气中的气体.
实验III.向2mL 0.1mol•L-1 FeCl3溶液中滴加2滴0.1mol•L-1KSCN溶液,变红,通入O2,无明显变化.
①实验I说明溶液红色褪去是因为SCN-发生了反应而不是Fe3+发生反应.
②实验III的目的是___.
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-和相关气体.写出该反应的离子方程式___.
步骤一:甲同学准备用两种方案制取FeCl2.
方案1:按如图装置用H2还原无水FeCl3制取.

(1)E中盛放的试剂是___;D中反应的化学方程式为___.
方案2:由0.1mol•L-1 FeCl3溶液制取FeCl2溶液,
(2)写出完成上述操作所涉及的离子方程式___.
步骤二:用重铬酸钾法测定方案2所配FeCl2溶液的物质的量浓度.
(3)①若需配制浓度为0.01000mol•L-1的K2Cr2O7标准溶液480mL,实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少___,___.
②本实验滴定过程中操作滴定管的图示正确的是___(填编号).

③下列错误的操作使测定的FeCl2溶液浓度偏小的是___
a.若在配制K2Cr2O7标准溶液定容时采取俯视姿势
b.若滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失.
c.锥形瓶洗净后未干燥
步骤三:向2mL FeCl2溶液中滴加2滴0.1mol•L-1KSCN溶液,无现象;再滴加5滴5% H2O2溶液(pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2).
(4)甲同学探究“步骤三”中溶液褪色的原因:
实验I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
实验II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀,并测得生成了两种可直接排放到空气中的气体.
实验III.向2mL 0.1mol•L-1 FeCl3溶液中滴加2滴0.1mol•L-1KSCN溶液,变红,通入O2,无明显变化.
①实验I说明溶液红色褪去是因为SCN-发生了反应而不是Fe3+发生反应.
②实验III的目的是___.
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-和相关气体.写出该反应的离子方程式___.
▼优质解答
答案和解析
步骤一:(1)方案1:按如图中装置可知,用H2还原无水FeCl3制取无水FeCl2,A装置一般用锌和稀盐酸制备H2,B装置用来除去氢气中的氯化氢,C装置用来干燥氢气,可以装置碱石灰,E装置中也要装置碱石灰,吸收氯化氢气体同时防止空气中的水份进入D装置,D装置中用氢气与氯化氯生成氯化亚,所以E中盛放的试剂是 碱石灰,D中反应的化学方程式为 H2+2FeCl3=2FeCl2+2HCl;
故答案为:碱石灰;H2+2FeCl3=2FeCl2+2HCl;
(2)方案2:由FeCl3溶液制取FeCl2溶液,可以在氯化铁溶液中加入足量铁粉,反应为:2Fe3++Fe=3Fe2+;
故答案为:2Fe3++Fe=3Fe2+;
(3)步骤二:①根据配制一定物质的量浓度溶液的操作步骤可知,配制溶液是需要500 mL容量瓶、胶头滴管、量筒、玻璃棒、烧杯等,在操作滴定管时应用左手握住活塞,手指在另上侧拧开活塞,故选 A;
故答案为:500 mL容量瓶、胶头滴管;A;
②在氧化还原滴定中:
A.若在配制K2Cr2O7标准溶液定容时采取俯视姿势,会使标准液的浓度偏高,导致消耗的标准液的体积偏小,会使测定的FeCl2溶液浓度偏小,故A正确;
B.若滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,使标准液的体积偏大,会使测定的FeCl2溶液浓度偏大,故B错误;
C.锥形瓶洗净后未干燥,对实验没有影响,故选A;
故答案为:A;
(4)步骤三:②根据实验步骤可知,实验III的目的是排除H2O2分解产生的O2氧化SCN-的可能;
在酸性条件下H2O2将SCN-氧化成SO42-和氮气,同时有二氧化碳生成,反应的离子方程式为2SCN-+11H2O2═2SO42-+2H++2 CO2↑+N2↑+10 H2O;
故答案为:排除H2O2分解产生的O2氧化SCN-的可能;2SCN-+11H2O2═2SO42-+2H++2 CO2↑+N2↑+10 H2O.
故答案为:碱石灰;H2+2FeCl3=2FeCl2+2HCl;
(2)方案2:由FeCl3溶液制取FeCl2溶液,可以在氯化铁溶液中加入足量铁粉,反应为:2Fe3++Fe=3Fe2+;
故答案为:2Fe3++Fe=3Fe2+;
(3)步骤二:①根据配制一定物质的量浓度溶液的操作步骤可知,配制溶液是需要500 mL容量瓶、胶头滴管、量筒、玻璃棒、烧杯等,在操作滴定管时应用左手握住活塞,手指在另上侧拧开活塞,故选 A;
故答案为:500 mL容量瓶、胶头滴管;A;
②在氧化还原滴定中:
A.若在配制K2Cr2O7标准溶液定容时采取俯视姿势,会使标准液的浓度偏高,导致消耗的标准液的体积偏小,会使测定的FeCl2溶液浓度偏小,故A正确;
B.若滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,使标准液的体积偏大,会使测定的FeCl2溶液浓度偏大,故B错误;
C.锥形瓶洗净后未干燥,对实验没有影响,故选A;
故答案为:A;
(4)步骤三:②根据实验步骤可知,实验III的目的是排除H2O2分解产生的O2氧化SCN-的可能;
在酸性条件下H2O2将SCN-氧化成SO42-和氮气,同时有二氧化碳生成,反应的离子方程式为2SCN-+11H2O2═2SO42-+2H++2 CO2↑+N2↑+10 H2O;
故答案为:排除H2O2分解产生的O2氧化SCN-的可能;2SCN-+11H2O2═2SO42-+2H++2 CO2↑+N2↑+10 H2O.
看了甲同学进行了FeCl2溶液的配...的网友还看了以下:
要在半径长为1米、圆心角为60°的扇形AOB铁皮上截取一块尽可能大的正方形.小明设计如下两种截取方 2020-05-16 …
下列各句中,没有语病的一句是(3分)A.对调整高考录取方案,有人认为最好能对选修科目按分数划等级, 2020-05-17 …
某机主存的读写周期为1μs,今采用增设Cache 方案和多体交叉存取方案来使其有效访问周期减少到0. 2020-05-26 …
在答题纸图4.2上,计算网络进度计划原始方案各工作的时间参数,确定网络进度计划原始方案的 2020-06-07 …
要在半径长为1米、圆心角为60°的扇形AOB铁皮上截取一块尽可能大的正方形.小明设计如下两种截取方 2020-06-18 …
银行存款利率:整存整取:一年两年三年五年年利率%}2.252.432.72.88王先生有一笔钱存入 2020-07-23 …
要在半径长为1米、圆心角为60°的扇形铁皮(如图)上截取一块面积尽可能大的正方形,请你设计一个截取 2020-07-26 …
下列各句中,没有语病的一句是A.对调整高考录取方案,有人认为最好能对选修科目按分数划等级,有人认为可 2020-12-22 …
如图,正方形卡片A类、B类和长方形卡片C类各若干张(a≠b),如果要选用上述3类卡片共12张拼成一个 2020-12-23 …
建造一个长方体水池,原计划水池深三米,水池周长为1400米,经过研讨,修改原方案,要把长与宽两边都增 2021-01-12 …