早教吧作业答案频道 -->化学-->
倍半硅氧烷在液晶显示、塑料阻燃、生物医用等领域具有重要应用,氢基倍半硅氧烷的分子结构如图A所示,其加热分解产物中SiO2的晶胞结构如图B所示,回答下列问题:(1)基态Si原子的最
题目详情
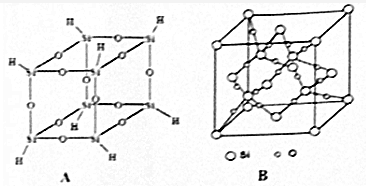
倍半硅氧烷在液晶显示、塑料阻燃、生物医用等领域具有重要应用,氢基倍半硅氧烷的分子结构如图A所示,其加热分解产物中SiO2的晶胞结构如图B所示,回答下列问题:
(1)基态Si原子的最外层电子排布式为___,其中成对电子之间的主要区别是___
(2)图A分子中H的化合价为___,Si原子采用___杂化,形成的极性共价键类型为___;键的极性Si-H键___Si-O(填空“>”、“<”、“=”)
(3)图A分子结构中,一个硅原子被3个___元环共有,硅的配位数为___,该分子的分子式为___
(4)氢基倍半硅氧烷为___晶体,SiO2为___晶体;
(5)每个SiO2晶胞含有Si原子的个数为___;已知SiO2晶体为面心立体结构,晶胞参为anm,阿伏加德罗常数的值为NA,则SiO2晶体的密度为___g•cm-3.

(1)基态Si原子的最外层电子排布式为___,其中成对电子之间的主要区别是___
(2)图A分子中H的化合价为___,Si原子采用___杂化,形成的极性共价键类型为___;键的极性Si-H键___Si-O(填空“>”、“<”、“=”)
(3)图A分子结构中,一个硅原子被3个___元环共有,硅的配位数为___,该分子的分子式为___
(4)氢基倍半硅氧烷为___晶体,SiO2为___晶体;
(5)每个SiO2晶胞含有Si原子的个数为___;已知SiO2晶体为面心立体结构,晶胞参为anm,阿伏加德罗常数的值为NA,则SiO2晶体的密度为___g•cm-3.
▼优质解答
答案和解析
(1)硅原子核外有14个电子,根据核外电子排布规律知,每个电子层上最多排2n2个电子,但最外层不大于8个电子,s能级上最多排2个电子,p能级上最多排6个电子,所以硅原子的最外层电子排布式为3s23p2;根据泡利原理成对电子自旋方向相反,
故答案为:3s23p2;自旋方向相反;
(2)A分子中O原子显-2价,则Si显+4价,H显-1价;Si原子与O原子、O原子形成4个共价键,即含有4个σ电子对,硅原子无孤对电子,所以Si原子采用的杂化类型为sp3杂化;两种元素非金属性差距越大极性越大,Si-O之间的非金属性之差大于Si-H之间的非金属性之差,所以Si-O键的极性强于Si-H键的极性,
故答案为:-1;sp3σ键;<;
(3)A分子结构中Si原子位于顶点,被3个面所共有,每个面含有4个O原子和4个Si原子,共8个原子,硅的配位数为4;A为分子结构式,所有原子均为一个分子共有,分子中含有8个Si原子,8个H原子和12个O原子,故分子的分子式为Si8H8O12,
故答案为:八;4;Si8H8O12;
(4)图A所示为氢基倍半硅氧烷的分子结构,所以则氢基倍半硅氧烷形成的晶体类型为分子晶体,而SiO2为原子晶体,
故答案为:分子;原子;
(5)SiO2晶体为面心立体结构,每个SiO2晶胞含有Si原子的个数为8×
+6×
+4=8,一个晶胞含有8个“SiO2”结构,所以一个晶胞的质量为
=
,晶胞边长为anm,故SiO2晶体的密度ρ=
=
.故答案为:8;
.
故答案为:3s23p2;自旋方向相反;
(2)A分子中O原子显-2价,则Si显+4价,H显-1价;Si原子与O原子、O原子形成4个共价键,即含有4个σ电子对,硅原子无孤对电子,所以Si原子采用的杂化类型为sp3杂化;两种元素非金属性差距越大极性越大,Si-O之间的非金属性之差大于Si-H之间的非金属性之差,所以Si-O键的极性强于Si-H键的极性,
故答案为:-1;sp3σ键;<;
(3)A分子结构中Si原子位于顶点,被3个面所共有,每个面含有4个O原子和4个Si原子,共8个原子,硅的配位数为4;A为分子结构式,所有原子均为一个分子共有,分子中含有8个Si原子,8个H原子和12个O原子,故分子的分子式为Si8H8O12,
故答案为:八;4;Si8H8O12;
(4)图A所示为氢基倍半硅氧烷的分子结构,所以则氢基倍半硅氧烷形成的晶体类型为分子晶体,而SiO2为原子晶体,
故答案为:分子;原子;
(5)SiO2晶体为面心立体结构,每个SiO2晶胞含有Si原子的个数为8×
| 1 |
| 8 |
| 1 |
| 6 |
| 60×8 |
| NA |
| 480 |
| NA |
| m |
| V |
| 480 |
| NA(a×10-7)3 |
| 480 |
| NA(a×10-7)3 |
看了倍半硅氧烷在液晶显示、塑料阻燃...的网友还看了以下:
在下表中,我们把第i行第j列的数记为ai,j(其中i,j都是不大于5的正整数),对于表中的每个数a 2020-05-14 …
如表,在5×5的表格中,用ai,j表示笫i行第i列的格子里的数(其中I,j都是不大于5的正整数), 2020-05-14 …
(1)某溶液中Cl离子、Br离子,I离子的物质的量之比为2:3:4,要使溶液中Cl离子和Br离子、 2020-05-17 …
复数和三角函数问题sin(i*x+t)能不能表示成不含i的形式?其中i是虚数单位我本来的想法是先展 2020-08-02 …
在含3molNaHSO3的溶液中加入含amolNaIO3的溶液充分反应(不考虑I2+I-⇌I3-), 2020-11-01 …
设由正整数构成的数列{an}满足a(10k-9)+a(10k-8)+...+a10k≤19对一切k∈ 2020-11-01 …
(2012•开封模拟)下列反应的离子方程式书写正确的是()A.向AgCl悬浊液中加入饱和NaI溶液: 2020-11-12 …
下图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固 2020-12-05 …
某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为(其中I、II为未知部分的结构) 2020-12-28 …
框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3),E、F、I为无 2021-02-09 …