早教吧作业答案频道 -->化学-->
铵明矾是一种广泛应用于医药、食品、污水处理等多个行业的重要化工产品.高岭土中含有SiO2、Al2O3和少量Fe2O3,下图是以高岭土为原料制备硫酸铝晶体和铵明矾的工艺流程.请回答下列问
题目详情
铵明矾是一种广泛应用于医药、食品、污水处理等多个行业的重要化工产品.高岭土中含有SiO2、Al2O3和少量Fe2O3,下图是以高岭土为原料制备硫酸铝晶体和铵明矾的工艺流程.
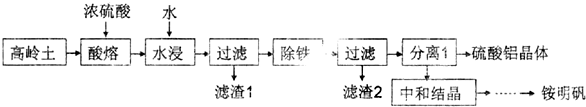
请回答下列问题:
(1)过滤操作中会使用到的玻璃仪器有烧杯、玻璃棒和___.
(2)除铁过程中需要适当调高溶液的pH,则滤渣2的主要成分为___(填化学式),若要检验除铁后的滤液中是否含有Fe3+,可采取的实验操作及现象为___.
(3)实验表明,铵明矾中只含有NH4+、Al3+、SO42-等三种离子,同时含有一定数目的结晶水.某实验小组为进一步测定铵明矾的化学式,首先取9.06g铵明矾配成溶液,然后逐滴加入0.2mol/LNaOH溶液至过量,产生的沉淀质量和加入的NaOH溶液体积关系如下图所示.
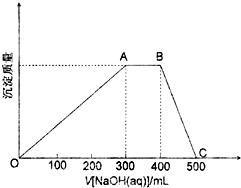
2出图中BC 段对应的化学方程式___.
②根据上图所提供的信息,通过计算求出铵明矾的化学式.(写出计算过程)

请回答下列问题:
(1)过滤操作中会使用到的玻璃仪器有烧杯、玻璃棒和___.
(2)除铁过程中需要适当调高溶液的pH,则滤渣2的主要成分为___(填化学式),若要检验除铁后的滤液中是否含有Fe3+,可采取的实验操作及现象为___.
(3)实验表明,铵明矾中只含有NH4+、Al3+、SO42-等三种离子,同时含有一定数目的结晶水.某实验小组为进一步测定铵明矾的化学式,首先取9.06g铵明矾配成溶液,然后逐滴加入0.2mol/LNaOH溶液至过量,产生的沉淀质量和加入的NaOH溶液体积关系如下图所示.

2出图中BC 段对应的化学方程式___.
②根据上图所提供的信息,通过计算求出铵明矾的化学式.(写出计算过程)
▼优质解答
答案和解析
(1)过滤操作中会使用到的玻璃仪器有烧杯、玻璃棒和漏斗,
故答案为:漏斗;
(2)滤渣2的主要成分为Fe(OH)3;铁离子能和KSCN溶液反应生成血红色溶液,所以要检验除铁后的滤液中是否含有Fe3+,应采取的实验方法为取少量除铁后的滤液于试管中,滴加几滴KSCN溶液,若溶液变为血红色则含Fe3+,否则不含Fe3+;,
故答案为:Fe(OH)3;取少量除铁后的滤液于试管中,滴加几滴KSCN溶液,若溶液变为血红色则含Fe3+,否则不含Fe3+;
(3)①沉淀减少过程(即BC段)中发生反应是氢氧化铝沉淀溶解于氢氧化钠溶液中的反应,反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
②根据图象B→C可知溶解氢氧化铝沉淀用去100mL氢氧化钠溶液,由Al(OH)3+NaOH=NaAlO2+2H2O 计算出n(Al3+)=0.2mol/L×0.1L=0.02mol,A→B沉淀量不变,说明NH4++OH-→NH3.H2O,由此 计算出n(NH4+)=0.2mol/L×0.1L=0.02mol,根据电荷守恒 计算出n(SO42-)=
=0.04mol,根据质量守恒 计算出n(H2O)=
=0.24mol,得n(NH4+):n(Al3+):n(SO42-):n(H2O)=0.02:0.02:0.04:0.24=1:1:2:12,所以铵明矾的化学式为NH4Al(SO4)2•12H2O,
故答案为:NH4Al(SO4)2•12H2O.
故答案为:漏斗;
(2)滤渣2的主要成分为Fe(OH)3;铁离子能和KSCN溶液反应生成血红色溶液,所以要检验除铁后的滤液中是否含有Fe3+,应采取的实验方法为取少量除铁后的滤液于试管中,滴加几滴KSCN溶液,若溶液变为血红色则含Fe3+,否则不含Fe3+;,
故答案为:Fe(OH)3;取少量除铁后的滤液于试管中,滴加几滴KSCN溶液,若溶液变为血红色则含Fe3+,否则不含Fe3+;
(3)①沉淀减少过程(即BC段)中发生反应是氢氧化铝沉淀溶解于氢氧化钠溶液中的反应,反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
②根据图象B→C可知溶解氢氧化铝沉淀用去100mL氢氧化钠溶液,由Al(OH)3+NaOH=NaAlO2+2H2O 计算出n(Al3+)=0.2mol/L×0.1L=0.02mol,A→B沉淀量不变,说明NH4++OH-→NH3.H2O,由此 计算出n(NH4+)=0.2mol/L×0.1L=0.02mol,根据电荷守恒 计算出n(SO42-)=
| 0.02mol+0.02mol×3 |
| 2 |
| 9.06g-0.02mol×27g/mol-0.02mol×18g/mol-0.04mol×96g/mol |
| 18g/mol |
故答案为:NH4Al(SO4)2•12H2O.
看了铵明矾是一种广泛应用于医药、食...的网友还看了以下:
V,D,E,E,E,L,L,L,L,O,O,O,R,R,S,S把所给的字母填入方格中,使横向,纵向 2020-06-06 …
D,E,E,E,L,L,L,L,O,O,O,R,R,S,S,V把所给的字母填入方格中,使横向,纵向 2020-06-06 …
已知A、B、C、D、E、F、G、H、L、K分别代表0至9中的不同数字,且有下列4个等式成立;D-E 2020-06-12 …
三元一次方程组a*x+b*y+c*z+d=0,e*x+f*y+g*z+h=0,i*x+j*y+k* 2020-08-03 …
一.看一看,将下列字母组成单词.1.t,o,e,f,n2.c,s,e,a,b,u,e3.l,e,p, 2020-10-31 …
(2008•揭阳)用你喜欢的方法计算.(e)2e0-2.6×e.l&nb七e;&nb七e;&nb七e 2020-11-12 …
英语:下1.将下联打乱的字母组成单词,并写出汉语意思1.a,e,h,g,c,n[]2.e,i,s,t 2020-12-10 …
科学施肥是实现农业增产的重要手段。硝酸铵()是一种常用的氮肥,其中氮、氢、氧三种元素的质量比为。若要 2020-12-22 …
(2013•青岛)科学施肥是实现农业增产的重要手段.硝酸铵(NH4NO3)是一种常用的氮肥,其中氮、 2020-12-22 …
英语单词排列以下字母排列成一个单词,1.e,n,a,l,r2.a,o,o,l,l,b,f,t3.i, 2020-12-24 …