早教吧作业答案频道 -->化学-->
某研发小组通过下列流程制备碱式次氯酸镁:(1)从上述流程中可以判断,滤液中可回收的主要物质是(2)NaClO用Cl2与NaOH反应制得化学方程式:.(3)有效氯的含量是衡量次氯酸盐氧
题目详情
某研发小组通过下列流程制备碱式次氯酸镁:
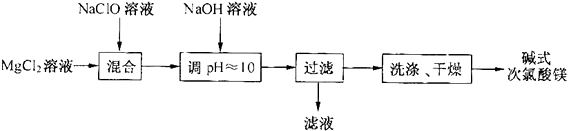
(1)从上述流程中可以判断,滤液中可回收的主要物质是___
(2)NaClO用Cl2与NaOH反应制得化学方程式:___.
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标.次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示:ClO-+Cl-+2H+═Cl2↑+H2O,有效氯含量=
×100%若测得某碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%.通过计算判断该产品中镁和有效氯含量的测定值与理论值相比,是偏高或偏低?(写出计算过程)

(1)从上述流程中可以判断,滤液中可回收的主要物质是___
(2)NaClO用Cl2与NaOH反应制得化学方程式:___.
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标.次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示:ClO-+Cl-+2H+═Cl2↑+H2O,有效氯含量=
| m(Cl2) |
| m(次氯盐酸) |
▼优质解答
答案和解析
向MgCl2溶液中加入NaClO溶液,然后向溶液中加入NaOH溶液并调节溶液的pH,碱式次氯酸镁[Mg2ClO(OH)3•H2O]微溶于水,所以得到碱式次氯酸镁[Mg2ClO(OH)3•H2O]沉淀和NaCl,过滤得到碱式次氯酸镁[Mg2ClO(OH)3•H2O]固体,滤液中成分是NaCl,然后将沉淀洗涤、干燥得到碱式次氯酸镁[Mg2ClO(OH)3•H2O],
(1)滤液中的主要物质是NaCl,所以滤液中可回收的主要物质是NaCl,故答案为:NaCl;
(2)Cl2与NaOH溶液反应生成NaCl、NaClO和H2O,反应方程式为2NaOH+Cl2=NaCl+NaClO+H2O,故答案为:2NaOH+Cl2=NaCl+NaClO+H2O;
(3)Mg2ClO(OH)3•H2O的式量为168.5,Mg2ClO(OH)3•H2O中Mg含量理论值=
=28.49%,某碱式次氯酸镁产品中镁含量为29.01%>28.49%,所以镁含量偏高,
由Mg2ClO(OH)3•H2O~ClO-~Cl2,Mg2ClO(OH)3•H2O中有效氯的理论值=
=42.14%>40.28%,所以偏低,
故答案为:偏高;偏低.
(1)滤液中的主要物质是NaCl,所以滤液中可回收的主要物质是NaCl,故答案为:NaCl;
(2)Cl2与NaOH溶液反应生成NaCl、NaClO和H2O,反应方程式为2NaOH+Cl2=NaCl+NaClO+H2O,故答案为:2NaOH+Cl2=NaCl+NaClO+H2O;
(3)Mg2ClO(OH)3•H2O的式量为168.5,Mg2ClO(OH)3•H2O中Mg含量理论值=
| 24×2 |
| 168.5 |
由Mg2ClO(OH)3•H2O~ClO-~Cl2,Mg2ClO(OH)3•H2O中有效氯的理论值=
| 35.5×2 |
| 168.5 |
故答案为:偏高;偏低.
看了 某研发小组通过下列流程制备碱...的网友还看了以下:
(2009•镇江一模)在化学反应中,只有活化分子才能发生有效碰撞而发生化学反应.使普通分子变成活化 2020-05-14 …
近年来,随着我国经济发展,对原料和能源的进口需求不断增加.其中来自非洲东海岸的货船,最便捷航海线要 2020-05-14 …
电解池原理!精通化学的请进!甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电 2020-05-17 …
选出下列词语解释有错误的一项A、礼尚往来(礼节上重在有来有往)残羹冷炙(吃剩的饭菜,炙:烤肉)国粹 2020-07-01 …
(1)二氧化硫是一种酸性氧化物,具有酸性氧化物的通性.用化学方程式表示二氧化硫具有酸性氧化物的三个 2020-07-25 …
《自己的话是然别人看的》变化是有的,但是美丽并没有变化.中“美丽”是指什么?快. 2020-11-04 …
钢化玻璃俗称普通玻璃的化身,是普通玻璃经一定物理方法处理后得到的.钢化玻璃一般不会发生自爆现象,但当 2020-11-20 …
在进行文化比较时,一个重要的原则是不能有文化中心主义。文化中心主义容易产生偏见,使文化僵化,不能适应 2020-11-20 …
高中物理必修一89页小字里“在超重和失重现象中,地球对物体的实际作用力并没有变化”中“地球对物体的实 2020-12-02 …
在进行文化比较时,一个重要的原则是不能有文化中心主义。文化中心主义容易产生偏见,使文化僵化,不能适应 2021-01-02 …