早教吧作业答案频道 -->化学-->
氢能被视为21世纪最具发展潜力的清洁能源.(1)水制取H2的常见原料,下列有关水的说法正确的是a.水分子是一种极性分子,水分子空间结构呈直线型b.H2O分子中有2个由s轨道与sp3杂化
题目详情
氢能被视为21世纪最具发展潜力的清洁能源.
(1)水制取H2的常见原料,下列有关水的说法正确的是___
a.水分子是一种极性分子,水分子空间结构呈直线型
b.H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H-O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键.
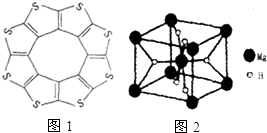
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为___,C16S8中碳硫键键长介于C-S与C=S之间,原因可能是___,C16S8与H2微粒间的作用力是___
②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(.用“→”表示)的氨硼烷的结构式___;与氨硼烷互为等电子体的有机小分子是___(写结构简式).
③一种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进人到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构相似,该晶体储氢后的化学式为___.
④MgH2是金属氢化物储氢材料,其晶胞如图2所示,已知该晶体的密度ag٠cm-3,则晶胞的体积为___cm3〔用含a,、NA的代数式表示,NA表示阿伏伽德罗常数〕.

(1)水制取H2的常见原料,下列有关水的说法正确的是___
a.水分子是一种极性分子,水分子空间结构呈直线型
b.H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H-O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键.
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为___,C16S8中碳硫键键长介于C-S与C=S之间,原因可能是___,C16S8与H2微粒间的作用力是___
②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(.用“→”表示)的氨硼烷的结构式___;与氨硼烷互为等电子体的有机小分子是___(写结构简式).
③一种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进人到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构相似,该晶体储氢后的化学式为___.
④MgH2是金属氢化物储氢材料,其晶胞如图2所示,已知该晶体的密度ag٠cm-3,则晶胞的体积为___cm3〔用含a,、NA的代数式表示,NA表示阿伏伽德罗常数〕.
▼优质解答
答案和解析
(1)a.H2O分子空间结构呈V型,正负电荷中心不重合,属于极性分子,故a错误;
b.H2O分子中2个氢原子的2个由s轨道与氧原子的sp3杂化轨道形成σ键,故b正确;
c.水形成冰晶体是通过氢键作用的,不是H-O键,故c错误;
d.冰晶胞: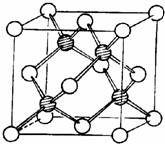 ,干冰晶胞:
,干冰晶胞: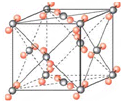 ,即冰晶胞中水分子的空间排列方式与干冰胞不同,故d错误;
,即冰晶胞中水分子的空间排列方式与干冰胞不同,故d错误;
故答案为:b;
(2)①根据图2结构可知:碳原子形成2个C-S,1个C=S二键,C原子杂化轨道数为(2+1)=3,C原子采取sp2杂化方式;
分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质,可导致C16S8中碳硫键键长介于C-S与C=S之间;
分子之间存在范德华力,C16S8与H2微粒间的作用力是范德华力,
故答案为:sp2;分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质;范德华力;
②氮原子提供一对共用电子对给硼原子形成配位键,氨硼烷的结构式为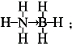 ,等电子体具有相同的电子数目和原子数目,与氨硼烷互为等电子体的有机小分子是CH3CH3,
,等电子体具有相同的电子数目和原子数目,与氨硼烷互为等电子体的有机小分子是CH3CH3,
故答案为: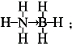 ;CH3CH3;
;CH3CH3;
③CaF2的结构如图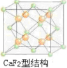 ,根据题意知,该晶胞中铜原子个数=6×
,根据题意知,该晶胞中铜原子个数=6×
=3,金原子个数=8×
=1,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,氢原子相当于该晶胞中的F离子,所以该晶胞中应含有8个H,所以其化学式为Cu3AuH8,
故答案为:Cu3AuH8;
④该晶胞中镁原子个数=
×8+1=2,氢原子个数=4×
+2=4,V=
=
cm3=
cm3,
故答案为:
.
b.H2O分子中2个氢原子的2个由s轨道与氧原子的sp3杂化轨道形成σ键,故b正确;
c.水形成冰晶体是通过氢键作用的,不是H-O键,故c错误;
d.冰晶胞:
 ,干冰晶胞:
,干冰晶胞: ,即冰晶胞中水分子的空间排列方式与干冰胞不同,故d错误;
,即冰晶胞中水分子的空间排列方式与干冰胞不同,故d错误;故答案为:b;
(2)①根据图2结构可知:碳原子形成2个C-S,1个C=S二键,C原子杂化轨道数为(2+1)=3,C原子采取sp2杂化方式;
分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质,可导致C16S8中碳硫键键长介于C-S与C=S之间;
分子之间存在范德华力,C16S8与H2微粒间的作用力是范德华力,
故答案为:sp2;分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质;范德华力;
②氮原子提供一对共用电子对给硼原子形成配位键,氨硼烷的结构式为
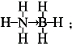 ,等电子体具有相同的电子数目和原子数目,与氨硼烷互为等电子体的有机小分子是CH3CH3,
,等电子体具有相同的电子数目和原子数目,与氨硼烷互为等电子体的有机小分子是CH3CH3,故答案为:
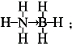 ;CH3CH3;
;CH3CH3;③CaF2的结构如图
 ,根据题意知,该晶胞中铜原子个数=6×
,根据题意知,该晶胞中铜原子个数=6×| 1 |
| 2 |
| 1 |
| 8 |
故答案为:Cu3AuH8;
④该晶胞中镁原子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| ρ |
| ||
| ρ |
| 52 |
| a•NA |
故答案为:
| 52 |
| a•NA |
看了氢能被视为21世纪最具发展潜力...的网友还看了以下:
我问一个问题,说:2.5与2.8哪个大,可不可以这样理解,把2看做整数,小数点后面的5是小数,2在 2020-05-20 …
3.2.1合并同类项与移项的答案一元一次方程第一题,写合并含相同字母的项:(1)2y+3y+6y( 2020-05-23 …
如图1,直线MN与直线AB、CD分别交于点E、F,∠1与∠2互补.(1)试判断直线AB与直线CD的 2020-06-23 …
求1+2+2^2+2^3+2^4+…+2^2014的值.设S=1+2+2^2+2^3+2^4+…+ 2020-07-09 …
观察下列两组算式(2*3)^2与2^2*3^2[(-1/3)*6]^2与(-1/3)^观察下列两组 2020-07-22 …
xyz=1,x+y+z=2,x^2+y^2+z^2=3,求x,y,z我解:xy=1/z,x+y=2- 2020-10-31 …
观察下列各式然后回答问题:1-1/2^2=1/2*2/3,1-1/3^2+2/3*4/3,1-1/4 2020-11-01 …
已知a,b属于正实数a^2+b^2/2=1求y=a√(1+b^2)的最大值参考书上是用y^2=[a√ 2020-12-31 …
这些题怎么数学解1已知(x+m)^2(x^2-2x+3)+x(x+1)中不含x^2项求m的值2已知a 2020-12-31 …
帮解决几道数学题目1、(-27)除与2又1/4乘4/9除与(-24)2、-1又1/5除与(-12)除 2021-01-11 …