早教吧作业答案频道 -->化学-->
废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如图:(1)为确定加入锌灰(主要成分为Zn、
题目详情
废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如图:
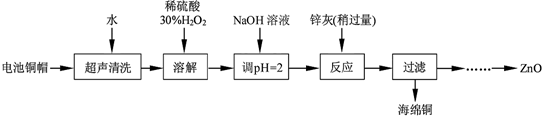
(1)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2;I2+2S2O32-═2I-+S4O62-
①Na2S2O3标准溶液应装在___(填酸式或碱式)滴定管内.
②滴定选用的指示剂为___,滴定终点观察到的现象为___.
③若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会___(填“偏高”“偏低”“不变”).
(2)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀pH范围(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
由除去铜的滤液制备ZnO的实验步骤依次为:
①___;
②___;
③过滤;
④___;
⑤过滤、洗涤、干燥
⑥900℃煅烧.

(1)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2;I2+2S2O32-═2I-+S4O62-
①Na2S2O3标准溶液应装在___(填酸式或碱式)滴定管内.
②滴定选用的指示剂为___,滴定终点观察到的现象为___.
③若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会___(填“偏高”“偏低”“不变”).
(2)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀pH范围(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
①___;
②___;
③过滤;
④___;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
▼优质解答
答案和解析
(1)①Na2S2O3标准溶液因为水解呈碱性,所以要放在碱式滴定管中,故答案为:碱式;②淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,故答案为:淀粉溶液;滴加...
看了废弃物的综合利用既有利于节约资...的网友还看了以下:
已知:有一个数列T,T[n]=1+(j=0到n-1)累计加T[j];且T[0]=1.求证:T[n] 2020-05-14 …
已知:有一个数列T,T[n]=1+(j=0到n-1)累计加T[j];且T[0]=1.求证:T[n] 2020-05-14 …
如图是小明在“探究电磁铁的磁性强弱跟什么因素有关”的实验中自制的电磁铁,电流从A端流入电池,在图中 2020-05-14 …
我想问您,我的N实98值是5.75,N实指数是0.6572,N值(至98年6月缴费年限)18.2, 2020-05-17 …
在比例尺1:200的图纸上,一个长方体的蓄水池长4厘米、宽2厘米、高1.5厘米.这个蓄水池实际占地 2020-06-03 …
实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+.某化学兴 2020-06-05 …
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时电极反 2020-06-14 …
电池的N极S极是什么?干电池和蓄电池都有NS极吗电池的N极S极是什么?干电池和蓄电池都有NS极吗 2020-06-15 …
下列词语的读音完全正确的一组是()A.桃杌(wù)纺缴(zhuó)伺者(cì)杳无音信(yǎo)B 2020-06-21 …
如图,在注满水的游泳池的池底有一点光源A,它到池边的水平距离为3.0m,从点光源A射向池边的光线A 2020-06-23 …