碱式碳酸钴[Cox(OH)y(C03)z]常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。(1)请完成下列
碱式碳酸钴[Cox(OH)y(C03)z]常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
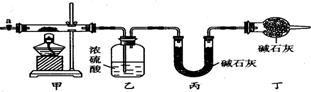
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并 .
③加热甲中玻璃管,当乙装置中 (填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是 o
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的 (填字母)连接在 (填装置连接位置)。
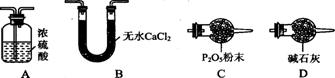
(4)若按正确装置进行实验,测得如下数据。
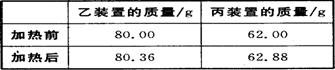
则该碱式碳酸钴的化学式为 。
(5)含有Co(A102)2的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为 。
(6)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如下:
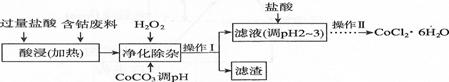
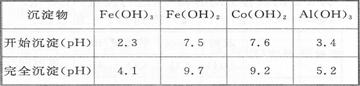
已知:25℃时,Ksp[Fe(OH)3]=2.79X10-39
①净化除杂时,加入H2O2发生反应的离子方程式为
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为 。
③已知:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq)ΔH=akJ/mol
Fe3+(aq)+3OH-(aq)ΔH=akJ/mol
H2O(l)=H+(aq)+OH-(aq)ΔH=b kJ/mol
请写出Fe3+发生水解反应的热化学方程式: .
水解平衡常数Kh= .
④加盐酸调整pH为2~3的目的为 。
⑤操作Ⅱ过程为蒸发浓缩、 (填操作名称)、过滤。
(7)某锂离子电池正极是LiCoO2,含Li+导电固体为电解质。充电时,Li+还原为Li,并以原子形式嵌入电池负极材料C6中(如图所示)。
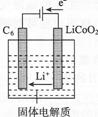
电池反应为LiCoO2+C6![]() CoO2+LiC6,写出该电池放电时的正极反应式: 。
CoO2+LiC6,写出该电池放电时的正极反应式: 。
【答案】(1)②检查装置的气密性③不再有气泡产生时
(2)将装置中生成的CO2和H2O(g)全部排入乙、丙装置中
(3)D 活塞a前(或装置甲前)
(4)Co3(OH)4(CO3)2
(5)蓝色
(6)①2Fe2+(aq)+H2O2+ 2 H+=2Fe3++2H2O ②Al(0H)3、Fe(0H)3
③Fe3+(aq)+3H2O(l)![]() Fe(OH)3(s)+ 3 H+(aq) ΔH=(3b-a) kJ/mol 10-3/2.79 (2分)
Fe(OH)3(s)+ 3 H+(aq) ΔH=(3b-a) kJ/mol 10-3/2.79 (2分)
④抑制CoC12的水解 ⑤冷却结晶
(7)CoO2+Li++e-= LiCoO2
【解析】
试题分析:(1)②装置连接好后,应先检查装置的气密性;③当乙装置中不再产生气体时,说明反应完全,停止加热;
(2)根据题意该物质分解产生三种氧化物,其中有水蒸气和二氧化碳,所以步骤④中缓缓通入空气数分钟的目的是将装置中生成的CO2和H2O(g)全部排入乙、丙装置中,使计算结果准确;
(3)该实验是利用产生的水蒸气和二氧化碳的质量减少其组成,而甲装置前无除去空气中二氧化碳和水蒸气的装置,所以应在甲之前加一装置,除去空气中的二氧化碳和水,与丁装置相同,所以选择D;
(4)根据表中数据生成水蒸气的质量是0.36g,物质的量是0.36g/18g/mol=0.02mol,氢氧根离子的物质的量是0.04mol;生成二氧化碳的质量是0.88g,物质的量是0.88g/44g/mol=0.02mol,碳酸根离子的物质的量是0.02mol;则3.65g固体中钴的物质的量是[3.65g-(0.02mol×2×17g/mol+0.02mol×60g/mol)]/59g/mol=0.03mol,所以化学式中Co、OH-、CO32-的物质的量之比为0.03:0.02×2:0.02=3:4:2,所以该碱式碳酸钴的化学式为Co3(OH)4(CO3)2;
(5)实验室常用透过蓝色钴玻璃片观察钾元素的焰色反应的颜色,所以含有Co(A102)2的玻璃的颜色为蓝色;
(6)①加入过氧化氢的目的是将亚铁离子氧化为铁离子,所以离子方程式为2Fe2+(aq)+H2O2+ 2 H+=2Fe3++2H2O;
②加入CoCO3调pH为5.2~7.6,此时铁离子、铝离子完全沉淀,而钴离子开始沉淀,所以操作I得到滤渣的成分是Al(0H)3、Fe(0H)3;
③铁离子水解的离子方程式为:Fe3+(aq)+3H2O(l)![]() Fe(OH)3(s)+ 3 H+(aq),根据盖斯定律,将已知第一个热化学方程式减去第二个热化学方程式乘以3后所得热化学方程式的逆反应即为Fe3+发生水解反应的热化学方程式,所以答案为Fe3+(aq)+3H2O(l)
Fe(OH)3(s)+ 3 H+(aq),根据盖斯定律,将已知第一个热化学方程式减去第二个热化学方程式乘以3后所得热化学方程式的逆反应即为Fe3+发生水解反应的热化学方程式,所以答案为Fe3+(aq)+3H2O(l)![]() Fe(OH)3(s)+ 3 H+(aq) ΔH=(3b-a) kJ/mol;因为Ksp[Fe(OH)3]=2.79X10-39=c(Fe3+)·c(OH-)3,水解平衡常数Kh= c(H+)3/ c(Fe3+)=Kw3/ Ksp[Fe(OH)3]=10-3/2.79;
Fe(OH)3(s)+ 3 H+(aq) ΔH=(3b-a) kJ/mol;因为Ksp[Fe(OH)3]=2.79X10-39=c(Fe3+)·c(OH-)3,水解平衡常数Kh= c(H+)3/ c(Fe3+)=Kw3/ Ksp[Fe(OH)3]=10-3/2.79;
④因为氯化钴水解使溶液成酸性,所以加盐酸调整pH为2~3的目的为抑制CoC12的水解;
⑤从溶液中得到晶体需要蒸发浓缩、冷却结晶、过滤等,所以操作Ⅱ过程为蒸发浓缩、冷却结晶;
(7)电池放电时,正极发生还原反应,元素的化合价降低,根据所给化学方程式,Co元素的化合价降低,所以CoO2发生还原反应,生成LiCoO2,则放电时的正极反应为CoO2+Li++e-= LiCoO2。
考点:考查工业流程的分析,实验装置的判断、基本操作的判断,溶度积的应用,电化学反应原理的应用
某学生在进行二氧化碳的制取和性质实验时经过认真分析研究对课本中的气体发生装置(如图A)进行了改进( 2020-05-13 …
某数学老师对本校2013届高三学生某次联考的数学成绩进行分析,按1:50进行分层抽样抽取的20名学 2020-05-17 …
某数学老师对本校2013届高三学生某次联考的数学成绩进行分析,按1:50进行分层抽样抽取20名学生 2020-05-17 …
已知ab两地相距50米,机器人从a地出发去b地,规定向右为前进,第一次它前进1米,第二次它后退2米 2020-07-10 …
: 某化学小组用一定量的AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体: 某 2020-07-11 …
已知ab两地相距50米,机器人从a地出发去b地,规定向右为前进,第一次它前进1米,第二次它后退2米 2020-07-30 …
已知ab两地相距50米,机器人从a地出发去b地,规定向右为前进,第一次它前进1米,第二次它后退2米 2020-07-30 …
怎样将CAD图中的某个图件进行"度分秒"旋转RT在某一CAD制图中需要将图中某一条线段或某一部分图 2020-08-01 …
已知ab两地相距50米,机器人从a地出发去b地,规定向右为前进,第一次它前进1米,第二次它后退2米. 2020-11-24 …
自行车前后轮转弯是否在一条线,为什么?自行车的前后轮是不是肯定走出一条线?也就是说,后轮始终是沿着前 2020-11-25 …