早教吧作业答案频道 -->化学-->
试依次回答下列相关问题:(1)磷有两种氧化物P4O6和P4O10,其球棍模型结构如图1所示,其中磷元素的杂化类型分别是、.(2)磷有三种含氧酸H3PO2、H3PO3、H3PO4,其中磷元素均以sp3杂化
题目详情
试依次回答下列相关问题:
(1)磷有两种氧化物P4O6和P4O10,其球棍模型结构如图1所示,其中磷元素的杂化类型分别是___、___.

(2)磷有三种含氧酸H3PO2、H3PO3、H3PO4,其中磷元素均以sp3杂化与相邻原子形成四个σ键,则H3PO3的结构式是___,写出H3PO2与足量氢氧化钠溶液反应的化学方程式___.磷的三种含氧酸H3PO2、H3PO3、H3PO4的酸性强弱顺序为H3PO2<H3PO3<H3PO4,其原因是___.
(3)磷的一种化合物磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成.三溴化硼分子和三溴化磷分子的立体构型分别是___、___.
(4)今有金属钼(Mo)与氯形成的配合物A,在水溶液中完全电离,生成一种简单阴离子和一种阳离子,个数比为4:1.其中阳离子结构呈立方体,十分对称,任意两个相离最远的氯原子的连线为此离子的三重轴,任意两个相离最远的Mo原子的连线为此离子的四重轴(n重轴表示某物质绕此轴旋转360°/n的角度,不能察觉其是否旋转过).
①写出配合物A的化学式___.
②在图2中画出A溶液中阳离子的结构:
③把一种常见含氯的二元化合物的晶胞去掉所有的氯原子,发现剩余部分与A中阳离子的结构竟十分相似.这种常见二元化合物是___.
(1)磷有两种氧化物P4O6和P4O10,其球棍模型结构如图1所示,其中磷元素的杂化类型分别是___、___.

(2)磷有三种含氧酸H3PO2、H3PO3、H3PO4,其中磷元素均以sp3杂化与相邻原子形成四个σ键,则H3PO3的结构式是___,写出H3PO2与足量氢氧化钠溶液反应的化学方程式___.磷的三种含氧酸H3PO2、H3PO3、H3PO4的酸性强弱顺序为H3PO2<H3PO3<H3PO4,其原因是___.
(3)磷的一种化合物磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成.三溴化硼分子和三溴化磷分子的立体构型分别是___、___.
(4)今有金属钼(Mo)与氯形成的配合物A,在水溶液中完全电离,生成一种简单阴离子和一种阳离子,个数比为4:1.其中阳离子结构呈立方体,十分对称,任意两个相离最远的氯原子的连线为此离子的三重轴,任意两个相离最远的Mo原子的连线为此离子的四重轴(n重轴表示某物质绕此轴旋转360°/n的角度,不能察觉其是否旋转过).
①写出配合物A的化学式___.
②在图2中画出A溶液中阳离子的结构:
③把一种常见含氯的二元化合物的晶胞去掉所有的氯原子,发现剩余部分与A中阳离子的结构竟十分相似.这种常见二元化合物是___.
▼优质解答
答案和解析
(1)球棍模型结构中红球代表磷原子,黄球代表氧原子,P4O6分子中每个磷原子形成4个σ键,无孤电子对,所以磷原子的杂化方式为sp3,P=O双键中有一σ键,P4O10分子中每个磷原子形成4个σ键,无孤电子对,所以磷原子的杂化方式为sp3,
故答案为:sp3; sp3;
(2)H3PO3其中磷元素与相邻原子形成四个σ键,以sp3杂化,含有两个-OH,所以磷和氧形成一个单键,一个双键,所以H3PO3的结构式是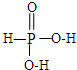 ,亚磷酸是二元酸,亚磷酸的电离为:H3PO3⇌H++H2PO3-,H2PO3-⇌H++HPO32-,亚磷酸与足量NaOH溶液反应,生成Na2HPO3,该反应方程式为:NaOH+H3PO2=Na H2PO2+H2O,H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强,
,亚磷酸是二元酸,亚磷酸的电离为:H3PO3⇌H++H2PO3-,H2PO3-⇌H++HPO32-,亚磷酸与足量NaOH溶液反应,生成Na2HPO3,该反应方程式为:NaOH+H3PO2=Na H2PO2+H2O,H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强,
故答案为: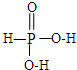 ; NaOH+H3PO2=Na H2PO2+H2O;H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强;
; NaOH+H3PO2=Na H2PO2+H2O;H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强;
(3)三溴化硼分子中硼原子的价层电子对数为
=3,B原子按sp2方式杂化,没有孤电子对,所以分子空间构型为平面三角形,结构式为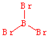 ,三溴化磷分子中磷原子的价层电子对数为
,三溴化磷分子中磷原子的价层电子对数为
=4,P原子按sp3方式杂化,有一对孤电子对,所以分子空间构型为三角锥形,结构式为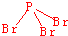 ,
,
故答案为:平面三角形;三角锥;
(4)①配合物中內界原子不能发生电离,外界离子在水溶液里能发生电离,金属钼(Mo)与氯形成的配合物A,在水溶液中完全电离,生成一种简单阴离子和一种阳离子,个数比为4:1,则配离子和外界离子之比为1:4,阳离子结构呈立方体,十分对称,任意两个相离最远的氯原子的连线为此离子的三重轴,任意两个相离最远的Mo原子的连线为此离子的四重轴,含有8个Cl,六个面含有Mo,所以配合物A的化学式为:[Mo6Cl8]Cl4,
故答案为:[Mo6Cl8]Cl4;
②A溶液中阳离子为:[Mo6Cl8]4+,含有8个Cl,在立方体的8个顶点,含有6个Mo,在六个面的中心,所以阳离子的结构为: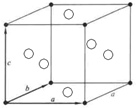 ,
,
故答案为: ;
;
③氯化钠晶胞结构为: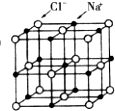 ,沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,钠离子的配位数是6,去掉所有的氯原子,剩余部分与A中阳离子的结构相似,
,沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,钠离子的配位数是6,去掉所有的氯原子,剩余部分与A中阳离子的结构相似,
故答案为:NaCl.
故答案为:sp3; sp3;
(2)H3PO3其中磷元素与相邻原子形成四个σ键,以sp3杂化,含有两个-OH,所以磷和氧形成一个单键,一个双键,所以H3PO3的结构式是
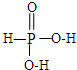 ,亚磷酸是二元酸,亚磷酸的电离为:H3PO3⇌H++H2PO3-,H2PO3-⇌H++HPO32-,亚磷酸与足量NaOH溶液反应,生成Na2HPO3,该反应方程式为:NaOH+H3PO2=Na H2PO2+H2O,H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强,
,亚磷酸是二元酸,亚磷酸的电离为:H3PO3⇌H++H2PO3-,H2PO3-⇌H++HPO32-,亚磷酸与足量NaOH溶液反应,生成Na2HPO3,该反应方程式为:NaOH+H3PO2=Na H2PO2+H2O,H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强,故答案为:
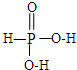 ; NaOH+H3PO2=Na H2PO2+H2O;H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强;
; NaOH+H3PO2=Na H2PO2+H2O;H3PO2、H3PO3、H3PO4中磷元素的化合价依次为+1,+3和+5价,中心磷原子的正电荷依次升高,导致P-O-H中O的电子更易向P偏移,因而H3PO2、H3PO3、H3PO4越易电离出氢离子,酸性越来越强;(3)三溴化硼分子中硼原子的价层电子对数为
| 3+3 |
| 2 |
 ,三溴化磷分子中磷原子的价层电子对数为
,三溴化磷分子中磷原子的价层电子对数为| 5+3 |
| 2 |
 ,
,故答案为:平面三角形;三角锥;
(4)①配合物中內界原子不能发生电离,外界离子在水溶液里能发生电离,金属钼(Mo)与氯形成的配合物A,在水溶液中完全电离,生成一种简单阴离子和一种阳离子,个数比为4:1,则配离子和外界离子之比为1:4,阳离子结构呈立方体,十分对称,任意两个相离最远的氯原子的连线为此离子的三重轴,任意两个相离最远的Mo原子的连线为此离子的四重轴,含有8个Cl,六个面含有Mo,所以配合物A的化学式为:[Mo6Cl8]Cl4,
故答案为:[Mo6Cl8]Cl4;
②A溶液中阳离子为:[Mo6Cl8]4+,含有8个Cl,在立方体的8个顶点,含有6个Mo,在六个面的中心,所以阳离子的结构为:
 ,
,故答案为:
 ;
;③氯化钠晶胞结构为:
 ,沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,钠离子的配位数是6,去掉所有的氯原子,剩余部分与A中阳离子的结构相似,
,沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,钠离子的配位数是6,去掉所有的氯原子,剩余部分与A中阳离子的结构相似,故答案为:NaCl.
看了 试依次回答下列相关问题:(1...的网友还看了以下:
石灰石中的盐酸不溶物是什么?在进行石灰石含钙量测定中,经过盐酸滴定反映后所遗留的杂质是什么?其遗留 2020-04-09 …
英语翻译1.又其煊赫有名者,大都尽于二书所录,良可信也.至明隆、万间而流传渐少,长兴臧懋循之刻《元 2020-06-09 …
小麦与偃麦草的杂交属于远缘杂交.远缘杂交的难题主要有三个:杂交不亲和、杂种不育和后代性状分离.(1 2020-06-30 …
电解冶炼铝的原料为铝土矿,其主要成份为氧化铝,杂质主要是氧化铁,某工厂冶炼铝及其副产品的利用如图1 2020-07-01 …
除去下列物质中的少量杂质,所用试剂及操作方法如下所示,其中正确的是()选项物质杂质所用试剂及操作方 2020-07-12 …
试依次回答下列相关问题:(1)磷有两种氧化物P4O6和P4O10,其球棍模型结构如图1所示,其中磷 2020-07-29 …
科学家用植物细胞杂交方法,将番茄的原生质体和马铃薯的原生质体融合,成功地培育出了“番茄-马铃薯”杂种 2020-10-29 …
科学家用植物细胞杂交方法,将番茄的原生质体和马铃薯的原生质体融合,成功地培育出了“番茄-马铃薯”杂种 2020-10-29 …
阅读下面的文字,完成1-3题元杂剧作者的特殊性,时常为论者所忽略。书会才人加工整理或者创作的杂剧,其 2020-11-26 …
普通金鱼(tt)和透明金鱼(TT)杂交,其后代为五花鱼(Tt).现五花鱼之间进行杂交,问其后代表现型 2021-01-01 …