早教吧作业答案频道 -->化学-->
1,2-二溴乙烷是常用的有机合成中间体,某小组用如下装置合成1,2-二溴乙烷.装置B中发生的反应为C2H5OH浓H2SO4170℃CH2=CH2↑+H2O产物和部分反应物
题目详情
1,2-二溴乙烷是常用的有机合成中间体,某小组用如下装置合成1,2-二溴乙烷.
装置B中发生的反应为C2H5OH
CH2=CH2↑+H2O
产物和部分反应物的相关数据如下:
合成反应:
在冰水浴冷却下将20.0mL浓硫酸与10.0mL95%乙醇混合均匀地到反应液,取出10.0mL加入三颈烧瓶B中,剩余部分装入滴液漏斗A中.E的试管中加入8.0g液溴,再加入2-3mL水,使管外用水冷却.断开D、E之间的导管,加热B,待装置内空气被排除后,连接D和E,继续加热并保持温度在170-180℃,打开滴液漏斗活塞,缓慢滴加反应液,直至反应完毕.
分离提纯:
将粗产物分别用10%的氢氧化钠溶液和水洗涤,分离后加入无水氯化钙干燥,待溶液澄清后进行蒸馏,得到纯净的1,2-二溴乙烷6.3g.
回答下列问题:
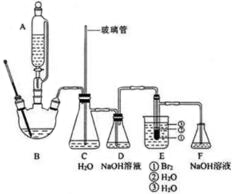
(1)混合浓硫酸与乙醇时,加入试剂的正确顺序是___;使用冰水浴降温的目的是___.
(2)为防止暴沸,装置B中还应加入___;C的作用是___;E中试管里加水的目的是___.
(3)判断生成1,2-二溴乙烷反应结束的方法是___;反应结束时正确的操作是___.
(4)洗涤和分离粗产物时使用的玻璃仪器是___.
(5)本实验中,1,2-二溴乙烷的产率为___.
(6)下列操作中,将导致产物产率降低的是___(填正确答案的标号).
a.乙烯通入溴时迅速鼓泡 b.实验室没有装置D
c.去掉装置E烧杯中的水 d.装置F中NaOH溶液用水代替.
装置B中发生的反应为C2H5OH
| 浓H2SO4 |
| |
| 170℃ |
产物和部分反应物的相关数据如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1,2-二溴乙烷 | 131.4 | 2.18 | 微溶 |
| 溴 | 58.8 | 3.12 | 微溶 |
| 乙醇 | 78.5 | 0.79 | 溶 |
在冰水浴冷却下将20.0mL浓硫酸与10.0mL95%乙醇混合均匀地到反应液,取出10.0mL加入三颈烧瓶B中,剩余部分装入滴液漏斗A中.E的试管中加入8.0g液溴,再加入2-3mL水,使管外用水冷却.断开D、E之间的导管,加热B,待装置内空气被排除后,连接D和E,继续加热并保持温度在170-180℃,打开滴液漏斗活塞,缓慢滴加反应液,直至反应完毕.
分离提纯:
将粗产物分别用10%的氢氧化钠溶液和水洗涤,分离后加入无水氯化钙干燥,待溶液澄清后进行蒸馏,得到纯净的1,2-二溴乙烷6.3g.
回答下列问题:

(1)混合浓硫酸与乙醇时,加入试剂的正确顺序是___;使用冰水浴降温的目的是___.
(2)为防止暴沸,装置B中还应加入___;C的作用是___;E中试管里加水的目的是___.
(3)判断生成1,2-二溴乙烷反应结束的方法是___;反应结束时正确的操作是___.
(4)洗涤和分离粗产物时使用的玻璃仪器是___.
(5)本实验中,1,2-二溴乙烷的产率为___.
(6)下列操作中,将导致产物产率降低的是___(填正确答案的标号).
a.乙烯通入溴时迅速鼓泡 b.实验室没有装置D
c.去掉装置E烧杯中的水 d.装置F中NaOH溶液用水代替.
▼优质解答
答案和解析
(1)浓硫酸密度较大,混合过程会放出大量热,所以正确操作方法为:先向试管中加入乙醇,然后边振荡边慢慢加入浓硫酸,乙醇沸点低,温度高易挥发,使用冰水浴降温可防止乙醇挥发,
故答案为:先加乙醇,再加浓硫酸;防止乙醇挥发;
(2)乙醇沸点低,加热易沸腾,装置B中还应加入碎瓷片引入汽化中心,防止暴沸,B装置产生乙烯气体,装置C有竖直的玻璃管为安全管,与空气相通,当C压力过大时,安全管中液面上升,使C瓶中压力稳定,并能发现装置是否堵塞,能平衡气压,液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,所以E中试管里加水的目的是防止溴、产物1,2-二溴乙烷挥发,
故答案为:碎瓷片;平衡气压;防止溴、产物1,2-二溴乙烷挥发;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以判断生成1,2-二溴乙烷反应结束的方法是E中试管里的液体变为无色,为防止倒吸,反应结束时正确的操作是断开DE之间的导管,再停止加热,
故答案为:E中试管里的液体变为无色;断开DE之间的导管,再停止加热;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层,所以需要的玻璃仪器为:分液漏斗、烧杯,
故答案为:分液漏斗、烧杯;
(5)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,8.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为9.4g,所以产率=
×100%=
×100%≈67%,
故答案为:67%;
(6)a.乙烯通入溴时迅速鼓泡,部分乙烯未被吸收,产量偏低,故选;
b.装置D:用氢氧化钠溶液除去SO2、CO2,实验室没有装置D,二氧化硫能与溴水反应生成硫酸和氢溴酸,产量偏低,故选;
c.液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,若去掉装置E烧杯中的水,产量偏低,故选;
d.装置F尾气吸收,其中的NaOH溶液用水代替,无影响,故不选.
故答案为:abc.
故答案为:先加乙醇,再加浓硫酸;防止乙醇挥发;
(2)乙醇沸点低,加热易沸腾,装置B中还应加入碎瓷片引入汽化中心,防止暴沸,B装置产生乙烯气体,装置C有竖直的玻璃管为安全管,与空气相通,当C压力过大时,安全管中液面上升,使C瓶中压力稳定,并能发现装置是否堵塞,能平衡气压,液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,所以E中试管里加水的目的是防止溴、产物1,2-二溴乙烷挥发,
故答案为:碎瓷片;平衡气压;防止溴、产物1,2-二溴乙烷挥发;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以判断生成1,2-二溴乙烷反应结束的方法是E中试管里的液体变为无色,为防止倒吸,反应结束时正确的操作是断开DE之间的导管,再停止加热,
故答案为:E中试管里的液体变为无色;断开DE之间的导管,再停止加热;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层,所以需要的玻璃仪器为:分液漏斗、烧杯,
故答案为:分液漏斗、烧杯;
(5)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,8.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为9.4g,所以产率=
| 实际产量 |
| 理论产量 |
| 6.3g |
| 9.4g |
故答案为:67%;
(6)a.乙烯通入溴时迅速鼓泡,部分乙烯未被吸收,产量偏低,故选;
b.装置D:用氢氧化钠溶液除去SO2、CO2,实验室没有装置D,二氧化硫能与溴水反应生成硫酸和氢溴酸,产量偏低,故选;
c.液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,若去掉装置E烧杯中的水,产量偏低,故选;
d.装置F尾气吸收,其中的NaOH溶液用水代替,无影响,故不选.
故答案为:abc.
看了 1,2-二溴乙烷是常用的有机...的网友还看了以下:
甲乙两人同时向敌机射击,已知甲击中敌机的概率为0.7,乙击中敌机的概率是0.5,则敌机被击中的概率 2020-06-16 …
甲、乙、丙三人同时向一架飞机设计,设他们击中飞机的概率均为0.4,如果只有一人击中飞机,其坠落的概 2020-06-16 …
在某次空战中,甲机先向乙机开火,击落乙机的概率时0.2;若乙机未被击落,就进行还击,击落甲机的概率 2020-07-08 …
usetheupanddownarrowkeystomovethehighlighttoyourc 2020-07-26 …
甲乙丙三人进行飞机射击训练,三人射中飞机的概率分别为0.4、0.5、0.7,飞机被射中一次坠毁的概率 2020-10-30 …
某次战役中,狙击手A受命射击敌机,若要击落敌机,需命中机首2次或命中机中3次或命中机尾1次,已知A每 2020-10-30 …
计算机中心有三台打字机A、B、C,程序交与各台打字机的概率依次是0.6,0.3,0.1,打字机发生故 2020-11-07 …
一台机床有1/3的时间加工零件A,其余时间加工零件B,加工零件A时,停机概率是0.3,加工零件B时, 2020-11-24 …
甲乙2人同时对飞机进行射击,甲的命中率为0.8,乙的命中率为0.7.若飞机被击中一次坠落的概率为0. 2020-12-13 …
在某次空战中,甲机先向乙机开火,击落乙机的概率时0.2;若乙机未被击落,就进行还击,击落甲机的概率时 2020-12-26 …