在20L恒容密闭容器中,按物质的量之比为1:2充入CO和H2发生:CO(g)+2H2(g)⇌CH3OH(g)△H=akJ/mol.测得CO的转化率随温度及不同压强的变化如图所示:n(H2)在P2及195℃时随时间变化如表所
在20L恒容密闭容器中,按物质的量之比为1:2充入CO和H2发生:CO(g)+2H2(g)⇌CH3OH(g)△H=akJ/mol.测得CO的转化率随温度及不同压强的变化如图所示:n(H2)在P2及195℃时随时间变化如表所示
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
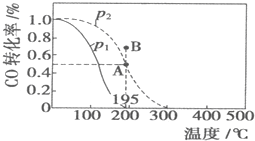
A. P1>P2,a<0
B. 在P2及195℃时,反应前3min的平均速率v(CH3OH)=0.08mol/(L•min)
C. 在P2及195℃时,该反应的平衡常数为25(mol/L)-2
D. 在B点时,v正>v逆
B.0~3 min,n(H2)=8-4=4mol,故n(CH3OH)=4÷2=2mol,v(CH3OH)=
| ||
| 3 |
C.由表中信息可知,起始时:c(H2)=
| 8mol |
| 20L |
| 1 |
| 2 |
| 4mol |
| 20L |
CO(g)+2H2(g)⇌CH3OH(g)
起始浓度(mol/L) 0.2 0.4 0
转化浓度(mol/L) 0.1 0.2 0.1
平衡浓度(mol/L) 0.1 0.2 0.1
K=
| c(CH 3OH) |
| c(CO)•c2(H 2) |
| 0.1 |
| 0.2×0.2×0.1 |
D.根据表中数据知,平衡时氢气转化率为50%,当可逆反应中初始反应物物质的量之比等于其计量数之比时,其反应物转化率相等,所以该温度和压强下CO的转化率为50%,根据图知,A点是平衡状态,B点转化率大于A点,该反应在该温度和压强下达到平衡状态,应该向逆反应方向移动,所以B点v(正)<v(逆),故D错误,
故选C.
把mgA物质溶于(100-m)g水中,配成100g溶质质量分数为n%的溶液(A可能是Na2O、SO 2020-04-09 …
已知f'(x)是f(x)的导函数,f(x)=1n(x+1)+m-2f'(1).f(x)=1n(x+ 2020-05-13 …
mA(s)+nB(g)=pC(g)+qD(g) 1.m+n=p+q 那么混合气体的平均相对分子质量 2020-05-13 …
如图所示,一个质量为M的人站在台秤上,用跨过定滑轮的绳子,将质量为m的物体自高处放下,当物体以a加 2020-05-17 …
操场上的体育运动联合器上吊着一质量为m的爬竿,一位质量为M的同学正沿着爬竿滑下,该同学受到的摩擦力 2020-06-20 …
(2014•四川)在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)⇌M(g 2020-06-23 …
问函数f(x)=a0+a1x+a2x^2+a3x^3+•••+anx^n(n∈N*),且y=f(x 2020-07-09 …
水的分子量是18,水的密度ρ=1.0×103kg/m3,阿伏加德罗常数NA=6.02×1023mo 2020-07-16 …
下列热化学方程式中,△H能正确表示物质的燃烧热的是A.CO(g)+1/2O2(g)==CO2(g) 2020-07-19 …
2道简单的机械能题!1.起重机吊钩下挂着质量为m的木箱,如果木箱以加速度a匀减速下降了高度h,则木箱 2020-11-22 …