早教吧作业答案频道 -->化学-->
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1molN2和3molH2使反应N2(g)+3H2(g)⇌2NH3(g)达到平衡,测得反应放出热量为Q1kJ.填写下列空白:(1
题目详情
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)⇌2NH3(g)达到平衡,测得反应放出热量为Q1kJ.
填写下列空白:
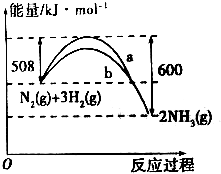
(1)Q1___92.
(2)b曲线是___时的能量变化曲线.
(3)上述条件下达平衡时H2的转化率为___.
(4)在温度体积一定的条件下,若通入2mol N2和6mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为___.
填写下列空白:

(1)Q1___92.
(2)b曲线是___时的能量变化曲线.
(3)上述条件下达平衡时H2的转化率为___.
(4)在温度体积一定的条件下,若通入2mol N2和6mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为___.
▼优质解答
答案和解析
(1)由图可知反应的热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=508-600=-92kJ•mol-1,N2与H2反应生成NH3的反应为可逆反应,反应为不能完全转化为生成物,即1mol N2和3mol H2不能完全反应生成1molNH3,则反应放出的热量值Q1<92;
故答案为:<;
(2)加催化剂降低反应的活化能,所以图中b曲线代表加入了催化剂;
故答案为:加催化剂;
(3)设转化的氢气为xmol,
N2(g)+3H2(g)=2NH3(g)△H=-92kJ•mol-1
3mol 92kJ
xmol Q1kJ
则x=
mol
所以 达平衡时H2的转化率为
=
;
故答案为:
;
(4)向密闭容器中通入1mol N2和3mol H2,不可能完全转化,所以达到平衡时放出热量Q1kJ;另一容积相同的密闭容器中通入2mol N2和6mol H2,达到平衡时原平衡相同,则放出热量应该是2QkJ,通入2mol N2和6mol H2的压强比通入1mol N2和3mol H2的大了,平衡还会向正向移动,放出的热量还会增大,即Q2>2Q1,
故答案为:Q2>2Q1.
故答案为:<;
(2)加催化剂降低反应的活化能,所以图中b曲线代表加入了催化剂;
故答案为:加催化剂;
(3)设转化的氢气为xmol,
N2(g)+3H2(g)=2NH3(g)△H=-92kJ•mol-1
3mol 92kJ
xmol Q1kJ
则x=
| 3Q1 |
| 92 |
所以 达平衡时H2的转化率为
| ||
| 3mol |
| Q1 |
| 92 |
故答案为:
| Q1 |
| 92 |
(4)向密闭容器中通入1mol N2和3mol H2,不可能完全转化,所以达到平衡时放出热量Q1kJ;另一容积相同的密闭容器中通入2mol N2和6mol H2,达到平衡时原平衡相同,则放出热量应该是2QkJ,通入2mol N2和6mol H2的压强比通入1mol N2和3mol H2的大了,平衡还会向正向移动,放出的热量还会增大,即Q2>2Q1,
故答案为:Q2>2Q1.
看了 N2与H2反应生成NH3的过...的网友还看了以下:
如图,直线a,b相交,∠1=40°1.若∠2是∠1的3倍,求∠3的度数2.若∠2-∠1=40°,求 2020-05-13 …
一个图形按1:2放大和按2:1缩小有什么不一样不好意思,打错了,应该是:一个图形按1:2放大和按2 2020-05-14 …
已知a-1/a=3,求a-1/a和a^2-1/a^2初一数学错了,是已知a+1/a=3,求a-1/ 2020-05-15 …
f(x)=x^2+|x-a|+1,x属于R,常数a为R,求f(x)最小值x=a再分别讨论a的取值情 2020-05-23 …
一道证明题,方差的公式和简化公式的证明过程方差公式和其简化公式相等的证明过程那个x上有“-”证明S 2020-06-10 …
规定a○b=1/ab+1/(a+1)(b+x),若2○1=2/3,则2004○2005等于多少?用 2020-06-12 …
设非负等差数列{a1}的公差d≠0,记Sn为数列{a1}的前n项和若a503≤1/1005,则{1 2020-07-30 …
1.一个数的一半,加上10除100的商,和是2.1,求这个数.2.两个加数的和是959,其中第一个 2020-07-31 …
若2/1+i=1+ai,其中a属于R,i是虚数单位,则2+ai若2/1+i=1+ai,其中a属于R, 2020-11-06 …
若2!=1×2,=1×2×3,=1×2×3×4×5×6求4!/5!昨天入学试考的题,我感觉题目错了, 2020-11-14 …