早教吧作业答案频道 -->化学-->
碱式氯化铜是重要的无机杀菌剂.(1)碱式氯化铜有多种制备方法①方法1:45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2(OH)2Cl2•3H2O,该反应的化学方程式为.②方法2:先制得CuCl2
题目详情
碱式氯化铜是重要的无机杀菌剂.
(1)碱式氯化铜有多种制备方法
①方法1:45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2•3H2O,该反应的化学方程式为___.
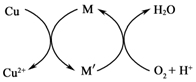
②方法2:先制得CuCl2,再与石灰乳反应生成碱式氯化铜.Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示. M′的化学式为___.
(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc•xH2O. 为测定某碱式氯化铜的组成,进行下列实验:
①称取样品1.1160g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得AgCl 0.1722g;
③另取25.00mL溶液A,调节pH 4~5,用浓度为0.08000mol•L-1的EDTA(Na2H2Y•2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++H2Y2-═CuY2-+2H+),滴定至终点,消耗标准溶液30.00mL.通过计算确定该样品的化学式(写出计算过程).
2222
223+

abc2
3
3
-12222+2+22-2-+
(1)碱式氯化铜有多种制备方法
①方法1:45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2•3H2O,该反应的化学方程式为___.
②方法2:先制得CuCl2,再与石灰乳反应生成碱式氯化铜.Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示. M′的化学式为___.

(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc•xH2O. 为测定某碱式氯化铜的组成,进行下列实验:
①称取样品1.1160g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得AgCl 0.1722g;
③另取25.00mL溶液A,调节pH 4~5,用浓度为0.08000mol•L-1的EDTA(Na2H2Y•2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++H2Y2-═CuY2-+2H+),滴定至终点,消耗标准溶液30.00mL.通过计算确定该样品的化学式(写出计算过程).
2222
223+

abc2
3
3
-12222+2+22-2-+
▼优质解答
答案和解析
(1)①45~50℃时,向CuCl悬浊液中持续通入空气得到Cu22 (OH)22 Cl22•3H22O,反应物为CuCl、氧气、水,Cu元素的化合价升高,O元素的化合价降低,由原子、电子守恒可知反应为4CuCl+O22+8H22O
2Cu2(OH)2Cl2•3H2O,
故答案为:4CuCl+O2+8H2O
2Cu2(OH)2Cl2•3H2O;
②Fe3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+,
故答案为:Fe2+;
(2)n(Cl-)=n(AgCl)×
=
×
=4.800×10-3mol,
n(Cu2+)=n(EDTA)×
=0.08000 mol•L-1×30.00 mL×10-3 L•mL-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
45-50℃ 45-50℃ 45-50℃ 45-50℃ 2Cu22(OH)22Cl22•3H22O,
故答案为:4CuCl+O22+8H22O
2Cu2(OH)2Cl2•3H2O;
②Fe3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+,
故答案为:Fe2+;
(2)n(Cl-)=n(AgCl)×
=
×
=4.800×10-3mol,
n(Cu2+)=n(EDTA)×
=0.08000 mol•L-1×30.00 mL×10-3 L•mL-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
45-50℃ 45-50℃ 45-50℃ 45-50℃ 2Cu22(OH)22Cl22•3H22O;
②Fe3+3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+2+,
故答案为:Fe2+2+;
(2)n(Cl--)=n(AgCl)×
=
×
=4.800×10-3mol,
n(Cu2+)=n(EDTA)×
=0.08000 mol•L-1×30.00 mL×10-3 L•mL-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
100.00mL 25.00mL 100.00mL 100.00mL 100.00mL25.00mL 25.00mL 25.00mL=
×
=4.800×10-3mol,
n(Cu2+)=n(EDTA)×
=0.08000 mol•L-1×30.00 mL×10-3 L•mL-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
0.1722g 143.5g/mol 0.1722g 0.1722g 0.1722g143.5g/mol 143.5g/mol 143.5g/mol×
100.00mL 25.00mL 100.00mL 100.00mL 100.00mL25.00mL 25.00mL 25.00mL=4.800×10-3-3mol,
n(Cu2+2+)=n(EDTA)×
=0.08000 mol•L-1×30.00 mL×10-3 L•mL-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
100.00mL 25.00mL 100.00mL 100.00mL 100.00mL25.00mL 25.00mL 25.00mL=0.08000 mol•L-1-1×30.00 mL×10-3-3 L•mL-1-1×
=9.600×10-3 mol,
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
100.00mL 25.00mL 100.00mL 100.00mL 100.00mL25.00mL 25.00mL 25.00mL=9.600×10-3-3 mol,
n(OH--)=2n(Cu2+2+)-n(Cl--)=2×9.600×10-3-3 mol-4.800×10-3-3 mol=1.440×10-2-2 mol,
m(Cl--)=4.800×10-3-3 mol×35.5 g•mol-1-1=0.1704 g,
m(Cu2+2+)=9.600×10-3-3 mol×64 g•mol-1-1=0.6144 g,
m(OH--)=1.440×10-2-2 mol×17 g•mol-1-1=0.2448 g,
n(H22O)=
=4.800×10-3 mol,
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
1.1160g-0.1704g-0.6144g-0.2448g 18g/mol 1.1160g-0.1704g-0.6144g-0.2448g 1.1160g-0.1704g-0.6144g-0.2448g 1.1160g-0.1704g-0.6144g-0.2448g18g/mol 18g/mol 18g/mol=4.800×10-3-3 mol,
则a:b:c:x=n(Cu2+2+):n(OH--):n(Cl--):n(H22O)=2:3:1:1,
即化学式为Cu22 (OH)33Cl•H22O,
答:该样品的化学式为Cu22 (OH)33Cl•H22O.
| ||
故答案为:4CuCl+O2+8H2O
| ||
②Fe3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+,
故答案为:Fe2+;
(2)n(Cl-)=n(AgCl)×
| 100.00mL |
| 25.00mL |
| 0.1722g |
| 143.5g/mol |
| 100.00mL |
| 25.00mL |
n(Cu2+)=n(EDTA)×
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| ||
| 45-50℃ |
. |
| 45-50℃ |
. |
| 45-50℃ |
. |
| 45-50℃ |
. |
.
.
.
.
.故答案为:4CuCl+O22+8H22O
| ||
②Fe3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+,
故答案为:Fe2+;
(2)n(Cl-)=n(AgCl)×
| 100.00mL |
| 25.00mL |
| 0.1722g |
| 143.5g/mol |
| 100.00mL |
| 25.00mL |
n(Cu2+)=n(EDTA)×
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| ||
| 45-50℃ |
. |
| 45-50℃ |
. |
| 45-50℃ |
. |
| 45-50℃ |
. |
.
.
.
.
.②Fe3+3+对该反应有催化作用,结合图可知,Cu元素的化合价升高,则M中Fe元素的化合价降低,可知M′的化学式为Fe2+2+,
故答案为:Fe2+2+;
(2)n(Cl--)=n(AgCl)×
| 100.00mL |
| 25.00mL |
| 0.1722g |
| 143.5g/mol |
| 100.00mL |
| 25.00mL |
n(Cu2+)=n(EDTA)×
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| 100.00mL |
| 25.00mL |
| 0.1722g |
| 143.5g/mol |
| 100.00mL |
| 25.00mL |
n(Cu2+)=n(EDTA)×
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| 0.1722g |
| 143.5g/mol |
| 100.00mL |
| 25.00mL |
n(Cu2+2+)=n(EDTA)×
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| 100.00mL |
| 25.00mL |
| 100.00mL |
| 25.00mL |
n(OH-)=2n(Cu2+)-n(Cl-)=2×9.600×10-3 mol-4.800×10-3 mol=1.440×10-2 mol,
m(Cl-)=4.800×10-3 mol×35.5 g•mol-1=0.1704 g,
m(Cu2+)=9.600×10-3 mol×64 g•mol-1=0.6144 g,
m(OH-)=1.440×10-2 mol×17 g•mol-1=0.2448 g,
n(H2O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| 100.00mL |
| 25.00mL |
n(OH--)=2n(Cu2+2+)-n(Cl--)=2×9.600×10-3-3 mol-4.800×10-3-3 mol=1.440×10-2-2 mol,
m(Cl--)=4.800×10-3-3 mol×35.5 g•mol-1-1=0.1704 g,
m(Cu2+2+)=9.600×10-3-3 mol×64 g•mol-1-1=0.6144 g,
m(OH--)=1.440×10-2-2 mol×17 g•mol-1-1=0.2448 g,
n(H22O)=
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+):n(OH-):n(Cl-):n(H2O)=2:3:1:1,
即化学式为Cu2 (OH)3Cl•H2O,
答:该样品的化学式为Cu2 (OH)3Cl•H2O.
| 1.1160g-0.1704g-0.6144g-0.2448g |
| 18g/mol |
则a:b:c:x=n(Cu2+2+):n(OH--):n(Cl--):n(H22O)=2:3:1:1,
即化学式为Cu22 (OH)33Cl•H22O,
答:该样品的化学式为Cu22 (OH)33Cl•H22O.
看了 碱式氯化铜是重要的无机杀菌剂...的网友还看了以下:
将圆心角为120°,面积为3π的扇形.作为圆锥的侧面,求圆锥的表面积和体积解:设圆锥母线为L,则: 2020-04-12 …
2^2-1^2=2*1+13^2-2^2=2*2+14^2-3^2=2*3+1……(n+1)^2- 2020-05-19 …
已知三角形的三个顶点分别为A(6,-7),B(-2,3),C(2,1),求AC边上的中线所在的直线 2020-06-03 …
某反应A+2B==C,经2min后,C的浓度由0.05mol/L增大到2.55mol/l,则用B的 2020-06-12 …
(2Rcosa-L/2)/sina=(L/2乘sina)/sin(90-2a)求详解我还是个初中生 2020-07-25 …
根式计算化简1、(1/x^2-3x+2)+(1/x^2-x)+(1/x^2+x)+(1/x^2+3 2020-07-30 …
定积分计算∫l/(d^2/4+l^2)^(3/2)*dl在[0,l]上的积分能计算吗?d是常数∫L 2020-08-02 …
5x^2+16x+12=12x^2-29x+15=12x^2-25xy+12y^2=20a^2+42 2020-10-31 …
求一道预备班数学期中考试的答案小明在做题时发现了一个规律:1*2/1=1-2/1,2*3/1=2/1 2020-11-05 …
原子结构原子中每个电子的运动状态由四个量子数n,l,m,ms确定.假设它的取值规则为:n=1,2,3 2020-12-02 …