早教吧作业答案频道 -->化学-->
硫酸亚铁铵晶体化学式为xFeSO4•y(NH4)2SO4•zH2O,在制药、电镀方面有广泛的应用.资料:①硫酸亚铁铵晶体易溶于水,不溶于乙醇;②硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去
题目详情
硫酸亚铁铵晶体化学式为xFeSO4•y(NH4)2SO4•zH2O,在制药、电镀方面有广泛的应用.
资料:①硫酸亚铁铵晶体易溶于水,不溶于乙醇;②硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去.
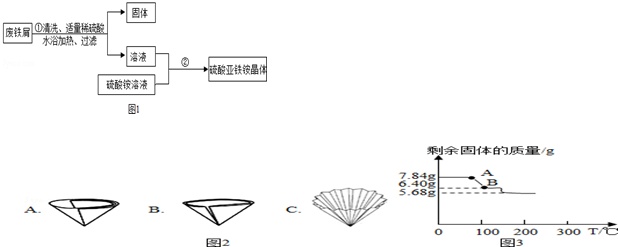
【探究一】:制备硫酸亚铁铵晶体:学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图1:
(1)在盛有废铁屑的容器中,倒入热水和洗涤剂,充分搅拌.以除去废铁屑表面的油污,这是利用洗涤剂的___作用;操作①中发生反应的化学方程式为___;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、___.过滤操作中滤纸有多种折法,为了加快过滤速率,你选择折法是___;(3)操作①中过滤时,要趁热进行说明:温度高,FeSO4溶解度___(大或小),过滤后得到的固体中一定含有的物质是___;
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是:b→___→___→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是___;
A、避免用水洗涤所造成的晶体损耗 B、酒精易挥发,可低温晾干晶体
【探究二】:探究硫酸亚铁铵的组成
【实验步骤】:取2份等质量的硫酸亚铁铵晶体,分别进行实验:向一份中加入过量的NaOH溶液,充分反应后得到0.68g NH3;向另一份中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀.回答下列问题:
(6)实验中生成的NH3能使湿润的___变蓝;写出(NH4)2SO4与NaOH反应的化学方程式:___;
(7)取最后一次洗涤液,加入Na2SO4溶液,___,则说明沉淀已经洗涤干净;根据实验数据,则x 和y的比值___(相对分子质量:NH3-17、BaSO4-233);为进一步确定硫酸亚铁铵晶体的组成,另取7.84g硫酸亚铁铵晶体,并加热使其分解,剩余固体质量与温度的关系如图3所示,则:根据图示数据,硫酸亚铁铵晶体中,x:y:z=___;
(8)写出A点到B点发生反应的化学方程式___.
资料:①硫酸亚铁铵晶体易溶于水,不溶于乙醇;②硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去.

【探究一】:制备硫酸亚铁铵晶体:学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图1:
(1)在盛有废铁屑的容器中,倒入热水和洗涤剂,充分搅拌.以除去废铁屑表面的油污,这是利用洗涤剂的___作用;操作①中发生反应的化学方程式为___;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、___.过滤操作中滤纸有多种折法,为了加快过滤速率,你选择折法是___;(3)操作①中过滤时,要趁热进行说明:温度高,FeSO4溶解度___(大或小),过滤后得到的固体中一定含有的物质是___;
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是:b→___→___→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是___;
A、避免用水洗涤所造成的晶体损耗 B、酒精易挥发,可低温晾干晶体
【探究二】:探究硫酸亚铁铵的组成
【实验步骤】:取2份等质量的硫酸亚铁铵晶体,分别进行实验:向一份中加入过量的NaOH溶液,充分反应后得到0.68g NH3;向另一份中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀.回答下列问题:
(6)实验中生成的NH3能使湿润的___变蓝;写出(NH4)2SO4与NaOH反应的化学方程式:___;
(7)取最后一次洗涤液,加入Na2SO4溶液,___,则说明沉淀已经洗涤干净;根据实验数据,则x 和y的比值___(相对分子质量:NH3-17、BaSO4-233);为进一步确定硫酸亚铁铵晶体的组成,另取7.84g硫酸亚铁铵晶体,并加热使其分解,剩余固体质量与温度的关系如图3所示,则:根据图示数据,硫酸亚铁铵晶体中,x:y:z=___;
(8)写出A点到B点发生反应的化学方程式___.
▼优质解答
答案和解析
(1)倒入热水和洗涤剂,充分搅拌,以除去废铁屑表面的油污,这是利用洗涤剂的乳化作用;铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗.过滤操作中滤纸有多种折法,为了加快过滤速率,你选择折法是A;
(3)加入稀硫酸后,铁可以和硫酸反应生成硫酸亚铁和氢气,但铜不会和硫酸反应,因此铜就被过滤出来,所以,过滤后得到的固体中一定含有的物质是铜;
(4)操作②的目的是得到硫酸亚铁铵晶体,由于硫酸亚铁铵的溶解度受温度的影响较大,所以基本操作步骤:加热浓缩,然后冷却结晶;再过滤;最后洗涤干燥.
(5)硫酸亚铁溶于水不溶于酒精,用A方法洗涤硫酸亚铁晶体损失较多,可用酒精洗涤,酒精又易挥发,能得到大量的纯净的硫酸亚铁晶体,故答案:AB;
(6)氨气能和水反应生成氨水,氨水呈碱性能使石蕊变蓝色;(NH4)2SO4与NaOH反应生成硫酸钠、水和氨气; 反应的方程式是(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O;
(7)加入硫酸钠若不产生白色沉淀证明沉淀上已不附着BaCl2,则说明沉淀已经洗涤干净,
设硫酸亚铁铵晶体中硫酸铵的质量为x;
(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O
132 34
x 0.68g
=
解得:x=2.64g
设和硫酸铵反应生成硫酸钡沉淀的质量为y
(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl
132 233
2.64g y
=
解得:y=4.66g y=4.66g
所以和硫酸亚铁反应产生硫酸钡沉淀的质量为9.32g-4.66g=4.66g;
设和硫酸亚铁反应生成硫酸钡沉淀的质量为z
FeSO4+BaCl2=BaSO4↓+FeCl2
152 233
z 4.66g
=
解得:z=3.04g
硫酸亚铁铵中
=
;
=
;故答案:1:1;
由A→B固体质量减轻的质量就是生成的水的质量,7.84g硫酸亚铁铵晶体中水的质量为7.84g-5.68g=2.16g,
=
;
=
故答案:1:1:6;
(8)(FeSO4•(NH4)2SO4•6H2O
FeSO4+(NH4)2SO4•2H2O+4H2O)加热FeSO4•(NH4)2SO4•6H2O分解得到硫酸亚铁、硫酸铵、和水,反应的方程式是:FeSO4•(NH4)2SO4•6H2O
FeSO4+(NH4)2SO4•2H2O+4H2O.
故答为:(1)乳化,Fe+H2SO4=FeSO4+H2↑;(2)漏斗,A;(3)大,Cu;(4)c、a;(5)AB;(6)(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O;(7)1:1,1:1:硫;(8)FeSO4•(NH4)2SO4•6H2O
FeSO4+(NH4)2SO4•2H2O+4H2O.
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗.过滤操作中滤纸有多种折法,为了加快过滤速率,你选择折法是A;
(3)加入稀硫酸后,铁可以和硫酸反应生成硫酸亚铁和氢气,但铜不会和硫酸反应,因此铜就被过滤出来,所以,过滤后得到的固体中一定含有的物质是铜;
(4)操作②的目的是得到硫酸亚铁铵晶体,由于硫酸亚铁铵的溶解度受温度的影响较大,所以基本操作步骤:加热浓缩,然后冷却结晶;再过滤;最后洗涤干燥.
(5)硫酸亚铁溶于水不溶于酒精,用A方法洗涤硫酸亚铁晶体损失较多,可用酒精洗涤,酒精又易挥发,能得到大量的纯净的硫酸亚铁晶体,故答案:AB;
(6)氨气能和水反应生成氨水,氨水呈碱性能使石蕊变蓝色;(NH4)2SO4与NaOH反应生成硫酸钠、水和氨气; 反应的方程式是(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O;
(7)加入硫酸钠若不产生白色沉淀证明沉淀上已不附着BaCl2,则说明沉淀已经洗涤干净,
设硫酸亚铁铵晶体中硫酸铵的质量为x;
(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O
132 34
x 0.68g
| 132 |
| 34 |
| x |
| 0.68g |
设和硫酸铵反应生成硫酸钡沉淀的质量为y
(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl
132 233
2.64g y
| 132 |
| 233 |
| 2.64g |
| y |
所以和硫酸亚铁反应产生硫酸钡沉淀的质量为9.32g-4.66g=4.66g;
设和硫酸亚铁反应生成硫酸钡沉淀的质量为z
FeSO4+BaCl2=BaSO4↓+FeCl2
152 233
z 4.66g
| 152 |
| 233 |
| z |
| 4.66g |
硫酸亚铁铵中
| 3.04g |
| 2.64g |
| 152x |
| 132y |
| x |
| y |
| 1 |
| 1 |
由A→B固体质量减轻的质量就是生成的水的质量,7.84g硫酸亚铁铵晶体中水的质量为7.84g-5.68g=2.16g,
| 132y |
| 18z |
| 2.64g |
| 2.16g |
| y |
| z |
| 1 |
| 6 |
(8)(FeSO4•(NH4)2SO4•6H2O
| ||
| ||
故答为:(1)乳化,Fe+H2SO4=FeSO4+H2↑;(2)漏斗,A;(3)大,Cu;(4)c、a;(5)AB;(6)(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O;(7)1:1,1:1:硫;(8)FeSO4•(NH4)2SO4•6H2O
| ||
看了硫酸亚铁铵晶体化学式为xFeS...的网友还看了以下:
列方程解应用题某地电话入网拨号有两种收费方式,用户可任选其一:1.及时制:3元/时;2.包月制:5 2020-05-13 …
ab垂直bc,ab=10cm,点m以1厘米每秒的速度从点a开始延ab向点b运动,点n同时以2厘米秒 2020-05-14 …
一个开关同时控制两盏灯泡的亮与灭,则这两盏灯泡1串联或并联都可以2并联3串联一个开关同时控制两盏灯 2020-05-14 …
有一道这样的常微分方程应用题,例3:一容器内装有10升盐水,其中含盐1千克.现以3升/分钟的速度往 2020-06-05 …
某肉食加工厂在烤制风味肠时主要依据的是下面表格中的数据:根据以上表格所提供的信息回答:(1)当烤制 2020-06-18 …
下列有关真核细胞DNA分子复制的叙述,正确的是()A.复制形成的两个子代DNA分子共4个游离的磷酸 2020-06-26 …
如何提高水产饲料调制温度我们产在生产2.0以下的水产饲料时,温度总是在74度左右.35的机子55K 2020-06-30 …
饱和亚硫酸氢钠溶液配制时出现的问题1、饱和亚硫酸氢钠溶液要临时配制,为什么?2、配方上说先配40%的 2020-11-07 …
证明当对角互补时,以2,3,4,5为边的四边形面积为最大值.要用到三角函数导数.跪谢!原题是英文,我 2020-12-01 …
一枚ICBM导弹从100km高度垂直下落初速度为3.6×104km/h.正下方一枚ABM导弹同时以2 2021-01-06 …