早教吧作业答案频道 -->化学-->
(1)1.00gCH4完全燃烧生成液态水和CO2,放出55.6kJ热量,写出表示CH4的燃烧热的热化学方程式.(2)等物质的量浓度的下列溶液:①(NH4)2SO4②NH4HCO3③NH4Cl④NH4Fe(SO4)2中,c(NH4+)由
题目详情
(1)1.00g CH4完全燃烧生成液态水和CO2,放出55.6kJ热量,写出表示CH4的燃烧热的热化学方程式___.
(2)等物质的量浓度的下列溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH4Fe(SO4)2中,c(NH4+)由大到小的顺序为___.
(3)写出符合要求的方程式
①饱和的FeCl3溶液滴入沸水中(写离子方程式)___
②NaHCO3在水溶液中存在的所有电离过程___
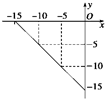
(4)某温度下的溶液中,c(H+)=10x mol•L-1,c(OH-)=10y mol•L-1.x与y的关系如图所示:
①该温度下,NaCl溶液的pH=___.
②该温度下,pH=8的Ba(OH)2溶液与pH=6的盐酸混合,并保持恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为___.(忽略溶液混合时体积变化)
(2)等物质的量浓度的下列溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH4Fe(SO4)2中,c(NH4+)由大到小的顺序为___.
(3)写出符合要求的方程式
①饱和的FeCl3溶液滴入沸水中(写离子方程式)___
②NaHCO3在水溶液中存在的所有电离过程___
(4)某温度下的溶液中,c(H+)=10x mol•L-1,c(OH-)=10y mol•L-1.x与y的关系如图所示:
①该温度下,NaCl溶液的pH=___.
②该温度下,pH=8的Ba(OH)2溶液与pH=6的盐酸混合,并保持恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为___.(忽略溶液混合时体积变化)

▼优质解答
答案和解析
(1)1g CH4完全燃烧生成液态水和CO2气体,放出55.6kJ的热量,则1mol即16g CH4完全燃烧生成液态水和CO2气体,16×55.6kJ=889.6kJ,则甲烷燃烧热的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1;
(2)物质的量浓度相同的下列溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH4Fe(SO4)2;先不考虑水解,则(NH4)2CO3 中含有两个NH4+,所以它们NH4+的浓度大于其它三种物质,②④二种物质中,④NH4Fe(SO4)2酸性最强,NH4+水解受到的抑制最大,即NH4+的量较多,溶液中c(NH4+)较大,
①NH4Cl,NH4+水解,②NH4HCO3,碳酸氢根离子的水解对铵根离子起促进作用,即溶液中c(NH4+)④>③>②;
按c(NH4+)由大到小的顺序排列为:①>④>③>②,
故答案为:①④③②;
(3)①饱和的FeCl3溶液滴入沸水中反应生成氢氧化铁胶体 的离子方程式为:Fe3++3 H2O
Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3 H2O
Fe(OH)3(胶体)+3H+;
②碳酸氢钠溶液中存在电离是碳酸氢钠完全电离,碳酸氢根离子部分电离;电离方程式为:NaHCO3=HCO3-+Na+,HCO3-⇌CO32-+H+,
故答案为:NaHCO3=HCO3-+Na+,HCO3-⇌CO32-+H+;
(4)①根据图知,当c(H+)=10-5 mol/L,c(OH-)=10-10 mol/L,由离子积常数=c(H+).c(OH-)=10-5×10-10=10-15,
中性溶液中,c(H+)=c(OH-)=
=10-7.5,pH=-lg10-7.5=7.5,
故答案为:7.5;
②设氢氧化钡容溶液的体积为xL,盐酸的体积为y,pH=8的Ba(OH)2溶液,溶液中c(OH-)=1×10-7mol/L,
pH=6的稀盐酸溶液中c(H+)=1×10-6mol/L,
欲使混合溶液pH=7<7.5,溶液此时显酸性,即混合后c(H+)=1×10-7mol/L,即
=1×10-5mol/L,解得x:y=9:2,
故答案为:9:2.
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1;
(2)物质的量浓度相同的下列溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH4Fe(SO4)2;先不考虑水解,则(NH4)2CO3 中含有两个NH4+,所以它们NH4+的浓度大于其它三种物质,②④二种物质中,④NH4Fe(SO4)2酸性最强,NH4+水解受到的抑制最大,即NH4+的量较多,溶液中c(NH4+)较大,
①NH4Cl,NH4+水解,②NH4HCO3,碳酸氢根离子的水解对铵根离子起促进作用,即溶液中c(NH4+)④>③>②;
按c(NH4+)由大到小的顺序排列为:①>④>③>②,
故答案为:①④③②;
(3)①饱和的FeCl3溶液滴入沸水中反应生成氢氧化铁胶体 的离子方程式为:Fe3++3 H2O
| ||
故答案为:Fe3++3 H2O
| ||
②碳酸氢钠溶液中存在电离是碳酸氢钠完全电离,碳酸氢根离子部分电离;电离方程式为:NaHCO3=HCO3-+Na+,HCO3-⇌CO32-+H+,
故答案为:NaHCO3=HCO3-+Na+,HCO3-⇌CO32-+H+;
(4)①根据图知,当c(H+)=10-5 mol/L,c(OH-)=10-10 mol/L,由离子积常数=c(H+).c(OH-)=10-5×10-10=10-15,
中性溶液中,c(H+)=c(OH-)=
| 10-15 |
故答案为:7.5;
②设氢氧化钡容溶液的体积为xL,盐酸的体积为y,pH=8的Ba(OH)2溶液,溶液中c(OH-)=1×10-7mol/L,
pH=6的稀盐酸溶液中c(H+)=1×10-6mol/L,
欲使混合溶液pH=7<7.5,溶液此时显酸性,即混合后c(H+)=1×10-7mol/L,即
| 10-6y-10-7x |
| x+y |
故答案为:9:2.
看了(1)1.00gCH4完全燃烧...的网友还看了以下:
(1)家用液化气的主要成分之一是丁烷(C4H10),当1kg丁烷完全燃烧生成二氧化碳和液态水时,放 2020-05-14 …
(1)家用液化气的主要成分之一是丁烷(C4H10),当1kg丁烷完全燃烧生成二氧化碳和液态水时,放 2020-05-14 …
已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkj,则乙炔燃烧的热化学方 2020-05-16 …
写出下列反应的热化学方程式:(1)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l) 2020-07-17 …
谁能解决下列英语问题翻译下列句子1.我的裙子和她的不同。2.我的裙子和她的一样。3.你能让我到处看看 2020-11-08 …
请用热化学方程式表示(1)1molN2(g)与适量H2(g)起反应,生成2molNH3(g),放出9 2021-02-16 …
依据事实,写出下列反应的热化学方程式.(1)1molN2(g)与适量H2(g)起反应,生成NH3(g 2021-02-16 …
依据事实,写出下列反应的热化学方程式.(1)1molN2(g)与适量H2(g)起反应生成NH3(g) 2021-02-16 …
(1)请用热化学方程式表示:A.1molN2(g)与适量H2(g)起反应,生成2molNH3(g), 2021-02-16 …
依据事实,写出下列反应的热化学方程式.(1)1molN2(g)与适量H2(g)起反应生成NH3(g) 2021-02-16 …