常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是()A.M点溶液中水的电离程度比原
常温下,向1L 0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )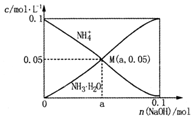
A. M点溶液中水的电离程度比原溶液大
B. a=0.05
C. 当n(NaOH)=0.05mol时溶液中有:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
D. 在M点时,n(OH-)-n(H+)=(a-0.05)mol
B.如果a=0.05,NH4Cl和NaOH反应后溶液中溶质为等物质的量的NH3.H2O和NH4Cl、NaCl,NH3.H2O的电离程度大于NH4Cl水解程度,导致溶液中c(NH4+)>c(NH3.H2O),要使混合溶液中c(NH4+)=c(NH3.H2O),则混合溶液中c(NH3.H2O)
C.当n(NaOH)=0.05mol时,NH4Cl和NaOH反应后溶液中溶质为等物质的量的NH3.H2O和NH4Cl、NaCl,NH3.H2O的电离程度大于NH4Cl水解程度,导致溶液呈碱性,钠离子、氯离子不水解,所以溶液中离子浓度大小顺序是c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故C错误;
D.M点存在的物料守恒为c(Cl-)=c(NH4+)+c(NH4+)=0.1mol/L,电荷守恒为c(Na+)+c(NH4+)+c(H+)=c(Cl-)+c(OH-),根据电荷守恒、物料守恒得c(OH-)-c(H+)=c(Na+)+c(NH4+)-c(Cl-)=(a+0.05-0.1)mol/L=(a-0.05)mol/L,n(OH-)-n(H+)=(a-0.05)mol/L×1L=(a-0.05)mol,故D正确;
故选D.
下列分子或离子在指定的分散系中能大量共存的一组是A.银氨溶液:Na+、K+、N、NH3•H2OB. 2020-04-13 …
离子平衡在100cm30.3mol/LNH4Cl中加入200cm30.3mol/LNaOH溶液,计 2020-04-26 …
高二化学求详细解释将 m mol/l的醋酸和n mol/l的氢氧化钠溶液等体积混合后溶液的PH 2020-05-13 …
某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA- H++A2-.关于下列四种溶液的说 2020-05-16 …
NaOH的溶液的PH值为9,所以溶液的H+为10-9.OH-为10-5,那么水电离的OH-和H+浓 2020-05-16 …
pH=6的稀盐酸稀释至1000倍,pH=?当强酸、强碱溶液的H+离子浓度接近水电离出的H+离浓度( 2020-05-17 …
弱酸稀释至n倍,c(H+)变化小于1/n假设强酸稀释n倍,c(H+)变化等于1/n.那么弱酸稀释之 2020-06-03 …
.求0.1mol/LHAc溶液的{H+}浓度,已知KaHAc=1.76x10^-5. 2020-06-03 …
某溶液的[H+]为0.1mol/L,该溶液的pH值是( )A.1B.2C.3D.4E.5 2020-06-07 …
请求一到化学题在一定温度下,在100mL某一元弱酸HA的溶液中,含有该弱酸的分子数为5.42×10 2020-06-27 …