25℃时,向盛有50mLpH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是A.HA溶液的物质的量浓度为0.0lm
25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是
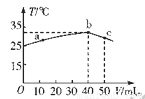
A.HA溶液的物质的量浓度为0.0l mol·L—1
B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应
C.a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+)
D.25℃时,HA的电离平衡常数K约为1.43×10—2
分 析:
A、当HA溶液和NaOH溶液恰好中和时混合溶液温度最高,即b点,此时消耗氢氧化钠的物质的量为0.004mol,得出HA的浓度为0.08mol/L,错误;B、b→c的过程中,温度降低的原因是加入温度较低的氢氧化钠溶液而使混合液的温度降低,错误;C、根据上述分析知,HA为弱酸,溶液呈酸性,NaA为强碱弱酸盐,溶液呈碱性,a→b的过程中,混合溶液中可能呈中性,存在:c(A-)=c(Na+),正确;D、电离平衡常数K=C(H+)·C(A-)/C(HA)=0.01×0.01÷0.08=1.25×10-3,错误。
考点:
考查酸碱混合问题的定性分析和计算。
A、B两种物质都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸 2020-04-11 …
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃).电解质平衡方程式平衡常数KK 2020-05-13 …
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃).电解质平衡方程式平衡常数KK 2020-05-13 …
溶酶体具有细胞内消化功能,其内部水解酶的最适pH在5.0左右.下列叙述错误的是()A.溶酶体内的水 2020-05-14 …
若80g质量分数为10%的氢氧化钠溶液与154g稀盐酸恰好完全中和,试计算反应后所得溶液中溶质质量 2020-05-14 …
(m0h4•黔西南州)&nhsp;如图是A、h、C三种固体物质的溶解度曲线,请回答.(h)th℃时 2020-05-15 …
5%的马来酸溶液中氧元素的质量分数为2.76%对吗,为什么?老师说是因为不知道马来酸溶液具体是多少 2020-07-17 …
有下列物质的溶液①CH3COOH②HCl③H2SO4④NaHSO4(1)若四种溶液的物质的量浓度相 2020-07-22 …
下列说法中正确的是()A常温下1L水中溶解0.01mol硫化氢,所得硫化氢溶液的浓度是0.01mo 2020-07-27 …
求NaOH的质量.有100g部分变质的NaOH溶液,向其中加入7.4g氢氧化钙恰好完全反应,过滤后得 2021-01-20 …