早教吧作业答案频道 -->化学-->
锰及其化合物在现代工业及国防建设中具有十分重要的地位.(1)隐形涂料是我国于2014年3月1日成功首飞的最新2011号歼20实现隐形的关键材料.锰锌铁氧体是当前广泛使用的一种隐形材料,
题目详情
锰及其化合物在现代工业及国防建设中具有十分重要的地位.
(1)隐形涂料是我国于2014年3月1日成功首飞的最新2011号歼20实现隐形的关键材料.锰锌铁氧体是当前广泛使用的一种隐形材料,其化学组成为MnxZn1-xFe2O4(铁为+3价),当锰、锌、铁三种金属的质量分数分别为4.6%、21.76%、46.86%时,所得到的锰锌铁氧体对雷达波的吸收能力最强,则锰锌铁氧体中锰元素的化合价为___,当雷达波吸收能力最强时x=___.
(2)碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)为主要原料制备碳酸锰的一种工艺流程如图所示
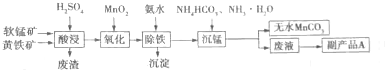
①写出提高酸浸时原料的浸出率的两种方法___,副产品A是___,从废墟中提取A的方法是___.
②酸浸时的氧化物是Fe3+、SO42-,写出对应的离子方程式:___,写出沉锰时反应的离子方程式:___
(3)KMnO4是一种十分重要的氧化剂,工业可以软锰矿为原料先制得锰酸钾,然后电解锰酸钾溶液就可以得到KMnO4,则电解时阳极上的电极反应式为___,当电路中有2 mol电子通过时,阳极上得到的产物的质量为___.
(1)隐形涂料是我国于2014年3月1日成功首飞的最新2011号歼20实现隐形的关键材料.锰锌铁氧体是当前广泛使用的一种隐形材料,其化学组成为MnxZn1-xFe2O4(铁为+3价),当锰、锌、铁三种金属的质量分数分别为4.6%、21.76%、46.86%时,所得到的锰锌铁氧体对雷达波的吸收能力最强,则锰锌铁氧体中锰元素的化合价为___,当雷达波吸收能力最强时x=___.
(2)碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)为主要原料制备碳酸锰的一种工艺流程如图所示

①写出提高酸浸时原料的浸出率的两种方法___,副产品A是___,从废墟中提取A的方法是___.
②酸浸时的氧化物是Fe3+、SO42-,写出对应的离子方程式:___,写出沉锰时反应的离子方程式:___
(3)KMnO4是一种十分重要的氧化剂,工业可以软锰矿为原料先制得锰酸钾,然后电解锰酸钾溶液就可以得到KMnO4,则电解时阳极上的电极反应式为___,当电路中有2 mol电子通过时,阳极上得到的产物的质量为___.
▼优质解答
答案和解析
(1)根据物质的量之比等于原子个数之比,得
:
=x:2,x=0.2;Zn的化合价为+2,根据物质的化合价为零,设Mn的化合价为y,则0.2y+2×0.8+2×3=4×2,y=+2;故答案为:+2;0.2;
(2)①升高温度、搅拌、减小固体的颗粒等均能加速固体的溶解,所以为了提高溶浸工序中原料的浸出效率,可以采取的措施有:适当升高温度,搅拌,研磨矿石,适当提高稀硫酸的浓度;溶浸过程中发生的反应生成硫酸根离子,后来又加入了氨水、碳酸氢铵,所以副产品是(NH4)2SO4,可以用重结晶法提取(NH4)2SO4;
故答案为:研磨矿石,适当提高稀硫酸的浓度等;(NH4)2SO4;重结晶法;
②FeS2与MnO2反应后生成Fe3+、Mn2+和SO42-,1molFeS2失去15mol电子,1molMnO2得到2mol电子,根据得失电子守恒,FeS2的计量数为2,MnO2的计量数为15,则生成的Fe3+计量数为2,SO42-的计量数为4,Mn2+的计量数为15,对应的离子方程式为2FeS2+15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42-;加入碳酸氢氨生成碳酸锰沉淀,离子方程式为Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
故答案为:2FeS2+15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42-;Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
(3)电解锰酸钾溶液时,阴极上水得电子生成氢气和氢氧根离子,电极反应为2H2O+2e-=H2↑+2OH-,阳极上锰酸根离子失电子生成高锰酸根离子,电极反应式为MnO42--e-=MnO4-;根据关系式:1e-~KMnO4,当电路中有1mol电子通过时,阳极上得到1molKMnO4,m(KMnO4)=1mol×158g/mol=158g;
故答案为:MnO42--e-=MnO4-;158g.
| 4.6% |
| 55 |
| 46.86% |
| 56 |
(2)①升高温度、搅拌、减小固体的颗粒等均能加速固体的溶解,所以为了提高溶浸工序中原料的浸出效率,可以采取的措施有:适当升高温度,搅拌,研磨矿石,适当提高稀硫酸的浓度;溶浸过程中发生的反应生成硫酸根离子,后来又加入了氨水、碳酸氢铵,所以副产品是(NH4)2SO4,可以用重结晶法提取(NH4)2SO4;
故答案为:研磨矿石,适当提高稀硫酸的浓度等;(NH4)2SO4;重结晶法;
②FeS2与MnO2反应后生成Fe3+、Mn2+和SO42-,1molFeS2失去15mol电子,1molMnO2得到2mol电子,根据得失电子守恒,FeS2的计量数为2,MnO2的计量数为15,则生成的Fe3+计量数为2,SO42-的计量数为4,Mn2+的计量数为15,对应的离子方程式为2FeS2+15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42-;加入碳酸氢氨生成碳酸锰沉淀,离子方程式为Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
故答案为:2FeS2+15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42-;Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
(3)电解锰酸钾溶液时,阴极上水得电子生成氢气和氢氧根离子,电极反应为2H2O+2e-=H2↑+2OH-,阳极上锰酸根离子失电子生成高锰酸根离子,电极反应式为MnO42--e-=MnO4-;根据关系式:1e-~KMnO4,当电路中有1mol电子通过时,阳极上得到1molKMnO4,m(KMnO4)=1mol×158g/mol=158g;
故答案为:MnO42--e-=MnO4-;158g.
看了锰及其化合物在现代工业及国防建...的网友还看了以下:
已知引力常量G和下列某组数据就能计算出地球的质量,这组数据是()A.地球绕太阳运行的周期及地球与太 2020-04-09 …
已知万有引力恒量,在以下各组数椐中,根椐哪几组可以测地球质量()A.地球绕太阳运行的周期及太阳与地 2020-04-11 …
已知引力常量G和下列某组数据,不能计算出地球质量。这组数据是[]A.地球绕太阳运行的周期及地球与太 2020-04-11 …
下列各组数据中,能计算出地球质量的是()A.地球绕太阳运行的周期及日、地间距离B.月球绕地球运行的 2020-05-14 …
已知万有引力常G和下列各组数据,能计算出地球质量的是()A.月球绕地球运行的周期及月球距地球的距离 2020-05-14 …
今天的汉语变化之快,已经是字典的改版的了,而所有这些的背后,是一个的社会.填入划横线部分最恰当的一 2020-06-12 …
教室里有一盒月饼,第一个同学过来拿了一块月饼以及剩余月饼的1/9,第二个同学拿了两块月饼以及剩余月 2020-06-14 …
下图示意某地区某月等温线分布,读图完成:小题1:该地区所在半球及图示月份为A.北半球7月B.北半球1 2020-11-02 …
我2013年,“嫦娥三号”计划将我国自主研发的“中华牌”月球车送上月球,使其完成使其完成月球软着陆过 2020-12-04 …
今年二月~五月玉米.猪肉统计表玉米500G(元)0.70.80.91猪肉同样7.5M6.256若今年 2020-12-28 …