早教吧作业答案频道 -->化学-->
你被遗忘在火星上,如何生存下去等待救援呢?(1)获得氢气.向火箭燃料液态联氨(N2H4)中加入铱催化剂,分解生成氮气和氢气.已知:3N2H4(l)⇌4NH3(g)+N2(g)△H=-336.6kJ•mol-1N2(g
题目详情
你被遗忘在火星上,如何生存下去等待救援呢?
(1)获得氢气.向火箭燃料液态联氨(N2H4)中加入铱催化剂,分解生成氮气和氢气.
已知:3N2H4(l)⇌4NH3(g)+N2(g)△H=-336.6kJ•mol-1
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
则N2H4(g)⇌N2(g)+2H2(g)△H=___kJ•mol-1,该反应平衡常数的表达式为___.
(2)获得氧气.火星大气中有稀薄的CO2.
以碱溶液为电解质可实现如下转化2CO2
2CO+O2,该反应在一定条件下能自发进行的原因是___,阴极的反应式为___.
(3)获得水.火星上含有高浓度高氯酸根的有毒卤水,可对其进行生物降解.
Ⅰ、在微生物的催化下,ClO4-可被CH3COO-还原,过程如图1所示,CH3COO-也可作为碳元素的来源,促进微生物生长.
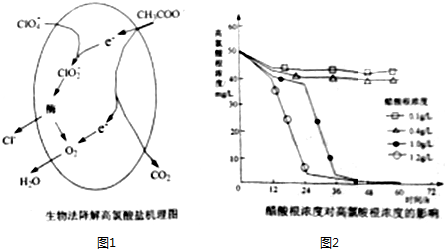
①该过程中总反应的离子方程式为___.
②CH3COO-的浓度对ClO4-降解程度的影响如图2所示,则12小时后,CH3COO-浓度小于0.4g/L的条件下,ClO4-的降解几乎停滞的原因是___.
Ⅱ.高氯酸、盐酸和硝酸的酸性在水溶液中差别不大.某温度下,这三种酸在冰醋酸中的电离平衡常数如表所示.冰醋酸做溶剂,这三种酸酸性最强的是___.在冰醋酸中,盐酸的电离方程式为___.
(1)获得氢气.向火箭燃料液态联氨(N2H4)中加入铱催化剂,分解生成氮气和氢气.
已知:3N2H4(l)⇌4NH3(g)+N2(g)△H=-336.6kJ•mol-1
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
则N2H4(g)⇌N2(g)+2H2(g)△H=___kJ•mol-1,该反应平衡常数的表达式为___.
(2)获得氧气.火星大气中有稀薄的CO2.
以碱溶液为电解质可实现如下转化2CO2
| ||
(3)获得水.火星上含有高浓度高氯酸根的有毒卤水,可对其进行生物降解.
Ⅰ、在微生物的催化下,ClO4-可被CH3COO-还原,过程如图1所示,CH3COO-也可作为碳元素的来源,促进微生物生长.

①该过程中总反应的离子方程式为___.
②CH3COO-的浓度对ClO4-降解程度的影响如图2所示,则12小时后,CH3COO-浓度小于0.4g/L的条件下,ClO4-的降解几乎停滞的原因是___.
Ⅱ.高氯酸、盐酸和硝酸的酸性在水溶液中差别不大.某温度下,这三种酸在冰醋酸中的电离平衡常数如表所示.冰醋酸做溶剂,这三种酸酸性最强的是___.在冰醋酸中,盐酸的电离方程式为___.
| 酸 | HClO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 1.6×10-9 | 4.2×10-10 |
▼优质解答
答案和解析
(1)已知:①3N2H4(l)⇌4NH3(g)+N2(g)△H=-336.6kJ•mol-1
②N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
据盖斯定律,则①×
-②×
得到N2H4(g)⇌N2(g)+2H2(g),所以
△H=(-336.6kJ•mol-1)×
(-92.4kJ•mol-1)=-50.6kJ•mol-1,平衡常数K=
=
,
故答案为:-50.6;K=
;
(2)转化2CO2
2CO+O2是一个熵增加的反应,有利于自发进行;在电解池的阴极上发生得电子的还原反应,阴极的反应式为:2CO2+4e-+2H2O=2CO+4OH-,
故答案为:△S>0;2CO2+4e-+2H2O=2CO+4OH-;
(3)Ⅰ、①微生物的催化下,ClO4-可被CH3COO-还原,得到二氧化碳和氯离子,离子方程式为:ClO4-+CH3COO-+H+=2CO2+2H2O+Cl-,故答案为:ClO4-+CH3COO-+H+=2CO2+2H2O+Cl-;
②根据CH3COO-的浓度对ClO4-降解程度的影响图可以看出:CH3COO-浓度过低,不能促进微生物生长CH3COO-浓度小于0.4g/L的条件下,ClO4-的降解几乎停滞,故答案为:CH3COO-浓度过低,不能促进微生物生长,失去催化作用,反应速率显著降低;
Ⅱ、电离平衡常数越大,酸的电离程度越大,酸性越强,所以这三种酸酸性最强的是HClO4;在冰醋酸中,盐酸不能完全电离,电离方程式为:HCl⇌H++Cl-.
故答案为:HClO4;HCl⇌H++Cl-.
②N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
据盖斯定律,则①×
| 1 |
| 3 |
| 2 |
| 3 |
△H=(-336.6kJ•mol-1)×
| 1 |
| 3 |
| 各生成物平衡浓度系数次幂之积 |
| 各反应物平衡浓度系数次幂之积 |
| [N2][H2]2 |
| [N2H4] |
故答案为:-50.6;K=
| [N2][H2]2 |
| [N2H4] |
(2)转化2CO2
| ||
故答案为:△S>0;2CO2+4e-+2H2O=2CO+4OH-;
(3)Ⅰ、①微生物的催化下,ClO4-可被CH3COO-还原,得到二氧化碳和氯离子,离子方程式为:ClO4-+CH3COO-+H+=2CO2+2H2O+Cl-,故答案为:ClO4-+CH3COO-+H+=2CO2+2H2O+Cl-;
②根据CH3COO-的浓度对ClO4-降解程度的影响图可以看出:CH3COO-浓度过低,不能促进微生物生长CH3COO-浓度小于0.4g/L的条件下,ClO4-的降解几乎停滞,故答案为:CH3COO-浓度过低,不能促进微生物生长,失去催化作用,反应速率显著降低;
Ⅱ、电离平衡常数越大,酸的电离程度越大,酸性越强,所以这三种酸酸性最强的是HClO4;在冰醋酸中,盐酸不能完全电离,电离方程式为:HCl⇌H++Cl-.
故答案为:HClO4;HCl⇌H++Cl-.
看了你被遗忘在火星上,如何生存下去...的网友还看了以下:
计算l0-5l-l(-4)-(+6)l-l(-7.5)+2-(+5.5)l11/4-[(-0.5) 2020-04-27 …
如图,在平面直角坐标系xoy中,多边形OABCDE的顶点坐标分别是O(0,0),A(0,6),B( 2020-05-16 …
负2.4加3.5减4.6加3.5 2020-06-02 …
神界危机4.6加强版飞哥刀证明有什么用? 2020-06-20 …
7.29乘4.6加46乘1.271可以简便计算吗? 2020-07-19 …
数学加减混合运算9分之5加1又6分之5加9分之4加(﹣2)|负7又8分之3加4又2分之1|加(负18 2020-12-17 …
你帮我回答的化简函数很厉害,你还可以帮我化简几道题吗?用卡诺图法化简1题L=∑m(0,1,3,5,7 2020-12-23 …
几道数学题1×2=22*3=2+43*4=2+4+64*5=2+4+6+8根据上述算式:1.请你推算 2020-12-28 …
如图所示为示波管的示意图,竖直偏转电极的极板长l=4.0cm,两板间距离d=1.0cm,极板右端与荧 2021-01-02 …
如图为示波管的示意图,竖直偏转电极的极板长l=4.0cm,两板间距离d=1.0cm,极板右端与荧光屏 2021-01-02 …