早教吧作业答案频道 -->化学-->
研究氮及其化合物的性质在人类进步过程中具有极为重要的意义.(1)工业上消除氮的氧化物可采用以下反应:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)△H在温度为T1和T2时,分别将0.5mol
题目详情
研究氮及其化合物的性质在人类进步过程中具有极为重要的意义.
(1)工业上消除氮的氧化物可采用以下反应:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)△H
在温度为T1和T2时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
①温度为T1℃时,0~20min内,v(CH4)=___.
②T1___T2(填“>”或“<”,下空同);△H___0,判断理由是___.
③反应CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=___,温度为T1℃时,K的值为___.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将___(填“增大”、“减小”或“不变”).
(2)已知反应N2O4(g)⇌2NO2(g),随温度升高,混合气体的颜色变深.将一定量N2O4气体充入如图绝热容器一段时间后,压缩和拉伸活塞过程中气体的透光率(气体颜色越浅,透光率越大)随时间变化如图所示.
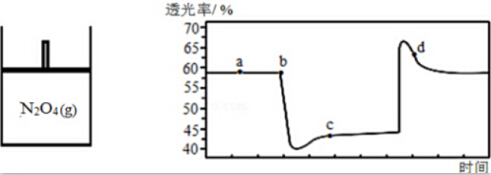
①a点与c点相比,c (NO2)更大的是___,体系温度更低的是___.
②d点,v正(NO2)___v逆(NO2)(填“>”、“<”或“=”).
③下列说法能说明透光率不再发生改变的有___.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变.
(1)工业上消除氮的氧化物可采用以下反应:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)△H
在温度为T1和T2时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
温度/℃ 时间/min | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
| T2 | 1.2 | 0.8 | 0.56 | … | 0.5 |
②T1___T2(填“>”或“<”,下空同);△H___0,判断理由是___.
③反应CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=___,温度为T1℃时,K的值为___.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将___(填“增大”、“减小”或“不变”).
(2)已知反应N2O4(g)⇌2NO2(g),随温度升高,混合气体的颜色变深.将一定量N2O4气体充入如图绝热容器一段时间后,压缩和拉伸活塞过程中气体的透光率(气体颜色越浅,透光率越大)随时间变化如图所示.

①a点与c点相比,c (NO2)更大的是___,体系温度更低的是___.
②d点,v正(NO2)___v逆(NO2)(填“>”、“<”或“=”).
③下列说法能说明透光率不再发生改变的有___.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变.
▼优质解答
答案和解析
(1)①温度为T1℃时,0~20min内v(NO2)=
=0.025mol/(L.s),速率之比等于化学计量数之比,则v(CH4)=
v(NO2)=0.0125mol/(L.s),
故答案为:0.0125mol/(L.s);
②由表中数据可知,T2温度反应速率较快,温度越高,反应速率越快,故温度T1<T2,温度T2先到达平衡,而升高温度,NO2的物质的量增大,说明平衡逆向移动,故正反应为放热反应,则△H<0,
故答案为:<;<;升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应;
③反应CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=
;
温度为T1℃时,40min到达平衡,平衡时二氧化氮物质的量为0.4mol,则:
CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)
起始量(mol):0.5 1.2 0 0 0
变化量(mol):0.4 0.8 0.4 0.4 0.8
平衡量(mol):0.1 0.4 0.4 0.4 0.8
容器的体积为1L,则平衡常数K=
=
=6.4,
故答案为:
;6.4;
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,等效再原平衡基础上增大压强,平衡逆向移动,达新平衡时CH4的转化率将减小,
故答案为:减小;
(2)①气体颜色越浅,透光率越大,则透光率越大,二氧化氮的浓度越小,a点透光率比c点大,c点c (NO2)更大;
随温度升高,混合气体的颜色变深,说明升高温度平衡正向移动,正反应为吸热反应,b点开始是压缩注射器的过程,平衡逆向移动,绝热条件下,容器内温度升高,故T(a)<T(c),
故答案为:c;a;
②d点后透光率减小,而二氧化氮浓度增大,平衡正向移动,故d点,v正(NO2)>v逆(NO2),
故答案为:>;
③透光率不再发生改变,说明二氧化氮的浓度不变,反应到达平衡,
a.气体颜色不再改变,说明二氧化氮浓度不变,透光率不再发生改变,故a正确;
b.焓变△H与是否到达平衡无关,与物质的聚集状态与化学计量数有关,故b错误;
c.应是2v正(N2O4)=v逆(NO2)时,反应到达平衡,二氧化氮的浓度不变,故c错误;
d.N2O4的转化率不再改变,反应到达平衡,二氧化氮的浓度不变,透光率不再发生改变,故d正确,
故选:ad.
| ||
| 20s |
| 1 |
| 2 |
故答案为:0.0125mol/(L.s);
②由表中数据可知,T2温度反应速率较快,温度越高,反应速率越快,故温度T1<T2,温度T2先到达平衡,而升高温度,NO2的物质的量增大,说明平衡逆向移动,故正反应为放热反应,则△H<0,
故答案为:<;<;升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应;
③反应CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=
| c(N2)×c(CO2)×c2(H2O) |
| c(CH4)×c2(NO2) |
温度为T1℃时,40min到达平衡,平衡时二氧化氮物质的量为0.4mol,则:
CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)
起始量(mol):0.5 1.2 0 0 0
变化量(mol):0.4 0.8 0.4 0.4 0.8
平衡量(mol):0.1 0.4 0.4 0.4 0.8
容器的体积为1L,则平衡常数K=
| c(N2)×c(CO2)×c2(H2O) |
| c(CH4)×c2(NO2) |
| 0.4×0.4×0.82 |
| 0.1×0.42 |
故答案为:
| c(N2)×c(CO2)×c2(H2O) |
| c(CH4)×c2(NO2) |
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,等效再原平衡基础上增大压强,平衡逆向移动,达新平衡时CH4的转化率将减小,
故答案为:减小;
(2)①气体颜色越浅,透光率越大,则透光率越大,二氧化氮的浓度越小,a点透光率比c点大,c点c (NO2)更大;
随温度升高,混合气体的颜色变深,说明升高温度平衡正向移动,正反应为吸热反应,b点开始是压缩注射器的过程,平衡逆向移动,绝热条件下,容器内温度升高,故T(a)<T(c),
故答案为:c;a;
②d点后透光率减小,而二氧化氮浓度增大,平衡正向移动,故d点,v正(NO2)>v逆(NO2),
故答案为:>;
③透光率不再发生改变,说明二氧化氮的浓度不变,反应到达平衡,
a.气体颜色不再改变,说明二氧化氮浓度不变,透光率不再发生改变,故a正确;
b.焓变△H与是否到达平衡无关,与物质的聚集状态与化学计量数有关,故b错误;
c.应是2v正(N2O4)=v逆(NO2)时,反应到达平衡,二氧化氮的浓度不变,故c错误;
d.N2O4的转化率不再改变,反应到达平衡,二氧化氮的浓度不变,透光率不再发生改变,故d正确,
故选:ad.
看了研究氮及其化合物的性质在人类进...的网友还看了以下:
1.下列词语中字形和加点字的读音全对的一项是()A.乐业(lè)行业(háng)羡慕(mù)断章取 2020-04-09 …
计算机进制换算题拜托了各位谢谢十进制数57.2D分别转换成二进制数B、八进制数O、十六进制数H。二 2020-06-09 …
一组宇航员乘坐太空穿梭机S,去修理位于离地球表面h=6.0×105m的圆形轨道上的太空望远镜H.机组 2020-11-21 …
一组太空人乘坐太空穿梭机去修理位于离地球表面h的圆形轨道上的哈勃太空望远镜H,机组人员使穿梭机S进入 2020-11-21 …
根据布拉凯特的充氮云室实验可知()A.质子是直接从氮核中打出来的B.α粒子打进氮核后形成一个复核,这 2020-11-26 …
我国工业结构调整正积极推进,将大力推进企业联合重组。加快推进企业兼并重组。中国汽车、钢铁行业之所以走 2020-11-28 …
已知在等温条件下,化学反应方向的判据为:ΔH-TΔS<0,反应能正向自发进行;ΔH-TΔS=0,反应 2020-12-15 …
湖南省政府近期发布了《关于做好促进就业工作的通知》,制定了一系列促进就业措施,积极扶持创业,以带动就 2020-12-18 …
计算机二级作业15.十进制数57.2D分别转换成二进制数B、八进制数O、十六进制数H.16.二进制数 2020-12-23 …
江苏省内部出现的这种产业转移,对苏北地区产生的有利影响是()①增加就业机会,促进市场繁荣②促进地方经 2020-12-30 …