早教吧作业答案频道 -->化学-->
化学反应中,物质所含元素的化合价发生变化的反应为氧化还原反应.其中化合价升高的物质发生氧化反应,作还原剂,元素化合价降低的物质发生还原反应,作氧化剂.(1)根据化合价
题目详情
化学反应中,物质所含元素的化合价发生变化的反应为氧化还原反应.其中化合价升高的物质发生氧化反应,作还原剂,元素化合价降低的物质发生还原反应,作氧化剂.
(1)根据化合价是否变化分析,下列反应属于氧化还原反应的是(填序号)___.
A、2Mg+O2
2MgO
B、CaO+H2O═Ca(OH)2
C、2H2O
2H2↑+O2↑
D、CaCO3
CaO+CO2↑
E、H2+CuO
Cu+H2O
F、HCl+NaOH═NaCl+H2O
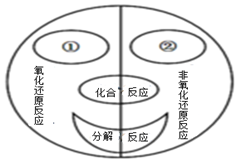
(2)如图是化学兴趣小组通过自主学习构建的四种基本反应类型与氧化-还原反应的关系图.根据此图回答下列问题:
①代表的基本反应类型是___;
②代表的基本反应类型是___;
③任意写出一个不属于四种基本反应类型,
但属于氧化-还原反应的化学方程式___,其中还原剂是___.
(3)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:C12+2NaBr═2NaCl+Br2;I2+Na2S═2NaI+S↓;Br2+2KI═2KBr+I2,由此可判断:
①S、C12、I2、Br2活动性由强到弱顺序是___;
②下列反应不能进行的是___.
A、C12+2NaI═2NaCl+I2
B、I2+2NaBr═2NaI+Br2
C、Br2+Na2S═2NaBr+S
D、C12+K2S═2KCl+S↓

(1)根据化合价是否变化分析,下列反应属于氧化还原反应的是(填序号)___.
A、2Mg+O2
| ||
B、CaO+H2O═Ca(OH)2
C、2H2O
| ||
D、CaCO3
| ||
E、H2+CuO
| ||
F、HCl+NaOH═NaCl+H2O
(2)如图是化学兴趣小组通过自主学习构建的四种基本反应类型与氧化-还原反应的关系图.根据此图回答下列问题:
①代表的基本反应类型是___;
②代表的基本反应类型是___;
③任意写出一个不属于四种基本反应类型,
但属于氧化-还原反应的化学方程式___,其中还原剂是___.
(3)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:C12+2NaBr═2NaCl+Br2;I2+Na2S═2NaI+S↓;Br2+2KI═2KBr+I2,由此可判断:
①S、C12、I2、Br2活动性由强到弱顺序是___;
②下列反应不能进行的是___.
A、C12+2NaI═2NaCl+I2
B、I2+2NaBr═2NaI+Br2
C、Br2+Na2S═2NaBr+S
D、C12+K2S═2KCl+S↓
▼优质解答
答案和解析
(1)A、Mg元素的化合价从0升高到+2价,O元素的化合价从0降低到-2价,有化合价的变化,属于氧化还原反应,故A正确;
B、反应中Ca、H、O三种元素的化合价都没有变化,则不属于氧化还原反应,故B错误;
C、H元素的化合价从+1降低到0,O元素的化合价从-2升高到0,有化合价的变化,属于氧化还原反应,故C正确;
D、反应中Ca、C、O三种元素的化合价都没有变化,则不属于氧化还原反应,故D错误;
E、H元素的化合价从0升高到+1,Cu元素的化合价从+2降低到0,有化合价的变化,属于氧化还原反应,故E正确;
F、反应中Na、H、O、Cl四种元素的化合价都没有变化,则不属于氧化还原反应,故F错误.
(2)分析①所处的位置可知它是属于氧化还原反应中的一种基本反应类型,因为氧化还原反应在反应前后有元素化合价发生变化,所以考虑基本反应类型中的置换反应,因为置换反应有单质参与和单质生成,所以一定有化合价变化,所以①代表的基本反应类型是置换反应,则②应该是复分解反应;不属于四种基本反应类型,但属于氧化还原反应的反应一定是有单质生成或参与,但不会是置换反应;如一氧化碳与氧化铁反应,化学方程式为:3CO+Fe2O3
2Fe+3CO2;其中CO是还原剂;
(2)①根据反应Cl2+2NaBr═2NaCl+Br2,得出Cl2>Br2;根据反应I2+Na2S═2NaI+S↓,得出I2>S;
根据反应Br2+2KI═2KBr+I2,得出Br2>I2.
故填:Cl2>Br2>I2>S;
②根据非金属活动性规律:Cl2>Br2>I2>S,可知Br2的活动性比I2强,因此单质I2不能把Br从其盐溶液中置换出来,所以反应I2+2KBr═2KI+Br2不正确.
故选:B.
故答案为:(1)ACE;(2)①置换反应;②复分解反应;③3CO+Fe2O3
2Fe+3CO2;CO(该题答案不唯一,合理即可)(3)①C12>Br2>I2>S;②B.
B、反应中Ca、H、O三种元素的化合价都没有变化,则不属于氧化还原反应,故B错误;
C、H元素的化合价从+1降低到0,O元素的化合价从-2升高到0,有化合价的变化,属于氧化还原反应,故C正确;
D、反应中Ca、C、O三种元素的化合价都没有变化,则不属于氧化还原反应,故D错误;
E、H元素的化合价从0升高到+1,Cu元素的化合价从+2降低到0,有化合价的变化,属于氧化还原反应,故E正确;
F、反应中Na、H、O、Cl四种元素的化合价都没有变化,则不属于氧化还原反应,故F错误.
(2)分析①所处的位置可知它是属于氧化还原反应中的一种基本反应类型,因为氧化还原反应在反应前后有元素化合价发生变化,所以考虑基本反应类型中的置换反应,因为置换反应有单质参与和单质生成,所以一定有化合价变化,所以①代表的基本反应类型是置换反应,则②应该是复分解反应;不属于四种基本反应类型,但属于氧化还原反应的反应一定是有单质生成或参与,但不会是置换反应;如一氧化碳与氧化铁反应,化学方程式为:3CO+Fe2O3
| ||
(2)①根据反应Cl2+2NaBr═2NaCl+Br2,得出Cl2>Br2;根据反应I2+Na2S═2NaI+S↓,得出I2>S;
根据反应Br2+2KI═2KBr+I2,得出Br2>I2.
故填:Cl2>Br2>I2>S;
②根据非金属活动性规律:Cl2>Br2>I2>S,可知Br2的活动性比I2强,因此单质I2不能把Br从其盐溶液中置换出来,所以反应I2+2KBr═2KI+Br2不正确.
故选:B.
故答案为:(1)ACE;(2)①置换反应;②复分解反应;③3CO+Fe2O3
| ||
看了化学反应中,物质所含元素的化合...的网友还看了以下:
第一题:在一定条件下,NO和氨气可以发生反应生成氮气和水.现有NO和氨气的混合物共1mol,充分反应 2020-03-31 …
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是()A.异 2020-04-06 …
A+B=C+D的反应中5gA物质跟4gB物质恰好完全反应,生成3gC物质和()gD物质这是根据什么 2020-05-02 …
1.将A、B、C各10g的混合物加热后,A全部参加反应,生成4gD,同时增加了8gC,则反应中A与 2020-05-02 …
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是()A.异 2020-05-13 …
已知IBr、SiCl4、PCl3、CH3COCl、CH3COOOCCH3常温下很容易与水反应,反应 2020-05-14 …
已知IBr、SiCl4、PCl3、CH3COCl、CH3COOOCCH3常温下很容易与水反应,反应 2020-05-14 …
氢气是一种十分熟悉的物质.在许多反应中既可以作为反应物,也可以作物生成物.(1)电解饱和食盐水制取 2020-05-14 …
已知硫醇RSH能和NaOH反应生成RSNa。化合物G()是合成治疗哮喘的药物MK-0476的中间体 2020-05-14 …
如图为植物光合作用过程图解.回答下列问题:(1)物质A是,D是;.(j)过程③称为,②表示COj的 2020-05-16 …