室温时,将0.10mol•L-1NaOH溶液滴入20.00mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积变化曲线如图.下列有关说法不正确的是()A.该一元酸溶液浓度为0.10mol•L-1B.a、b、c
室温时,将0.10mol•L-1 NaOH溶液滴入20.00mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积变化曲线如图.下列有关说法不正确的是( )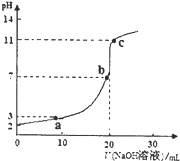
A. 该一元酸溶液浓度为0.10mol•L-1
B. a、b、c点的水溶液导电性依次增强
C. 室温时,HA的电离常数Ka≈1×10-5
D. a点和c点所示溶液中H2O的电离程度相同
B、溶液的导电能力与离子浓度成正比,HA是弱电解质,NaOH、NaA是强电解质,完全电离,根据图象知,a、b、c点的水溶液中,溶液中自由移动离子浓度逐渐增大,所以其导电性依次增强,故B正确;
C、根据图象知,0.10mol/LHA溶液中pH=2,则c(H+)=0.01mol/L,HA的电离常数Ka=
| [H+]•[A-] |
| [HA] |
| (0.01)2 |
| 0.1-0.01 |
D、D、a点c(H+)=0.01mol/L,则由水电离出来的c(OH-)=1.0×10-11,c点c(H+)=1.0×10-11全部由水电离出来,故D正确;
故选C.
设l,m是两条不同的直线,a是一个平面,有下列四个命题:(1)若l⊥a,m⊂a,则l⊥m;(2)若 2020-05-13 …
高中数学困惑根据下列符号表示的语句,说明点、线、面之间的位置关系l⊂a,m∩a=A,A不属于l书上 2020-05-13 …
25℃时,浓度均为0.1mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是 2020-05-14 …
已知直线l:2x-3y+1=0,点A(-1,-2),求:1>点A关于l的对称点A'的坐标;2>直线 2020-05-16 …
设直线l的方程为(a+1)x+y-2-a=0(x∈R)若直线l在两坐标轴上的截距相等,求l方程.: 2020-05-16 …
已知直线L过点P(1,0,-1),平行于向量a=(2,1,1),平面过直线L与点M(1,2,3,) 2020-05-16 …
已知直线L:(a-1)x+y+a+1=0及定点A(3,4),a为何值时,点A到L的距离最大 2020-06-06 …
会公差的进来下1用游标卡尺测量2孔中心距有3种方法,其中测量精度最高的是(xx)A分别量出2孔的内 2020-07-09 …
表内末尾句号都要去掉吗2011年标点新规附录A.1说:图或表的短语式说明文字,句子末尾不用句号;或者 2020-11-08 …
三角函数sinθ=L/a-1,tanθ=√3/6(a为已知量,用两条式子求出L) 2020-12-05 …