早教吧作业答案频道 -->化学-->
用含钴废料(主要成分为Co,含有一定量的Ni、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4•2H2O)的工业流程如图.己知:①草酸钴晶体难溶于水②RH为有机物(难电离)(1)滤渣I的主要成分
题目详情
用含钴废料(主要成分为Co,含有一定量的Ni、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4•2H2O)的工业流程如图.己知:①草酸钴晶体难溶于水②RH为有机物(难电离)
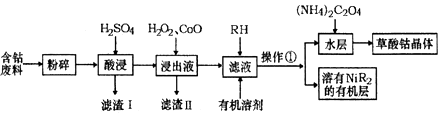
(1)滤渣I的主要成分是___(填化学式),写出一种能提高酸浸速率的措施___.
(2)操作①用到的主要仪器有___.
(3)H2O2是一种绿色氧化剂,写出加入H2O2后发生反应的离子方程式___.
(4)加入氧化钴的目的是___.
(5)草酸钴晶体分解后可以得到多种钴的氧化物(其中Co的化合价为+2、+3),取一定量钴的氧化物,用280mL 5mol/L盐酸恰好完全溶解,并得到CoCl2溶液和2.24L(标准状况)黄绿色气体,由此可确定该钴氧化物中Co、O的物质的量之比为___.
(6)实验室可以用酸性KMnO4标准液滴定草酸根离子(C2O42-),测定溶液中C2O42-的浓度,写出此反应的离子方程式___;KMnO4 标准溶液常用硫酸酸化,若用盐酸酸化,会使测定结果___(填“偏高”、“偏低”或“无影响”).

(1)滤渣I的主要成分是___(填化学式),写出一种能提高酸浸速率的措施___.
(2)操作①用到的主要仪器有___.
(3)H2O2是一种绿色氧化剂,写出加入H2O2后发生反应的离子方程式___.
(4)加入氧化钴的目的是___.
(5)草酸钴晶体分解后可以得到多种钴的氧化物(其中Co的化合价为+2、+3),取一定量钴的氧化物,用280mL 5mol/L盐酸恰好完全溶解,并得到CoCl2溶液和2.24L(标准状况)黄绿色气体,由此可确定该钴氧化物中Co、O的物质的量之比为___.
(6)实验室可以用酸性KMnO4标准液滴定草酸根离子(C2O42-),测定溶液中C2O42-的浓度,写出此反应的离子方程式___;KMnO4 标准溶液常用硫酸酸化,若用盐酸酸化,会使测定结果___(填“偏高”、“偏低”或“无影响”).
▼优质解答
答案和解析
(1)用含钴废料,粉碎后用硫酸溶解,SiO2不与硫酸反应,滤渣Ⅰ为SiO2,提高硫酸的浓度、提高反应的温度、搅拌能提高酸浸速率;
故答案为:SiO2;提高硫酸的浓度、提高反应的温度、搅拌;
(2)通过操作①得到水层和有机层,则操作①为分液,分液需要的仪器有:分液漏斗、烧杯;
故答案为:分液漏斗、烧杯;
(3)H2O2氧化亚铁离子生成铁离子,离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(4)加入氧化钴的目的是调节溶液的pH,使铁离子铝离子沉淀;
故答案为:调节溶液pH;
(5)取一定量钴的氧化物,用280mL 5mol/L盐酸恰好完全溶解,则n(Cl)=0.28L×5mol/L=1.4mol,有得到CoCl2溶液和2.24L(标准状况)黄绿色气体,n(Cl2)=
=0.1mol,故n(CoCl2)=0.6mol,则n(Co原子)总=0.6mol,
由电子守恒:Cl2~2e-~2Co3+,则n(Co3+)=2n(Cl2)=0.2mol,
所以固体中的n(Co2+)=0.6mol-0.2mol=0.4mol,
根据化合价为0,氧化物中n(O)=(0.2mol×3+0.4mol×2)÷2=0.7mol,
故该钴氧化物中n(Co):n(O)=0.6mol:0.7mol=6:7;
故答案为:6:7;
(6)用酸性KMnO4标准液滴定草酸根离子(C2O42-),发生氧化还原反应,离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++l0CO2↑+8H2O,KMnO4 标准溶液常用硫酸酸化,若用盐酸酸化,高锰酸钾会氧化盐酸中的氯离子,消耗高锰酸钾偏多,测定结果偏高;
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++l0CO2↑+8H2O;偏高.
故答案为:SiO2;提高硫酸的浓度、提高反应的温度、搅拌;
(2)通过操作①得到水层和有机层,则操作①为分液,分液需要的仪器有:分液漏斗、烧杯;
故答案为:分液漏斗、烧杯;
(3)H2O2氧化亚铁离子生成铁离子,离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(4)加入氧化钴的目的是调节溶液的pH,使铁离子铝离子沉淀;
故答案为:调节溶液pH;
(5)取一定量钴的氧化物,用280mL 5mol/L盐酸恰好完全溶解,则n(Cl)=0.28L×5mol/L=1.4mol,有得到CoCl2溶液和2.24L(标准状况)黄绿色气体,n(Cl2)=
| 2.24L |
| 22.4L/mol |
由电子守恒:Cl2~2e-~2Co3+,则n(Co3+)=2n(Cl2)=0.2mol,
所以固体中的n(Co2+)=0.6mol-0.2mol=0.4mol,
根据化合价为0,氧化物中n(O)=(0.2mol×3+0.4mol×2)÷2=0.7mol,
故该钴氧化物中n(Co):n(O)=0.6mol:0.7mol=6:7;
故答案为:6:7;
(6)用酸性KMnO4标准液滴定草酸根离子(C2O42-),发生氧化还原反应,离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++l0CO2↑+8H2O,KMnO4 标准溶液常用硫酸酸化,若用盐酸酸化,高锰酸钾会氧化盐酸中的氯离子,消耗高锰酸钾偏多,测定结果偏高;
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++l0CO2↑+8H2O;偏高.
看了用含钴废料(主要成分为Co,含...的网友还看了以下:
电荷守恒的!在碳酸氢钠中,氢离子浓度+钠离子浓度=碳酸氢根离子浓度+2×碳酸根离子浓度+氢氧根离子 2020-05-13 …
一个半径为R的带电球体,其电荷体密度p=kr^2,r是到球心的距离,求带电体的电场分布规律我想知道 2020-05-13 …
高锰酸根与+2价的锰离子高锰酸根在酸性条件下发生氧化还原反应生成+2价,但是又可以和+2价锰离子发 2020-05-14 …
圆和直线方程D的应用题已知圆x^2+y^2=4l:y=x+b当b为何值时x^2+y^2=4恰有3点 2020-05-22 …
设弧所在圆的半径是R,则圆心到弦的距离是:R-3.根据勾股定理:R^2=(R-3)^2+(19.7 2020-06-05 …
同步卫星离地心距离为r.加速度为a1地球赤道上物体向心加速度为a2,地球半径为R则a1/a2=r/ 2020-06-07 …
把固体柠檬酸加进碳酸氢钠水溶液中,混合物会泛起泡沫.下列离子或化合物,何者导致泡沫泛起?1.钠离子 2020-06-28 …
已知:氧化性高锰酸根离子大于三价铁离子.还原性碘离子大于2价铁离子.在酸性条件下.将分别含有高锰酸 2020-07-08 …
若半径为r的圆C,x^2+y^2+Dx+Ey+F=0,的圆心C到直线l:Dx+Ey+F=0的距离为 2020-07-26 …
复习酸,碱,盐资料一、认识酸、碱、盐1.酸的概念:电离时,生成的阳离子是离子的化合物.酸→H++酸根 2020-11-23 …