早教吧作业答案频道 -->化学-->
钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域.(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性.①该催化剂中铁元素的化合价为.②
题目详情
钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域.
(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性.
①该催化剂中铁元素的化合价为___.
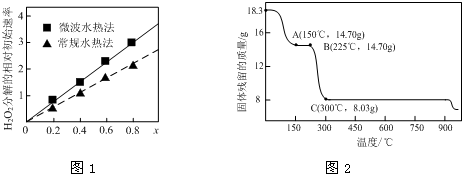
②图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线.由图中信息可知:___法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是___.
(2)草酸钴是制备钴的氧化物的重要原料.下图2为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.
①通过计算确定C点剩余固体的化学成分为___(填化学式).试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式:___.
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480mL 5mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体.试确定该钴氧化物中Co、O的物质的量之比.___.
(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性.
①该催化剂中铁元素的化合价为___.
②图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线.由图中信息可知:___法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是___.
(2)草酸钴是制备钴的氧化物的重要原料.下图2为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.
①通过计算确定C点剩余固体的化学成分为___(填化学式).试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式:___.

②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480mL 5mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体.试确定该钴氧化物中Co、O的物质的量之比.___.
▼优质解答
答案和解析
(1)①CoxNi(1-x)Fe2O4中Co、Ni均为+2,O为-2价,则Fe的化合价为
=+3,
故答案为:+3;
②过氧化氢的分解速率越大,催化剂活性更高,根据图象可知,x相同时,微波水热法初始速度大于常规水热法,故微波水热法制得催化剂的活性更高;
由图可知,随x值越大,过氧化氢的分解速率越大,而x增大,Co2+的比例增大,故Co2+的催化活性更高,
故答案为:微波水热;Co2+;
(2)①由图可知,CoC2O4•2H2O的质量为18.3g,其物质的量为0.1mol,Co元素质量为5.9g,C点钴氧化物质量为8.03g,氧化物中氧元素质量为8.03g-5.9g=2.13g,则氧化物中Co原子与O原子物质的量之比为0.1mol:
≈3:4,故C的Co氧化物为Co3O4;
B点对应物质的质量为14.7g,与其起始物质的质量相比减少18.3g-14.7g=3.6g,为结晶水的质量,故B点物质为CoC2O4,与氧气反应生成Co3O4与二氧化碳,反应方程式为:3CoC2O4+2O2
Co3O4+6CO2,
故答案为:Co3O4;3CoC2O4+2O2
Co3O4+6CO2;
②由电子守恒:n(Co3+)=2 n(Cl2)=2×
=0.4 mol,
由电荷守恒:n(Co原子)总=n(Co2+)溶液=
n(Cl-)=
×( 0.48L×5mol/L-0.4mol)=1 mol,所以固体中的n(Co2+)=1mol-0.4mol=0.6 mol,
根据化合价电荷守恒为0,氧化物中n(O)=(0.6mol×2+0.4mol×3)÷2=1.2mol,
故该钴氧化物中n(Co):n(O)=1mol:1.2mol=5:6,
故答案为:5:6.
| 4×2-(2x+2-2x) |
| 2 |
故答案为:+3;
②过氧化氢的分解速率越大,催化剂活性更高,根据图象可知,x相同时,微波水热法初始速度大于常规水热法,故微波水热法制得催化剂的活性更高;
由图可知,随x值越大,过氧化氢的分解速率越大,而x增大,Co2+的比例增大,故Co2+的催化活性更高,
故答案为:微波水热;Co2+;
(2)①由图可知,CoC2O4•2H2O的质量为18.3g,其物质的量为0.1mol,Co元素质量为5.9g,C点钴氧化物质量为8.03g,氧化物中氧元素质量为8.03g-5.9g=2.13g,则氧化物中Co原子与O原子物质的量之比为0.1mol:
| 2.13g |
| 16g/mol |
B点对应物质的质量为14.7g,与其起始物质的质量相比减少18.3g-14.7g=3.6g,为结晶水的质量,故B点物质为CoC2O4,与氧气反应生成Co3O4与二氧化碳,反应方程式为:3CoC2O4+2O2
| ||
故答案为:Co3O4;3CoC2O4+2O2
| ||
②由电子守恒:n(Co3+)=2 n(Cl2)=2×
| 4.48L |
| 22.4L/mol |
由电荷守恒:n(Co原子)总=n(Co2+)溶液=
| 1 |
| 2 |
| 1 |
| 2 |
根据化合价电荷守恒为0,氧化物中n(O)=(0.6mol×2+0.4mol×3)÷2=1.2mol,
故该钴氧化物中n(Co):n(O)=1mol:1.2mol=5:6,
故答案为:5:6.
看了钴及其化合物广泛应用于磁性材料...的网友还看了以下:
在比较2的16次方和3的12次方的大小时,我们可以这样来处理:你能类似地比较出①2的100次方与3 2020-04-07 …
已知关于X的一元二次方程x^2+2(k-1)x+k^2-1=0有两个不相等的实数根已知关于x的一元 2020-05-16 …
通过(1)的比较,请你分析、归纳出当a,b为有理数时,IaI+IbI与Ia+bI的大小关系1.I- 2020-06-11 …
比较句子,哪个好?为什么?(1)1,一排排高楼大厦像雨后春笋,一件件家用电器琳琅满目.2,一排排高 2020-07-12 …
已知某强氧化剂[RO(OH)2]2+离子中的元素R可被亚硫酸钠还原到较低价态.若把1.2×10-3 2020-07-25 …
请帮我想想如何用较简便的方法解这题:过直线x+y+1=0和圆x^2+y^2-2x-2y-7=0的交 2020-07-26 …
y=f(x)在(0,2)上是增函数且f(x+2)的图像关于y轴对称比较f(π/2)f(π/4f(大 2020-08-01 …
(x-2)^2=9(x+3)(步骤)用十字相乘法:x^2-5倍的根号2*x+83x^2-2x-1= 2020-08-03 …
虽然有些问的比较2,1.检验SO42-加HCl酸化,无明显现象,再加BaCl2,若产生白色沉淀说明有 2020-11-01 …
比较2−1与3−2的大小可以采用下面的方法:2−1=(2−1)(2+1)2+1=2−12+1=12+ 2020-12-04 …