早教吧作业答案频道 -->化学-->
已知R、W、X、Y、Z是周期表中前四周期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同
题目详情
已知R、W、X、Y、Z是周期表中前四周期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1; W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同的电子层结构;Y元素 原子的3P能级处于半充满状态;Z+的电子层都充满电子.请回答下列问题:
(1)写出Z的基态原子的外围电子排布式___.
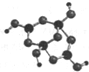
(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如上图所示:在Am-中,R原子轨道杂化类型有___;m=___.(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子 所构成的立体几何构型为___.
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]S04,下列说法正确的是___
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH3)4]2+中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4的组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是YCl4+和YCl6- 构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为a pm,则晶胞的密度为___g•cm-3.

(1)写出Z的基态原子的外围电子排布式___.
(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如上图所示:在Am-中,R原子轨道杂化类型有___;m=___.(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子 所构成的立体几何构型为___.
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]S04,下列说法正确的是___
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH3)4]2+中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4的组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是YCl4+和YCl6- 构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为a pm,则晶胞的密度为___g•cm-3.
▼优质解答
答案和解析
R、W、X、Y、Z是周期表中前四周期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1,及p能级只有1个电子,R原子核外电子排布为1s22s22p1,故R为硼元素;Y元素原子的3p能级处于半充满状态,Y原子的核外电子排布为1s22s22p63s23p3,故Y为磷元素;W的氢化物的沸点比同族其它元素氢化物的沸点高,考虑氢键的存在,且X2+与W2-具有相同的电子层结构,故X处于第三周期、W处于第二周期,故X为Mg元素、W为氧元素;Z+的电子层都充满电子,各层电子数为2、8、18,故Z原子核外电子数为2+8+18+1=29,故Z为Cu元素,
(1)Z为Cu元素,原子核外电子数为29,原子核外电子排布式为1s22s22p63s23p63d104s1,Cu的基态原子的外围电子排布式为3d104s1,
故答案为:3d104s1;
(2)H原子成1个键,O原子成2个键,B原子一般是形成3个键,B形成4个键,其中1个键很可能就是配位键,则成3个键的B原子为SP2杂化,成4个键的B为SP3杂化;
观察模型,可知Am-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,
故答案为:SP2、SP3;2;
(3)经X射线探明,Mg与O形成化合物的晶体结构与NaCl的晶体结构相似,Mg2+的周围有6个O原子,为如图结构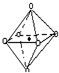 ,故配位原子所构成的立体几何构型为正八面体,
,故配位原子所构成的立体几何构型为正八面体,
故答案为:正八面体;
(4)A.[Z(NH3)4]SO4中,内界离子[Cu(NH3)4]2+与外界离子SO42形成离子键,Cu2+与NH3形成配位键,NH3中N原子与H原子之间形成极性键,故A正确;
B.在[Z(NH3)4]SO4中Z2+提供空轨道,NH3给出孤对电子,故B错误;
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是N元素,故C错误;
D.SO42-与PO43-互为等电子体,价层电子总数相同,空间结构相同,SO42-中S原子成4个σ键,孤对电子对数为
=0,价层电子对为4,为正四面体,故D正确;
故答案为:AD;
(5)固体PCl5的结构实际上是PCl4+和PCl6-构成的离子晶体,其晶体结构与CsCl相似,则晶胞的组成为P2Cl10,晶胞中相当于含有2个PCl5,若晶胞边长为apm,则晶胞的密度为
=
g•cm-3,
故答案为:
.
(1)Z为Cu元素,原子核外电子数为29,原子核外电子排布式为1s22s22p63s23p63d104s1,Cu的基态原子的外围电子排布式为3d104s1,
故答案为:3d104s1;
(2)H原子成1个键,O原子成2个键,B原子一般是形成3个键,B形成4个键,其中1个键很可能就是配位键,则成3个键的B原子为SP2杂化,成4个键的B为SP3杂化;
观察模型,可知Am-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,
故答案为:SP2、SP3;2;
(3)经X射线探明,Mg与O形成化合物的晶体结构与NaCl的晶体结构相似,Mg2+的周围有6个O原子,为如图结构
 ,故配位原子所构成的立体几何构型为正八面体,
,故配位原子所构成的立体几何构型为正八面体,故答案为:正八面体;
(4)A.[Z(NH3)4]SO4中,内界离子[Cu(NH3)4]2+与外界离子SO42形成离子键,Cu2+与NH3形成配位键,NH3中N原子与H原子之间形成极性键,故A正确;
B.在[Z(NH3)4]SO4中Z2+提供空轨道,NH3给出孤对电子,故B错误;
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是N元素,故C错误;
D.SO42-与PO43-互为等电子体,价层电子总数相同,空间结构相同,SO42-中S原子成4个σ键,孤对电子对数为
| 6+2-4×2 |
| 2 |
故答案为:AD;
(5)固体PCl5的结构实际上是PCl4+和PCl6-构成的离子晶体,其晶体结构与CsCl相似,则晶胞的组成为P2Cl10,晶胞中相当于含有2个PCl5,若晶胞边长为apm,则晶胞的密度为
| ||
| (a×10-10cm)3 |
| 417×1030 |
| a3NA |
故答案为:
| 417×1030 |
| a3NA |
看了已知R、W、X、Y、Z是周期表...的网友还看了以下:
短周期元素abcd的原子序数依次增大短周期元素ABCD的原子序数依次增大,他们的原子序数之和,为3 2020-04-08 …
已知X、Y、Z、W是短周期中的四种金属元素,他们的原子序数依次增大X元素的原子形成的离子已知X、Y 2020-04-08 …
JAVA一个球从100米高空落下,每次落地后弹回原高度的一半再落下,求在几次吼反弹高度小于0.1米 2020-07-15 …
化学推断题(高一下期)A、B、C、D为短周期元素(除稀有气体元素外),它们的原子序数依次增大,其中 2020-07-29 …
已知R、W、X、Y、Z是周期表中前四周期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨 2020-10-31 …
一个球从a米高处自由落下,每次着地后有跳回到原高度的一半后再落下一个球从a米高处自由落下,每次着地后 2020-11-24 …
下列递变规律不正确的是()A.Na、Mg、Al还原性依次减弱B.I2、Br2、Cl2氧化性依次增强C 2020-11-27 …
短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,且X、Y、W原子 2020-12-05 …
下列说法正确的是A.Li、Na、K原子的电子层数依次增多,最高正价依次升高B.Si、P、S、Cl的原 2021-01-05 …
(2012•醴陵市模拟)有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次增大.B元素的最 2021-01-05 …