早教吧作业答案频道 -->化学-->
工业上测定SO2、N2、O2混合气体中SO2含量的装置如图.反应管中装有碘的淀粉溶液,SO2和I2发生反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI(1)混合气体进入反应管后,量气管内增加的水
题目详情
工业上测定SO2、N2、O2混合气体中SO2含量的装置如图.反应管中装有碘的淀粉溶液,SO2和I2发生反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI
(1)混合气体进入反应管后,量气管内增加的水的体积等于___的体积(填写混合气体的分子式)
(2)读数前应冷却到室温、___、___
(3)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量___(选填:偏高,偏低,不受影响)
(4)若碘溶液体积为Va mL,浓度为Cmol/L.N2与O2的体积为Vb mL(已折算成标准状况下的体积).用C、Va、Vb表示SO2的体积百分含量为___.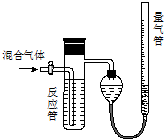
(1)混合气体进入反应管后,量气管内增加的水的体积等于___的体积(填写混合气体的分子式)
(2)读数前应冷却到室温、___、___
(3)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量___(选填:偏高,偏低,不受影响)
(4)若碘溶液体积为Va mL,浓度为Cmol/L.N2与O2的体积为Vb mL(已折算成标准状况下的体积).用C、Va、Vb表示SO2的体积百分含量为___.

▼优质解答
答案和解析
(1)混合气体进入反应管中,其中SO2与I2发生反应:SO2+I2+2H2O=H2SO4+2HI不产生气体,剩余的气体仅有N2和O2,量气管内增加的水的体积等于N2和O2的总体积,
故答案为:N2、O2;
(2)读数时,要注意视线应于量气管凹液面的最低处保持水平;每次读数前应上下移动水准管,待两管液面相平再读数是为了防止水的压强造成的误差
故答案为:调整量器筒内外液面高度相平;平视凹液面读数;
(3)根据反应:SO2+I2+2H2O═H2SO4+2HI可求出吸收的SO2的体积:V(SO2)=Vm×n(I2),SO2的体积百分含量φ(SO2)=
式中V(SO2)的量是由n(I2)的物质的量决定的,而“没有及时停止通气”就会使得V(混合气体)增大,则φ(SO2)偏低,
故答案为:偏低;
(4)由所给反应知SO2气体的物质的量等于碘的物质的量Va×10-3L×c mol•L-1=Vac×10-3mol,其体积为V(SO2)=Vac×10-3mol×22400 mL•mol-1=22.4Va•c mL,所以SO2的体积百分含量为=
×100%,即SO2的百分含量为:
×100%,
故答案为:
×100%.
故答案为:N2、O2;
(2)读数时,要注意视线应于量气管凹液面的最低处保持水平;每次读数前应上下移动水准管,待两管液面相平再读数是为了防止水的压强造成的误差
故答案为:调整量器筒内外液面高度相平;平视凹液面读数;
(3)根据反应:SO2+I2+2H2O═H2SO4+2HI可求出吸收的SO2的体积:V(SO2)=Vm×n(I2),SO2的体积百分含量φ(SO2)=
| V(SO2) |
| V(混合气体) |
故答案为:偏低;
(4)由所给反应知SO2气体的物质的量等于碘的物质的量Va×10-3L×c mol•L-1=Vac×10-3mol,其体积为V(SO2)=Vac×10-3mol×22400 mL•mol-1=22.4Va•c mL,所以SO2的体积百分含量为=
| 22.4cVa |
| 22.4Va+Vb |
| 22.4cVa |
| 22.4Va+Vb |
故答案为:
| 22.4cVa |
| 22.4Va+Vb |
看了工业上测定SO2、N2、O2混...的网友还看了以下:
求助一道关于洗牌的题目,麻烦高手写一下推理步骤,不胜感激!任意6张扑克,假设为红桃8,9,10,J 2020-05-16 …
回答实验室用高锰酸钾制取氧气的相关问题.(1)如图1所示,发生装置应选用,(填编号,下同)收集装置 2020-07-05 …
活动与探究定量测定空气中氧气的含量.(1)装置一和装置二中气球的位置不同,(填“装置一”或“装置二 2020-07-18 …
甲在纸上写了一个数,让乙猜.乙猜7538,甲说对了2个数字,但位置不正确,乙猜1269,甲说对了2 2020-07-26 …
如图,△ABC的三个顶点位置分别是A(1,0),B(-2,3),C(-3,0).(1)求△ABC的 2020-07-26 …
甲乙丙三人所处位置不同,甲说以我坐标为原点,乙的位置是(2,3)丙说以我的位置为坐标原点,乙的位置 2020-07-30 …
用行初等变换求矩阵的逆矩阵:求x1=(1,2,2)的转置,X2=(2,-2,1)的转置,X3=(- 2020-08-02 …
不同的音调的相同音阶在吉他上弹的位置为啥是不一样的比方说CE调的1DAO音在吉他上弹的位置不一样我搞 2020-11-10 …
我想问一下,对于对称阵的相似对角化,可以不单位化吗,我们书上的都是有单位化比如有一题是,设3阶对称阵 2020-11-28 …
一个N极朝下的条形磁铁竖直下落,恰能穿过水平防止的方形导线框,1位置在线框之上,2位置在线框之上,1 2020-12-17 …