二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:某软锰矿的主要成分为MnO2还含Si(16.27%)、Fe(
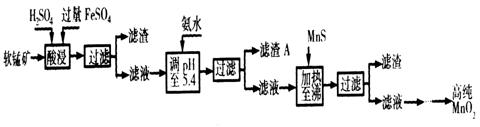
二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
![]()
![]()
![]()
![]()
![]() 某软锰矿的主要成分为MnO 2 还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
某软锰矿的主要成分为MnO 2 还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 |
![]()
| 沉淀物 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(1)硫酸亚铁在酸性条件下将MnO 2 还原为MnSO 4 ,酸浸时发生的主要反应的化学方程式为 。
![]() (2)滤渣A的主要成分为 。
(2)滤渣A的主要成分为 。
![]() (3)加入MnS的目的是除去 杂质。
(3)加入MnS的目的是除去 杂质。
![]() (4)碱性锌锰干电池中,MnO 2 参与的电极反应方程式为 。
(4)碱性锌锰干电池中,MnO 2 参与的电极反应方程式为 。
![]() (5)从废旧碱性锌锰干电池中可以回收利用的物质有 (写出两种)。
(5)从废旧碱性锌锰干电池中可以回收利用的物质有 (写出两种)。
(1)MnO 2 +2FeSO 4 +2H 2 SO 4 MnSO 4 +Fe 2 (SO 4 ) 3 +2H 2 O
![]() (2)Fe(OH) 3 、Al(OH) 3
(2)Fe(OH) 3 、Al(OH) 3
![]() (3)Cu 2+ 、Zn 2+
(3)Cu 2+ 、Zn 2+
![]()
![]()
![]() (4)MnO 2 +H 2 O+e - MnOOH+OH - (或2MnO 2 +H 2 O+2e - Mn 2 O 3 +2OH - )
(4)MnO 2 +H 2 O+e - MnOOH+OH - (或2MnO 2 +H 2 O+2e - Mn 2 O 3 +2OH - )
![]() (5)锌、二氧化锰
(5)锌、二氧化锰![]()
![]()
![]()
![]()
(1)根据FeSO 4 在反应条件下将MnO 2 还原为MnSO 4 ,Fe 2+ 被氧化为Fe 3+ ,可以写其反应方程式2FeSO 4 +MnO 2 +2H 2 SO 4 MnSO 4 +Fe 2 (SO 4 ) 3 +2H 2 O。
![]() (2)根据反应后滤液(Mn 2+ 、Fe 3+ 、Al 3+ 、Cu 2+ 、Zn 2+ 、Fe 2+ )加氨水调pH至5.4,结合题表可知滤渣A的主要成分为Fe(OH) 3 和Al(OH) 3 。
(2)根据反应后滤液(Mn 2+ 、Fe 3+ 、Al 3+ 、Cu 2+ 、Zn 2+ 、Fe 2+ )加氨水调pH至5.4,结合题表可知滤渣A的主要成分为Fe(OH) 3 和Al(OH) 3 。
![]() (3)根据题表可知加入MnS是为了生成溶解度更小的CuS、ZnS而除去Cu 2+ 、Zn 2+ 。
(3)根据题表可知加入MnS是为了生成溶解度更小的CuS、ZnS而除去Cu 2+ 、Zn 2+ 。
![]()
![]()
![]() (4)碱性锌锰干电池中Zn作负极,则MnO 2 作正极得电子。其电极反应式应为MnO 2 +H 2 O+e - MnOOH+OH - 或2MnO 2 +H 2 O+2e - Mn 2 O 3 +2OH - 。
(4)碱性锌锰干电池中Zn作负极,则MnO 2 作正极得电子。其电极反应式应为MnO 2 +H 2 O+e - MnOOH+OH - 或2MnO 2 +H 2 O+2e - Mn 2 O 3 +2OH - 。
![]() (5)从碱性锌锰干电池的原料可知,其废旧电池可回收利用的物质为锌和MnO 2 。
(5)从碱性锌锰干电池的原料可知,其废旧电池可回收利用的物质为锌和MnO 2 。
实验室提供如图所示的仪器(发生装置所选仪器不得重复使用)(1)欲利用上述仪器完成高锰酸钾制取氧气的 2020-04-08 …
某学生利用高锰酸钾分解制氧气的反应,测量氧气的相对分子质量.实验步骤如下:①取适量高锰酸钾,放入干 2020-05-12 …
【高二化学】高锰酸钾酸性溶液与有机物的选择题》》》》》利用高锰酸钾酸性溶液可以( )(A)除去H 2020-05-16 …
为了比较下列四种蔬菜中维生素C的含量,某同学利用高锰酸钾进行了实验(维生素C的水溶液能够使高锰酸钾 2020-06-27 …
过氧化氢(H2O2)溶液在二氧化锰作催化剂的条件下能迅速分解产生水和氧气(如图所示).分液漏斗可以 2020-07-08 …
I.利用含锰废水(主要含Mn2+、SO、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸 2020-11-02 …
如图是利用高锰酸钾制取氧气的装置图:(1)写出高锰酸钾制取氧气的符号表达式:(2)该实验中有一处不足 2020-11-10 …
课堂上同学们利用高锰酸钾制取氧气,将带火星的木条伸入试管内检验,带火星的木条复燃;但用甲装置做过氧化 2020-11-29 …
(2014•哈尔滨)实验室现有高锰酸钾、二氧化锰、稀盐酸、用石蕊试液染成紫色的湿润纸花、火柴、棉花及 2020-12-02 …
实验室现有下列仪器和药品.药品:氯酸钾、二氧化锰、锌粒、石灰石、稀硫酸和稀盐酸.仪器:如图所示.(1 2020-12-22 …