早教吧作业答案频道 -->化学-->
现有10%的Na2CO3溶液,请按照下面要求计算:(1)106g上述溶液中所含溶质的质量为g.(2)106g上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?(3)向106g上述溶液中逐滴加入10%的盐
题目详情
现有10%的Na2CO3溶液,请按照下面要求计算:
(1)106g上述溶液中所含溶质的质量为___g.
(2)106g上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?
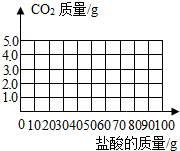
(3)向106g上述溶液中逐滴加入10%的盐酸并不断搅拌,此时发生的反应为:Na2CO3+HCl=NaHCO3+NaCl;当Na2CO3全部转化为NaHCO3后,再加入盐酸才开始放出CO2.请在图中画出产生气体的曲线.
(4)另取10% Na2CO3溶液边搅拌边加入10%的盐酸,有关反应物与生成物的量如表格:
则m=___,该反应的化学方程式为___.

(1)106g上述溶液中所含溶质的质量为___g.
(2)106g上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?
(3)向106g上述溶液中逐滴加入10%的盐酸并不断搅拌,此时发生的反应为:Na2CO3+HCl=NaHCO3+NaCl;当Na2CO3全部转化为NaHCO3后,再加入盐酸才开始放出CO2.请在图中画出产生气体的曲线.
(4)另取10% Na2CO3溶液边搅拌边加入10%的盐酸,有关反应物与生成物的量如表格:
| 物质 | Na2CO3 | HCl | x | NaCl | CO2 | H2O |
| 质量/g | 31.8 | 14.6 | 16.8 | 23.4 | 4.4 | m |
▼优质解答
答案和解析
(1)106g溶液中所含溶质的质量=106g×10%=10.6g,故填:10.6.
(2)设生成二氧化碳的质量为x,消耗的盐酸溶液中溶质的质量为a,则有
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
10.6g a x
=
x=4.4g
=
a=7.3g
答:最多生成二氧化碳的质量为4.4g.
(3)设全部转化为碳酸氢钠需要盐酸溶液中溶质的质量为y
Na2CO3+HCl=NaHCO3+NaCl
106 36.5
10.6g y
=
y=3.65g
盐酸溶液的质量为
=36.5g;
碳酸钠完全反应消耗盐酸的质量为:
=73g
故碳酸氢钠完全反应生成二氧化碳消耗盐酸的质量为73g-36.5g=36.5g,故曲线为: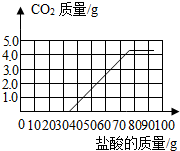
(4)根据表格提供的数据,生成4.4g二氧化碳,需要碳酸钠的质量是10.6g,生成氯化钠的质量是11.7g,说明给出的碳酸钠有一部分转化生成了碳酸氢钠和氯化钠,X为NaHCO3,碳酸钠和HCl是反应物,碳酸氢钠、氯化钠、二氧化碳和水是生成物,根据质量守恒定律可得31.6g+14.6g=16.8g+23.4g+4.4g+m,m=1.8g
设反应方程式为aNa2CO3+bHCl═cNaHCO3+dNaCl+eH2O+fCO2↑
a:b:c:d:e:f=
:
:
:
:
:
=0.3:0.4:0.2:0.4:0.1:0.1=3:4:2:4:1:1
方程式为3Na2CO3+4HCl═2NaHCO3+4NaCl+H2O+CO2↑
故填:1.8,3Na2CO3+4HCl═2NaHCO3+4NaCl+H2O+CO2↑.
(2)设生成二氧化碳的质量为x,消耗的盐酸溶液中溶质的质量为a,则有
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
10.6g a x
| 106 |
| 44 |
| 10.6g |
| x |
| 106 |
| 44 |
| 10.6g |
| a |
答:最多生成二氧化碳的质量为4.4g.
(3)设全部转化为碳酸氢钠需要盐酸溶液中溶质的质量为y
Na2CO3+HCl=NaHCO3+NaCl
106 36.5
10.6g y
| 106 |
| 36.5 |
| 10.6g |
| y |
盐酸溶液的质量为
| 3.65g |
| 10% |
碳酸钠完全反应消耗盐酸的质量为:
| 7.3g |
| 10% |
故碳酸氢钠完全反应生成二氧化碳消耗盐酸的质量为73g-36.5g=36.5g,故曲线为:

(4)根据表格提供的数据,生成4.4g二氧化碳,需要碳酸钠的质量是10.6g,生成氯化钠的质量是11.7g,说明给出的碳酸钠有一部分转化生成了碳酸氢钠和氯化钠,X为NaHCO3,碳酸钠和HCl是反应物,碳酸氢钠、氯化钠、二氧化碳和水是生成物,根据质量守恒定律可得31.6g+14.6g=16.8g+23.4g+4.4g+m,m=1.8g
设反应方程式为aNa2CO3+bHCl═cNaHCO3+dNaCl+eH2O+fCO2↑
a:b:c:d:e:f=
| 31.6g |
| 106 |
| 14.6g |
| 36.5 |
| 16.8g |
| 84 |
| 23.4g |
| 58.5 |
| 1.8g |
| 18 |
| 4.4g |
| 44 |
方程式为3Na2CO3+4HCl═2NaHCO3+4NaCl+H2O+CO2↑
故填:1.8,3Na2CO3+4HCl═2NaHCO3+4NaCl+H2O+CO2↑.
看了 现有10%的Na2CO3溶液...的网友还看了以下:
一个物体质量为200g以初速度20m/s竖直上抛,上升最大高度16m,一个物体质量为200g以初速度 2020-03-30 …
已知1/3≤a≤1,若函数f(x)=ax^2-2x+1,在区间[1,3]上的最大值为M(a),最小 2020-04-05 …
已知1/3≤a≤1若函数f(x)=ax²-2x+1在区间[1,3]上的最大值为Ma最小值为Na令g 2020-05-16 …
化学反应中的热量应用1.2A(l)+B(l)=2C(g);△H=+Q12.2A(g)+B(g)=2 2020-06-04 …
已知函数f(x)=2x^2-2ax+3在[-1,1]上有最小值,记作g(a)求g(a)的最大值以前 2020-06-07 …
反应N2(g)+3H2(g)2NH3(g)△H<0在某一时间段中反应速率与反应过程的曲线关系如图, 2020-07-03 …
f(x)=1/3x^3-x-1.f(x)在t≤x≤t+3上最大值为M(t),最小值为m(t)记g( 2020-07-13 …
某超市出售的三种品牌食品袋上,分别标有质量为(500±5)g,(500±10)g,(500±20)g 2020-11-07 …
(2012•宜宾)已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见金属 2020-11-12 …
消毒鲜牛奶上标有“净重(500±5)g”,其中500g表示标准质量,+5g表示符合要求的牛奶质量最多 2020-12-02 …