现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸。检验CuO经氢气还原所得到红色产物中是否含有碱性氧化物Cu2O的试剂是,反应的离子方程式
现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl 3 稀溶液及pH试纸。检验CuO经氢气还原所得到红色产物中是否含有碱性氧化物Cu 2 O的试剂是 ,反应的离子方程式 。
Ⅲ.实验室有黄铜(铜和锌两种金属的混合物)粉末。课外化学兴趣小组欲利用给出的实验仪器及试剂,测定该样品中锌的质量分数。除托盘天平必用外,供选择的实验装置如下图所示:
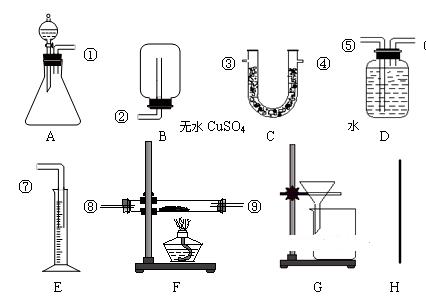
实验中可测得的数据:
黄铜的质量 a g ; 充分反应后在标况下生成氢气的体积为 b L
反应前仪器和药品的质量为 c g ;充分反应后剩余固体的质量为 d g
充分反应后仪器和药品的质量为 e g
(1)实验中可供选择的药品除样品外,还有:①足量的浓硫酸、②足量的稀硫酸、③氧化铜。你认为一定要用到的药品是 (填序号)。
(2)甲同学实验中使用了A、D、E三种装置,组装时接口编号的连接顺序为 ,(填序号)写出合金中锌的质量分数的计算式 。
(3)乙同学实验中测得的数据为:黄铜的质量 a g;充分反应后剩余固体的质量为 d g。他在实验中使用了上图中 装置(填符号)。
离心泵使用一段时间之后(比如一年)产生了气缚现象,试分析其原因 2020-05-20 …
炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便出现红棕色锈斑(该锈斑为Fe(OH)3失水的产 2020-06-30 …
如何利用和避免离心现象.知道什么是离心运动以及产生离心运动的条件如何利用和避免离心现象?什么是离心 2020-08-03 …
数学题,(速度)某制药公司有三条生产线生产中成药产品.公司进行产品结构调整,决定用现有产品生产线的剩 2020-11-05 …
如图装置中,试管①②③里已分别盛有相应药品,向该装置中缓缓通入二氧化碳气体,经过一段时间后关闭止水夹 2020-11-07 …
线性规划:某制药公司有三条生产线生产中成药产品.公司进行产品结构调整某制药公司有三条生产线生产中成药 2020-12-01 …
某制药公司有三条生产线生产中成药产品,公司进行产品结构调整,决定用现有产品生产线的剩余生产能力试生产 2020-12-03 …
某村的一块试验田,去年种植普通水稻,今年该试验田的1/3种上超级水稻,收割时发现该试验田的水稻总产量 2020-12-05 …
某村的一块试验田,去年种植普通水稻,今年该试验田的三分之种上超级水稻,收割时发现该试验田的水稻总量是 2020-12-16 …
下列关于离心现象的说法正确的是()A.当物体所受的离心力大于向心力时产生离心现象B.做匀速圆周运动的 2021-01-13 …