早教吧作业答案频道 -->化学-->
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素的原子最外层电子排布式可表示如下:asa、bsbbpb、csccp2c。甲是一种溶解度较小的化合物,却可溶于乙
题目详情
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素的原子最外层电子排布式可表示如下:as a 、bs b bp b 、cs c cp 2c 。甲是一种溶解度较小的化合物,却可溶于乙的水溶液。由此可知甲、乙的化学式分别是_______、_______;甲溶于乙的水溶液的化学方程式为____________________。
(2)已知112号元素是用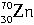 高能原子轰击
高能原子轰击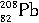 的靶子,使锌核与铅核熔合而得。科学家通过该放射性元素的一系列衰变产物确定了它的存在。
的靶子,使锌核与铅核熔合而得。科学家通过该放射性元素的一系列衰变产物确定了它的存在。
①112号是第几周期第几族元素?
②它是金属还是非金属?
③你认为它的最高氧化态至少可以达到多少?
(2)已知112号元素是用
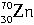 高能原子轰击
高能原子轰击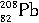 的靶子,使锌核与铅核熔合而得。科学家通过该放射性元素的一系列衰变产物确定了它的存在。
的靶子,使锌核与铅核熔合而得。科学家通过该放射性元素的一系列衰变产物确定了它的存在。①112号是第几周期第几族元素?
②它是金属还是非金属?
③你认为它的最高氧化态至少可以达到多少?
▼优质解答
答案和解析
见解析
【试题分析】
(1)由于s轨道上最多只能容纳2个电子,所以as a 可能为1s 1 ,也可能为2s 2 ,即此元素可能为氢,也可能为铍。bs b bp b 中,由于p轨道上进入电子,所以能量较低的s轨道上必充满电子,而s轨道上最多只能容纳2个电子,所以b=2,故此元素的价电子排布式为2s 2 2p 2 ,它为碳。与前一种元素的推断方法相同,cs c cp 2c 中的c=2,从而得出该元素的价电子排布式为2s 2 2p 4 ,它为氧。
通过上面的分析,我们可以得出,甲、乙两种物质分别为BeCO 3 和H 2 CO 3 。反应的化学方程式为BeCO 3 +H2CO 3 =Be(HCO 3 ) 2 。
(2)①我们可以利用核外电子排布的三个原则,写出电子进入轨道的顺序,从而确定112号元素在元素周期表中的位置;也可利用各周期容纳元素的数目及元素周期表的结构,推测出112号元素在元素周期表中的位置。通过比较不难发现,用后一种方法更简单。前七周期的元素种类为:2+8+8+18+18+32+32=118,利用元素周期表的结构倒推可得112号元素位于第7周期ⅡB族。
②按金属与非金属的分界线划分,第7周期只有0族元素为非金属元素,其余都为金属元素,因此112号元素为金属元素。
③由于112号元素的价电子排布式为6d 10 7s 2 ,所以在一般情况下,其最高氧化态至少可以达到+2价。
【试题分析】
(1)由于s轨道上最多只能容纳2个电子,所以as a 可能为1s 1 ,也可能为2s 2 ,即此元素可能为氢,也可能为铍。bs b bp b 中,由于p轨道上进入电子,所以能量较低的s轨道上必充满电子,而s轨道上最多只能容纳2个电子,所以b=2,故此元素的价电子排布式为2s 2 2p 2 ,它为碳。与前一种元素的推断方法相同,cs c cp 2c 中的c=2,从而得出该元素的价电子排布式为2s 2 2p 4 ,它为氧。
通过上面的分析,我们可以得出,甲、乙两种物质分别为BeCO 3 和H 2 CO 3 。反应的化学方程式为BeCO 3 +H2CO 3 =Be(HCO 3 ) 2 。
(2)①我们可以利用核外电子排布的三个原则,写出电子进入轨道的顺序,从而确定112号元素在元素周期表中的位置;也可利用各周期容纳元素的数目及元素周期表的结构,推测出112号元素在元素周期表中的位置。通过比较不难发现,用后一种方法更简单。前七周期的元素种类为:2+8+8+18+18+32+32=118,利用元素周期表的结构倒推可得112号元素位于第7周期ⅡB族。
②按金属与非金属的分界线划分,第7周期只有0族元素为非金属元素,其余都为金属元素,因此112号元素为金属元素。
③由于112号元素的价电子排布式为6d 10 7s 2 ,所以在一般情况下,其最高氧化态至少可以达到+2价。
看了 (1)无机化合物甲、乙分别由...的网友还看了以下:
五种短周期元素的部分性质数据如下:元素TXYZW原子半径(nm)0.0370.0750.0990. 2020-04-08 …
下面四个命题正确的有几个:(1)集合N中最小的数是1:;(2)若-a不属于N,则a属于N;(3)若 2020-05-15 …
一,用描述法表示下列集合(1)被3除余2的正整数集合一,用描述法表示下列集合(1)被3除余2的正整 2020-06-14 …
已知七种短周期元素a~g的有关信息如下表所示:元素编号abcdefg原子半径/nm0.0370.0 2020-07-18 …
读图,完成小题。小题1:最适合上图的图名为()A.区域整体性示意图B.自然地理环境整体性示意图C. 2020-07-31 …
对某芳香烃A分析结果如下:质谱图显示其最大质荷比为120,红外光谱显示其有两个甲基,核磁共振氢谱显示 2020-11-11 …
(2010•徐州)某校地理兴趣小组运用一“等高线地形图”(如图1所示)进行野外考察,结合图1、图2, 2020-11-11 …
1、某工厂生产的产品在质量和长度上都合格时,该产品才合格.若用A表示...1、某工厂生产的产品在质量 2020-11-16 …
一、在1,-1,-2这三个数中,任意两数之差的最小值是二、(1)如果|x-1|=2,求X,并观察数轴 2020-11-18 …
1.集合P={x|x=2n-1,n∈N*,n≤10}的含有三个元素的全体子集的所有元素之和为多少?2 2020-12-07 …