早教吧作业答案频道 -->化学-->
锂元素被誉为“能源元素”.锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用.Ⅰ锂的原子结构示意图为;锂暴露在湿空气中时,会迅速地
题目详情
锂元素被誉为“能源元素”.锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用.
Ⅰ锂的原子结构示意图为___;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式___.
Ⅱ下面是从锂辉石(Li2O•Al2O3•SiO2)中提出锂的工业流程示意图.
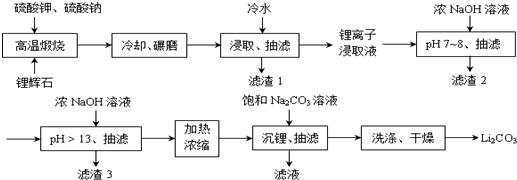
①高温煅烧时的反应原理为:
Li2O•Al2O3•SiO2+K2SO4═K2O•Al2O3•SiO2+Li2SO4
Li2O•Al2O3•SiO2+Na2SO4═Na2O•Al2O3•SiO2+Li2SO4
②锂离子浸取液中含有的金属离子为:K+、Na+、Li+、Fe3+、Fe2+、Al3+、Mn2+.
③几种金属离子沉淀完全的pH
④Li2SO4、Li2CO3在不同温度下的溶解度(g/100g水)
(1)浸取时使用冷水的原因是___.
(2)滤渣2的主要成分为___.
(3)流程中分2次调节pH(pH7~8和pH>13),有研究者尝试只加一次浓NaOH溶液使pH>13,结果发现在加饱和碳酸钠溶液沉锂后,随着放置时间延长,白色沉淀增加,最后得到的Li2CO3产品中杂质增多.Li2CO3产品中的杂质可能是___,用离子方程式表示其产生的原因___.
(4)加热浓缩的作用是___.
(5)洗涤Li2CO3晶体使用___.
Ⅰ锂的原子结构示意图为___;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式___.
Ⅱ下面是从锂辉石(Li2O•Al2O3•SiO2)中提出锂的工业流程示意图.

①高温煅烧时的反应原理为:
Li2O•Al2O3•SiO2+K2SO4═K2O•Al2O3•SiO2+Li2SO4
Li2O•Al2O3•SiO2+Na2SO4═Na2O•Al2O3•SiO2+Li2SO4
②锂离子浸取液中含有的金属离子为:K+、Na+、Li+、Fe3+、Fe2+、Al3+、Mn2+.
③几种金属离子沉淀完全的pH
| 金属离子 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 沉淀完全的pH | 4.7 | 9.0 | 3.2 | 10.1 |
| 温度 溶解度 | 10℃ | 20℃ | 50℃ | 80℃ |
| Li2SO4 | 35.4 | 34.7 | 33.1 | 31.7 |
| Li2CO3 | 1.43 | 1.33 | 1.08 | 0.85 |
(2)滤渣2的主要成分为___.
(3)流程中分2次调节pH(pH7~8和pH>13),有研究者尝试只加一次浓NaOH溶液使pH>13,结果发现在加饱和碳酸钠溶液沉锂后,随着放置时间延长,白色沉淀增加,最后得到的Li2CO3产品中杂质增多.Li2CO3产品中的杂质可能是___,用离子方程式表示其产生的原因___.
(4)加热浓缩的作用是___.
(5)洗涤Li2CO3晶体使用___.
▼优质解答
答案和解析
I.锂的原子核外有2个电子层,各层电子数为2、1,原子结构示意图为: ,Li与氮气反应生成Li3N,反应方程式为:6Li+N2=2Li3N,
,Li与氮气反应生成Li3N,反应方程式为:6Li+N2=2Li3N,
故答案为: ;6Li+N2=2Li3N;
;6Li+N2=2Li3N;
Ⅱ.锂辉石(Li2O•Al2O3•4SiO2)煅烧后,冷却、研磨,有利于冷水的浸取,抽滤,得到滤渣为硅酸盐,结合锂离子浸取液中含有的金属离子、离子沉淀完全pH,可知加热NaOH浓溶液,调节溶液pH=7~8,Al3+、Fe3+转化为Al(OH)3、Fe(OH)3,抽滤后再加入NaOH浓溶液,调节溶液pH>13,应是将Mn2+转化为沉淀,抽滤后,加热浓缩,加入饱和碳酸钠溶液,由于Li2CO3的溶解度远小于Li2SO4,会析出Li2CO3,由于Li2CO3的溶解度随温度升高而减小,用热水洗涤可减少Li2CO3的损失,得到最终产物碳酸锂.
(1)Li2SO4的溶解度随温度升高而减少,用冷水浸取可以提高浸取率,故用冷水浸取,
故答案为:Li2SO4的溶解度随温度升高而减少,用冷水浸取可以提高浸取率;
(2)由上述分析可知,滤渣2为Al(OH)3、Fe(OH)3,
故答案为:Al(OH)3、Fe(OH)3;
(3)只加一次浓NaOH溶液使pH>13,会使溶液中Al3+转化为AlO2-,放置后,空气中二氧化碳与AlO2-、水反应生成Al(OH)3,Li2CO3产品中的杂质可能是Al(OH)3,相应的离子方程式为:Al3++4OH-=AlO2-+2H2O、2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,
故答案为:Al(OH)3;Al3++4OH-=AlO2-+2H2O;2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(4)Li2CO3的溶解度随温度升高而减小,加热浓缩,提高Li+ 浓度和溶液温度,使得Li2CO3容易析出,
故答案为:提高Li+浓度和溶液温度,使得Li2CO3容易析出;
(5)Li2CO3的溶解度随温度升高而减小,用热水洗涤可以减少碳酸锂的损耗,
故答案为:热水.
 ,Li与氮气反应生成Li3N,反应方程式为:6Li+N2=2Li3N,
,Li与氮气反应生成Li3N,反应方程式为:6Li+N2=2Li3N,故答案为:
 ;6Li+N2=2Li3N;
;6Li+N2=2Li3N;Ⅱ.锂辉石(Li2O•Al2O3•4SiO2)煅烧后,冷却、研磨,有利于冷水的浸取,抽滤,得到滤渣为硅酸盐,结合锂离子浸取液中含有的金属离子、离子沉淀完全pH,可知加热NaOH浓溶液,调节溶液pH=7~8,Al3+、Fe3+转化为Al(OH)3、Fe(OH)3,抽滤后再加入NaOH浓溶液,调节溶液pH>13,应是将Mn2+转化为沉淀,抽滤后,加热浓缩,加入饱和碳酸钠溶液,由于Li2CO3的溶解度远小于Li2SO4,会析出Li2CO3,由于Li2CO3的溶解度随温度升高而减小,用热水洗涤可减少Li2CO3的损失,得到最终产物碳酸锂.
(1)Li2SO4的溶解度随温度升高而减少,用冷水浸取可以提高浸取率,故用冷水浸取,
故答案为:Li2SO4的溶解度随温度升高而减少,用冷水浸取可以提高浸取率;
(2)由上述分析可知,滤渣2为Al(OH)3、Fe(OH)3,
故答案为:Al(OH)3、Fe(OH)3;
(3)只加一次浓NaOH溶液使pH>13,会使溶液中Al3+转化为AlO2-,放置后,空气中二氧化碳与AlO2-、水反应生成Al(OH)3,Li2CO3产品中的杂质可能是Al(OH)3,相应的离子方程式为:Al3++4OH-=AlO2-+2H2O、2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,
故答案为:Al(OH)3;Al3++4OH-=AlO2-+2H2O;2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(4)Li2CO3的溶解度随温度升高而减小,加热浓缩,提高Li+ 浓度和溶液温度,使得Li2CO3容易析出,
故答案为:提高Li+浓度和溶液温度,使得Li2CO3容易析出;
(5)Li2CO3的溶解度随温度升高而减小,用热水洗涤可以减少碳酸锂的损耗,
故答案为:热水.
看了 锂元素被誉为“能源元素”.锂...的网友还看了以下:
在60米赛跑中,甲冲过终点线时比乙领先10米,乙比丙领先20米,假如乙和丙的速度始终不变,那么当乙 2020-04-27 …
交通工具的速度是不是越快越好呢?为什么铁路大提速?磁悬浮列车有污染吗(噪音污染、电磁污染)? 2020-05-21 …
交通工具的速度是不是越快越好? 2020-05-21 …
公路上有相距54公里的两站A和B,还有C站位于A和B之间.现有两种交通工具,一种交通工具的速度是另 2020-06-14 …
有三个队到王师傅的库房去领劳动工具,甲队领工具需要10分钟,乙队领工具需要15分钟,丙队领工具需2 2020-06-27 …
如图所示,某同学利用玩具枪练习射击本领,空中用细线悬挂一个苹果,苹果离地高度为h,玩具枪的枪口与苹 2020-07-10 …
(2011年连云港市)传说孙悟空具有腾云驾雾的本领,一个筋斗能翻十万八千里(折合5.4×l04km 2020-07-11 …
传说孙悟空具有腾云驾雾的本领,一个筋斗能翻十万八千里(折合5.4×104km),我国高铁的安全运行 2020-07-11 …
甲乙丙三人进行400米跑比赛.当甲跑到300米时,比乙领先30米,比丙领先60米.假如乙的速度不变 2020-07-12 …
甲乙丙三人进行400米赛跑比赛.当甲跑到300米时,比乙领先30米,比丙领先60米.如乙的速度不变 2020-07-12 …