室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是()A.若Ⅰ代表HB,加入20mLNaOH后溶液中:c(B-)+c(HB)=0.05mol/LB.若V(NaOH)=20.00mL
室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )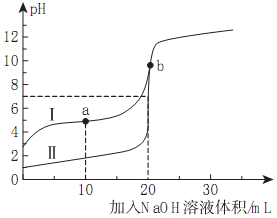
A. 若Ⅰ代表HB,加入20mLNaOH后溶液中:c(B-)+c(HB)=0.05mol/L
B. 若V(NaOH)=20.00mL时,NaB溶液呈碱性,NaA呈中性则HA是强酸
C. a点时的溶液中离子浓度最大的离子是Na+
D. 若Ⅱ代表HA的滴定曲线,则Ka(HB)≈10-5
B.若V(NaOH)=20.00mL时,与HA的体积、浓度相同,二者完全反应,NaA呈中性,可说明HA是强酸,故B正确;
C.a点时的溶液中溶质是等物质的量的NaB和HB,溶液显酸性,则c(Na+)
D.a点时的溶液中溶质是等物质的量的NaB和HB,则溶液中c(HB)≈c(B-),溶液的pH=5,c(H+)=10-5mol/L,Ka(HB)=
| c(H+)•c(B-) |
| c(HB) |
故选C.
如图所示,在一株发生向光弯曲生长的玉米幼苗上,a表示弯曲部位的向光侧细胞,b表示弯曲部位的背光侧细 2020-04-07 …
高中双曲线概念问题双曲线的标准方程是a²分之x²-b²分之y²=1(a>0,b>0)这是表示焦点在 2020-05-13 …
已知方程x^2/(1+k)+y^2/(1-k)=1表示双曲线,请你写出三个符合条件的双曲线标准方程 2020-05-13 …
对于曲线C:x2/4-k+y2/k-1,给出下面四个命题:1、曲线C不可能表示椭圆2、当1<k<4 2020-05-15 …
方程x24-t+y2t-2=1所表示的曲线为C,有下列命题:①若曲线C为椭圆,则2<t<4;②若曲 2020-05-15 …
设A是任意实数,则方程x^2*cosA+y^2=1所表示的曲线不可能是A.直线B双曲线C椭圆设A是 2020-06-02 …
下肢烧伤后,若膝关节后侧烧伤,膝关节应保持 ( )A.微屈5°~10°B.微屈10°~20°C.屈曲 2020-06-07 …
几道数学题(答对有赏)1.极坐标方程4Psin^2A/2=5表示的曲线是()A.圆.B.椭圆.C. 2020-06-26 …
|PF1|-|PF2|=2a什么时候表示双曲线.什么时候表示双曲线的右支.什么时候表示双曲线的一支 2020-07-20 …
参数方程x=t+1ty=t?1t表示的曲线是()A.椭圆B.双曲线C.抛物线D.参数方程x=t+1t 2021-01-22 …