早教吧作业答案频道 -->化学-->
某实验小组向100mLFeI2溶液中逐渐通入Cl2,会依次发生如下反应:①Cl2+2I-═2Cl-+I2②Cl2+2Fe2+═2Cl-+2Fe3+③5Cl2+I2+6H2O═10Cl-+2IO3-+12H+其中Fe3+,I2的物质的量随n(Cl2)的变化如图所示.请回答下列问
题目详情
某实验小组向100mL FeI2溶液中逐渐通入Cl2,会依次发生如下反应:
①Cl2+2I-═2Cl-+I2
②Cl2+2Fe2+═2Cl-+2Fe3+
③5Cl2+I2+6H2O═10Cl-+2IO3-+12H+
其中Fe3+,I2的物质的量随n(Cl2)的变化如图所示.
请回答下列问题:
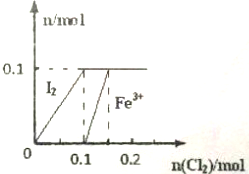
(1)当n(Cl2)=0.13mol时,不考虑水的电离及金属离子的水解,分析溶液中所含金属阳离子,以及其物质的量___(写出必要的计算过程,否则不得分).
(2)当溶液中n(Cl-):n(IO3-)=10:1时,通入的Cl2在标准状况下的体积为___L(写出必要的计算过程,否则不得分)
①Cl2+2I-═2Cl-+I2
②Cl2+2Fe2+═2Cl-+2Fe3+
③5Cl2+I2+6H2O═10Cl-+2IO3-+12H+
其中Fe3+,I2的物质的量随n(Cl2)的变化如图所示.
请回答下列问题:

(1)当n(Cl2)=0.13mol时,不考虑水的电离及金属离子的水解,分析溶液中所含金属阳离子,以及其物质的量___(写出必要的计算过程,否则不得分).
(2)当溶液中n(Cl-):n(IO3-)=10:1时,通入的Cl2在标准状况下的体积为___L(写出必要的计算过程,否则不得分)
▼优质解答
答案和解析
(1)根据图象,结合反应Cl2+FeI2=FeCl2+I2 知,当通入0.1molCl2时碘离子完全被氧化生成碘单质,碘化亚铁的物质的量是0.1mol,
剩余的0.03molCl2与Fe2+反应生成Fe3+,由Cl2+2Fe2+═2Cl-+2Fe3+可知0.03molCl2消耗0.06molFe2+,生成0.06molFe3+,则溶液中剩余0.04molFe2+,
故答案为:0.04molFe2+,0.06molFe3+;
(2)当溶液中n(Cl-):n(IO3-)=10:1时,碘离子转化为碘酸根离子时,Fe2+全部被氧化为Fe3+,由(1)可知碘化亚铁的物质的量是0.1mol,
设碘酸根的物质的量是x,则氯离子的物质的量是10x,根据氧化还原反应中得失电子数相等得x×6+(0.2-x)×1+0.1×1=10x×1,x=0.06,所以溶液中碘酸根的物质的量是0.06mol,氯离子的物质的量是0.6mol,根据Cl2~2Cl-知,氯气的物质的量是0.3mol,氯气的体积=0.3mol×22.4L/mol=6.72L,
故答案为:6.72.
剩余的0.03molCl2与Fe2+反应生成Fe3+,由Cl2+2Fe2+═2Cl-+2Fe3+可知0.03molCl2消耗0.06molFe2+,生成0.06molFe3+,则溶液中剩余0.04molFe2+,
故答案为:0.04molFe2+,0.06molFe3+;
(2)当溶液中n(Cl-):n(IO3-)=10:1时,碘离子转化为碘酸根离子时,Fe2+全部被氧化为Fe3+,由(1)可知碘化亚铁的物质的量是0.1mol,
设碘酸根的物质的量是x,则氯离子的物质的量是10x,根据氧化还原反应中得失电子数相等得x×6+(0.2-x)×1+0.1×1=10x×1,x=0.06,所以溶液中碘酸根的物质的量是0.06mol,氯离子的物质的量是0.6mol,根据Cl2~2Cl-知,氯气的物质的量是0.3mol,氯气的体积=0.3mol×22.4L/mol=6.72L,
故答案为:6.72.
看了 某实验小组向100mLFeI...的网友还看了以下:
请问下这个公式是什么意思=ROUNDDOWN(IF(Q27>R27,Q27/0.5,Q27*2), 2020-04-06 …
根据要求作图(1)人眼看到斜插入水中的筷子发生弯折(如图1),请在图2中法线两侧画出能正确说明产生 2020-05-13 …
已知数列,中,对任何正整数n都有:+…+.(1)若数列是首项为1和公比为2的等比数列,求数列的通项 2020-05-14 …
一)单选题1.标题《XX公司关于铺张浪费问题的请示》是正确的.(A)对(B)错2.公文的作者与阅者 2020-06-13 …
在通假字下面画线,并写出与之相通的本字。1.君不如肉袒伏斧质请罪2.秦王以十五城请易寡人之璧,可予 2020-06-29 …
(1)如图所示,磁体N极与通电螺线管的A端相互吸引,请标出通电螺线管的N极、S极和导线中的电流方向 2020-07-04 …
bn+1=2bn²-bn+1/2求通项!我要的是方法!公式!已知f(x)=x²-1/2x+1/4若 2020-07-09 …
英语翻译1(代表);2(邀请您出席于11月2日周二上午9点在山东国际交流中心召开的美国文化论坛.) 2020-07-24 …
请问这个微分方程组是怎么通过转化成极坐标而得到如下答案的,dx/dt=ux-wy-x(x^2+y^ 2020-07-31 …
(1)如图(1)所示,请画出静止在水平面上的西瓜所受到的力.(2)如图(2)所示,请画出物体AB在平 2020-10-29 …