早教吧作业答案频道 -->化学-->
甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)⇌HCOOH(l)+CH3OH(l);△H>0某小组通过试验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始量如表:组分HC
题目详情
甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)⇌HCOOH(l)+CH3OH(l);△H>0
某小组通过试验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始量如表:
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如图:
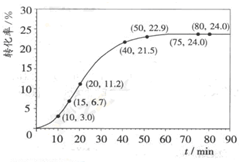
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
请计算15-20min范围内甲酸甲酯的减少量为___mol,甲酸甲酯的平均反应速率为___mol•min-1.
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因:___.
(3)上述反应的平衡常数表达式为:K=
,则该反应在温度T1下的K值为___.
某小组通过试验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始量如表:
| 组分 | HCOOCH3 | H2O | HCOOH | CH3OH |
| 物质的量/mol | 1.00 | 1.99 | 0.01 | 0.52 |

(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
| 反应时间范围/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均反应速率/(10-3mol•min-1) | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因:___.
(3)上述反应的平衡常数表达式为:K=
| c(HCOOH)•c(CH3OH) |
| c(HCOOCH3)•c(H2O) |
▼优质解答
答案和解析
(1)15min时,甲酸甲酯的转化率为6.7%,所以15min时,甲酸甲酯的物质的量为1-1.00mol×6.7%=0.933mol;20min时,甲酸甲酯的转化率为11.2%所以20min时,甲酸甲酯的物质的量为1-1.00mol×11.2%=0.888mol,所以15至20min甲酸甲酯的减少量为0.933mol-0.888mol=0.045mol,则甲酸甲酯的平均速率=0.045mol/5min=0.009mol•min-1.
故答案为:0.045mol;0.009;
(2)从题给数据不难看出,平均速率的变化随转化率的增大先增大再减小,后保持不变.因为反应开始甲酸甲酯的浓度大,所以反应速率较大,后随着反应进行甲酸甲酯的浓度减小,反应速率减小,当达到平衡时,反应速率几乎不变.
故答案为:①反应初期:虽然甲酸甲酯的量较大,但甲酸量很小,催化效果不明显,反应速率较慢.
②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
(3)由图象与表格可知,在75min时达到平衡,甲酸甲酯的转化率为24%,所以甲酸甲酯转化的物质的量为1.00×24%=0.24mol,结合方程式可计算得平衡时,甲酸甲酯物质的量=0.76mol,水的物质的量1.75mol,甲酸的物质的量=0.25mol,甲醇的物质的量=0.76mol.所以K=(0.76×0.25)/(1.75×0.76)=
,
故答案为:
.
故答案为:0.045mol;0.009;
(2)从题给数据不难看出,平均速率的变化随转化率的增大先增大再减小,后保持不变.因为反应开始甲酸甲酯的浓度大,所以反应速率较大,后随着反应进行甲酸甲酯的浓度减小,反应速率减小,当达到平衡时,反应速率几乎不变.
故答案为:①反应初期:虽然甲酸甲酯的量较大,但甲酸量很小,催化效果不明显,反应速率较慢.
②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
(3)由图象与表格可知,在75min时达到平衡,甲酸甲酯的转化率为24%,所以甲酸甲酯转化的物质的量为1.00×24%=0.24mol,结合方程式可计算得平衡时,甲酸甲酯物质的量=0.76mol,水的物质的量1.75mol,甲酸的物质的量=0.25mol,甲醇的物质的量=0.76mol.所以K=(0.76×0.25)/(1.75×0.76)=
| 1 |
| 7 |
故答案为:
| 1 |
| 7 |
看了 甲酸甲酯水解反应方程式为:H...的网友还看了以下:
异口同声等左边谜面右边谜底异口同声一孔之见不寒而栗以身作则四面楚歌不能自拔坐井观天手足无措包罗万象 2020-06-22 …
如图所示,为质量--体积图象,请根据图象回答下列问题:(1)甲物质的密度ρ甲为多少?(2)甲物质的 2020-07-20 …
下列词语中,加点的字的读音完全相同的一项是:()A.累积连累连篇累牍果实累累B.模特模具模棱两可劳动 2020-11-03 …
下列各项中,每对词语加横线字读音完全不同的一组是()A.露面/露马脚犄角/掎角之势亟待解决/亟来问讯 2020-11-26 …
下列词语中加粗字的读音完全相同的一组是A.量入为出量体裁衣再三思量量力而行B.处女作处变不惊处心积虑 2020-12-09 …
下列词语中,加点的字的读音完全相同的一项是:A.累积连累连篇累牍果实累累B.模特模具模棱两可劳动模范 2020-12-14 …
苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备原理是:C6H5C2H5(g)⇌C6H 2020-12-25 …
(14分)向某密闭容器中加入0.6molA、0.2molC和一定量的B三种气体,一定条件下发生反应, 2020-12-25 …
化学反应方向:为反应体系提供能量为反应体系提供能量是什么意思?举些例子.同时,它与给定温度、压强、催 2020-12-25 …
苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:C8H10(g)(乙苯)⇌C8H8(g)( 2020-12-25 …