早教吧作业答案频道 -->化学-->
由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图1转化关系(部分生成物和反应条件已略去).(1)若A为金属钠,则E为,A与水反应的离子方程式为.(2)若A为过
题目详情
由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图1转化关系(部分生成物和反应条件已略去).
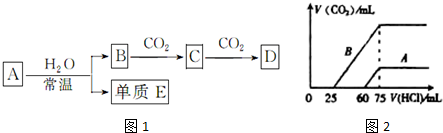
(1)若A为金属钠,则E为___,A与水反应的离子方程式为___.
(2)若A为过氧化钠,则E为___,A与水反应的化学方程式为___.
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是___,
(4)向10ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图2示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为___;原NaOH溶液的物质的量浓度为___;由曲线A、B可知,两次实验通入的CO2的体积比为___.

(1)若A为金属钠,则E为___,A与水反应的离子方程式为___.
(2)若A为过氧化钠,则E为___,A与水反应的化学方程式为___.
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是___,
(4)向10ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图2示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为___;原NaOH溶液的物质的量浓度为___;由曲线A、B可知,两次实验通入的CO2的体积比为___.
▼优质解答
答案和解析
(1)若A为金属钠,A与水反应生成单质E为H2,则B为NaOH,C为Na2CO3,D为NaHCO3,A与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,
故答案为:H2;2Na+2H2O=2Na++2OH-+H2↑;
(2)若A为过氧化钠,A与水反应生成单质E为O2,则B为NaOH,C为Na2CO3,D为NaHCO3,A与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,
故答案为:O2;2Na2O2+2H2O═4NaOH+O2↑;
(3)根据(1)(2)的分析可知,D为NaHCO3,
故答案为:NaHCO3;
(4)生成气体发生反应为:HCO3-+H+=H2O+CO2↑,假设溶液中溶质只有Na2CO3,开始没有气体生成时发生的反应为:H++CO32-=HCO3-,前后两过程消耗HCl的体积相等,而A曲线中实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3,B曲线中,前后消耗盐酸的体积之比为1:3,则曲线B表明M中溶质为Na2CO3、NaHCO3,且二者物质的量之比为1:2,
当加入75mL盐酸时,溶液中溶质为NaCl,根据钠离子、氯离子守恒可知n(NaOH)=n(NaCl)=n(HCl)=0.1mol/L×0.075L=0.0075mol,所以氢氧化钠的物质的量浓度为
=0.55mol/L,
曲线A生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线B生成二氧化碳消耗盐酸体积为(75-25)mL=50mL,由HCO3-+H+=H2O+CO2↑可知,则两次实验通入的CO2的体积之比=15mL:50mL=3:10,
故答案为:Na2CO3、NaHCO3;0.75mol/L;3:10.
故答案为:H2;2Na+2H2O=2Na++2OH-+H2↑;
(2)若A为过氧化钠,A与水反应生成单质E为O2,则B为NaOH,C为Na2CO3,D为NaHCO3,A与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,
故答案为:O2;2Na2O2+2H2O═4NaOH+O2↑;
(3)根据(1)(2)的分析可知,D为NaHCO3,
故答案为:NaHCO3;
(4)生成气体发生反应为:HCO3-+H+=H2O+CO2↑,假设溶液中溶质只有Na2CO3,开始没有气体生成时发生的反应为:H++CO32-=HCO3-,前后两过程消耗HCl的体积相等,而A曲线中实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3,B曲线中,前后消耗盐酸的体积之比为1:3,则曲线B表明M中溶质为Na2CO3、NaHCO3,且二者物质的量之比为1:2,
当加入75mL盐酸时,溶液中溶质为NaCl,根据钠离子、氯离子守恒可知n(NaOH)=n(NaCl)=n(HCl)=0.1mol/L×0.075L=0.0075mol,所以氢氧化钠的物质的量浓度为
| 0.0075mol |
| 0.01L |
曲线A生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线B生成二氧化碳消耗盐酸体积为(75-25)mL=50mL,由HCO3-+H+=H2O+CO2↑可知,则两次实验通入的CO2的体积之比=15mL:50mL=3:10,
故答案为:Na2CO3、NaHCO3;0.75mol/L;3:10.
看了 由短周期元素组成的中学常见的...的网友还看了以下:
在等边三角形ABC中,D为线段BC上的动点,连接AD,在角ADC内作角ADE等于60度,交AC边于 2020-05-13 …
如图是人体内某化学反应的图解,其中英文字母代表物质,数字表示反应前、中、后过程,请根据图回答:(1 2020-05-17 …
△ABC中,D为BC上的一点,若BD:DC=2:3,则S△ABD:S△ABC=(),若AE是△AC 2020-06-06 …
初中几何题,要有详解△ABC中,D为BC边上一点,且DC=2BD,若∠ABC=45°,∠ADC=6 2020-06-14 …
在平面直角坐标系中,已知O(0,0)A(2,0),B(0,4),C(0,3),D为x轴上一点.若以 2020-06-14 …
如图,Rt△ABC中,∠ACB=90°,D是AB上的一点,过D作DE⊥AB交AC于点E,CE=DE 2020-06-17 …
⑴如图在三角形abc中.若ab为,三角形abc的角平分线,求证,三角形abd的面积比三角形acd的 2020-06-27 …
已知,在三角形ABC中,D为直线AC上一点,角ABC=角ACB=x度,角ADF=角AFD=y度,直 2020-07-21 …
如图,在三棱柱...接上,三棱柱ABC-A'B'C'中,D为BC上一点,且A'B平行于平面AC'D. 2020-11-03 …
中学常见的某反应的化学方程式为a+b→c+d+H2O(未配平,反应条件略去)。请回答下列问题:(1) 2021-02-18 …