早教吧作业答案频道 -->化学-->
亚硝酸钠广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂,它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似
题目详情
亚硝酸钠广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂,它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生被当食盐误食的事件.某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置,利用一氧化氮与过氧化钠反应制备亚硝酸钠.(夹持装置和A中加热装置已略,气密性已检验)
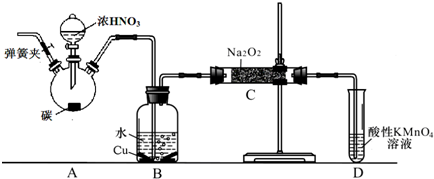
查阅资料:①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②NO2-能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO4-还原为Mn2+且无气体生成;
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸;
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2;
⑤AgNO2是一种难溶于水易溶于酸的白色化合物.
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1)___.
(2)D装置的作用是___.
(3)经检验C产物中亚硝酸钠含量较少.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠.为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是___(写名称).
(4)人体正常的血红蛋白中含Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是___.
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(5)能用来鉴别NaNO2和NaCl的方法是___.
A.测溶液pH法 B.加酸法 C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法 E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式___.

查阅资料:①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②NO2-能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO4-还原为Mn2+且无气体生成;
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸;
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2;
⑤AgNO2是一种难溶于水易溶于酸的白色化合物.
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1)___.
(2)D装置的作用是___.
(3)经检验C产物中亚硝酸钠含量较少.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠.为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是___(写名称).
(4)人体正常的血红蛋白中含Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是___.
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(5)能用来鉴别NaNO2和NaCl的方法是___.
A.测溶液pH法 B.加酸法 C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法 E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式___.
▼优质解答
答案和解析
根据题中实验装置及原理可知,装置A中碳与浓硝酸加热条件下反应生成二氧化氮和二氧化碳,装置B中铜、水与A中产生的二氧化氮反应生成一氧化氮,装置C中一氧化氮与过氧化钠反应制备亚硝酸钠,A中生成的二氧化碳也能与D中过氧化钠反应,所以在混合气体通入C装置前要除去二氧化碳,所以在B和C之间再加一个装有碱石灰的装置,未反应的一氧化氮会污染空气,所以用高锰酸钾溶液吸收,
(1)C中是用一氧化氮与过氧化钠反应制备亚硝酸钠,反应方程式为2NO+Na2O2═2NaNO2,
故答案为:2NO+Na2O2═2NaNO2;
(2)根据上面的分析可知,D装置的作用是除去未反应的NO,防止污染空气,
故答案为:除去未反应的NO,防止污染空气;
(3)根据上面的分析可知,E中盛放的试剂应是碱石灰,
故答案为:碱石灰;
(4)服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+,Fe元素化合价降低,被氧化,则维生素具有还原性,而亚硝酸盐,会导致Fe2+转化为Fe3+,说明亚硝酸盐具有氧化性,在反应中为氧化剂,被还原,所以维生素C是还原剂,
故答案为:A;
(5)A、亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,相同物质的量浓度的两种溶液的pH不同,所以可以用测定这两种溶液的pH值鉴别,故A能用来鉴别NaNO2和NaCl;
B、HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O,所以加酸后若有气泡产生的为NaNO2,没有气泡的是NaCl,故B能用来鉴别NaNO2和NaCl;
C、亚硝酸根离子不和银离子反应,氯离子和银离子反应生成不溶于硝酸的白色沉淀,反应现象不同,所以可以用AgNO3和HNO3两种试剂来区别,故C能用来鉴别NaNO2和NaCl;
D、在酸性条件下,亚硝酸钠和碘离子反应方程式为2NO2-+2I-+4H+=2NO↑+I2+2H2O,碘遇淀粉变蓝色,氯离子和碘离子不反应,所以反应现象不同,所以可以用酸性条件下的KI淀粉试液来区别,故D能用来鉴别NaNO2和NaCl,
故答案为:E;
(6)溴水加到NaNO2溶液观察到溴水褪色,说明溴水与NaNO2溶液发生氧化还原反应,根据元素守恒和电子得失守恒可知该反应的离子方程式为NO2-+Br2+H2O=NO3-+2Br-+2H+,
故答案为:NO2-+Br2+H2O=NO3-+2Br-+2H+.
(1)C中是用一氧化氮与过氧化钠反应制备亚硝酸钠,反应方程式为2NO+Na2O2═2NaNO2,
故答案为:2NO+Na2O2═2NaNO2;
(2)根据上面的分析可知,D装置的作用是除去未反应的NO,防止污染空气,
故答案为:除去未反应的NO,防止污染空气;
(3)根据上面的分析可知,E中盛放的试剂应是碱石灰,
故答案为:碱石灰;
(4)服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+,Fe元素化合价降低,被氧化,则维生素具有还原性,而亚硝酸盐,会导致Fe2+转化为Fe3+,说明亚硝酸盐具有氧化性,在反应中为氧化剂,被还原,所以维生素C是还原剂,
故答案为:A;
(5)A、亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,相同物质的量浓度的两种溶液的pH不同,所以可以用测定这两种溶液的pH值鉴别,故A能用来鉴别NaNO2和NaCl;
B、HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O,所以加酸后若有气泡产生的为NaNO2,没有气泡的是NaCl,故B能用来鉴别NaNO2和NaCl;
C、亚硝酸根离子不和银离子反应,氯离子和银离子反应生成不溶于硝酸的白色沉淀,反应现象不同,所以可以用AgNO3和HNO3两种试剂来区别,故C能用来鉴别NaNO2和NaCl;
D、在酸性条件下,亚硝酸钠和碘离子反应方程式为2NO2-+2I-+4H+=2NO↑+I2+2H2O,碘遇淀粉变蓝色,氯离子和碘离子不反应,所以反应现象不同,所以可以用酸性条件下的KI淀粉试液来区别,故D能用来鉴别NaNO2和NaCl,
故答案为:E;
(6)溴水加到NaNO2溶液观察到溴水褪色,说明溴水与NaNO2溶液发生氧化还原反应,根据元素守恒和电子得失守恒可知该反应的离子方程式为NO2-+Br2+H2O=NO3-+2Br-+2H+,
故答案为:NO2-+Br2+H2O=NO3-+2Br-+2H+.
看了 亚硝酸钠广泛用于印染、漂白等...的网友还看了以下:
①“千里之堤,溃于蚁穴”,此话不假。白蚁对江河堤坝可谓危害严重。2001年四川会理县大路沟水库因白 2020-04-07 …
用塑料瓶子装白酒到底有没有危害那天看电视说 用塑料瓶子装白酒.醋,开水等液体.容易产生致癌物质.( 2020-05-16 …
为什么要去除污水中的有机物,有机物有什么危害?我们吃的糖类蛋白质不都是有机物吗?这些物质好像没有危 2020-06-04 …
小文在做“开水煮白菜”这道菜的过程中,有以下分析,其中正确的是A.放一点盐,汤就有了咸味,说明分子 2020-06-27 …
下列有关“白色污染”的说法不正确的是A.白色污染主要是由白色材料的废弃物造成的B.白色污染仅影响环境 2020-11-05 …
①“千里之堤,溃于蚁穴”,此话不假。白蚁对江河堤坝可谓危害严重。2001年四川会理县大路沟水库因白蚁 2020-11-08 …
下列过程中发生了化学变化的是()A.干冰升华,形成白雾B.咸菜长期放置在空气中表面有一层“白霜”C. 2020-11-16 …
四个月前买的白糖,现在白糖湿润(也就是说吸水)了,这白糖还能吃吗?对身体健康有没有危害?最好说出能吃 2021-01-12 …
下面划线的句子有语病的一句是(3分)有人说,美女的人生充满了机会,而丑女的人生处处都有危机。A然而, 2021-01-12 …
宝宝大便发白有危险吗?胎便是什么颜色的? 2021-04-03 …