称取铁粉和氧化铜的混合物6.40g,进行如下实验:根据实验所得数据,下列说法正确的是()A.原混合物中铜元素的质量不一定为0.64gB.生成气体体积为2.016LC.实验中反应的硫酸的物质
称取铁粉和氧化铜的混合物6.40g,进行如下实验: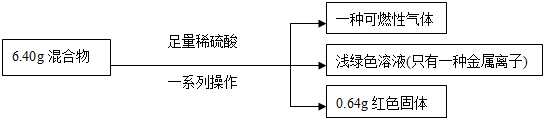
根据实验所得数据,下列说法正确的是( )
A. 原混合物中铜元素的质量不一定为0.64g
B. 生成气体体积为2.016L
C. 实验中反应的硫酸的物质的量为0.1mol
D. 原混合物中铁的质量分数为87.5%
生成0.64gCu,其物质的量:
| 0.64 |
| g64g/mol |
故混合物中:m(CuO)=0.01mol×80g/mol=0.8g,则:m(Fe)=6.40g-0.8g=5.6g,n(Fe)=
| 5.6g |
| 56g/mol |
A.根据分析可知,铜的质量为0.64g,故A错误;
B.设氢气的物质的量为nmol,根据电子转移守恒可得:2n+0.01mol×2=0.1mol×2,解得n=0.09mol,没有告诉在标准状况下,不能使用标准状况下气体摩尔体积计算氢气体积,故B错误;
C.铁的物质的量为0.1mol,反应生成溶质为硫酸亚铁,则反应消耗的硫酸的物质的量为0.1mol,故C正确;
D.由上述分析可知,Fe的质量为5.6g,混合物中Fe的质量分数为:
| 5.6g |
| 6.4g |
故选CD.
立体图形工地上放着两根质地相同的圆柱形木料,它们长度相等,甲的底面半径是乙的2倍,队长让技术员称一 2020-05-13 …
把一根铁钉放入到一定质量的硫酸铜溶液中,过一会儿称量,质量增重0、8克,则有多少克铁参加反应? 2020-05-17 …
有两根质量相同的铜棒和锌棒,用导线连接后插入硫酸铜溶液中,经过一段时间后,取出洗净并干燥后称量,铜 2020-06-27 …
工地上放着两根质地相同的圆柱形木料,甲底面半径是乙底面半径的2倍,一定长度是甲的2倍.队长让技术员 2020-07-31 …
有一个不等臂的杠杆,把一个物体放在左盘秤质量为m1,放在右盘秤称得质量为m2,问这个物体的真实质量 2020-08-01 …
用如下步骤测定Na2SO4•xH2O晶体中x的值:①称量质量为W1②称量质量为W2③称量质量为W3④ 2020-10-31 …
初三的物理报告、调查现实生活中称量质量的工具调查称量几吨或几十吨质量的工具是什么?称量几十千克甚至一 2020-11-05 …
(1)在质量守恒定律的实验探究活动中,某小组同学将一根用砂纸打磨干净的长镁条和一个石棉网一起放在托盘 2020-12-02 …
一袋香肠有10根,其中有9根质量相同,另有1根质量不足,轻一些.至少称几次能保证找出这根香肠来?用图 2020-12-20 …
称量前,当天平的指针不在零点而偏右时,用以称量物质,天平达到平衡时,称得的物质质量与实际需要称的质量 2021-01-02 …