早教吧作业答案频道 -->化学-->
化学反应过程中总是伴随着能量的变化,能量间可以相互转化.(l)己知:甲烷和一氧化碳的燃烧热(△H).分别为-890kJ•moL-1、-283kJ•moL-1.则CH4(g)+2CO2(g)═4CO(g)+2H2O(l)△H=kJ
题目详情
化学反应过程中总是伴随着能量的变化,能量间可以相互转化.
(l)己知:甲烷和一氧化碳的燃烧热(△H).分别为-890kJ•moL-1、-283kJ•moL-1.则CH4(g)+2CO2(g)═4CO(g)+2H2O(l)△H=___kJ•moL-1
(2)自然界发生的一个固氮反应是N2(g)+O2(g)⇌2NO(g),己知N2、O2、NO三种分子中化学键断裂所吸收的能里依次为946kJ•moL-1、498kJ•moL-1、632kJ•moL-1,则该反应的△H=___kJ•moL-1.
(3)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si粗
SiCl4
SiCl4纯
Si硅
在由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___.
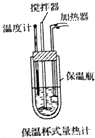
(4)在量热计(如图)中将100mL 0.50kJ•moL-1的CH3COOH溶液与100mL 0.55kJ•moL-1NaOH 溶液混合,温度从298.0K升高到300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J•K-1,溶液密度均为1g•mL-1,生成溶液的比热容c=4.184J•g-1•K-1(己知CH3COOH电离要吸热).
则实验测得CH3COOH的中和热△H=___.
(5)已知:
P4(g)+6Cl2(g)═4PCl3(g),△H=a kJ•moL-1,
P4(g)+10Cl2(g)═4PCl5(g),△H=b kJ•moL-1,
P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ•moL-1,PCl3中P-Cl键的键能为1.2kJ•moL-1,则Cl-Cl键的键能为___kJ•moL-1.
(l)己知:甲烷和一氧化碳的燃烧热(△H).分别为-890kJ•moL-1、-283kJ•moL-1.则CH4(g)+2CO2(g)═4CO(g)+2H2O(l)△H=___kJ•moL-1
(2)自然界发生的一个固氮反应是N2(g)+O2(g)⇌2NO(g),己知N2、O2、NO三种分子中化学键断裂所吸收的能里依次为946kJ•moL-1、498kJ•moL-1、632kJ•moL-1,则该反应的△H=___kJ•moL-1.
(3)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si粗
| Cl2 |
| |
| 460℃ |
| 蒸馏 |
| |
| H2 |
| |
| 1100℃ |
在由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___.
(4)在量热计(如图)中将100mL 0.50kJ•moL-1的CH3COOH溶液与100mL 0.55kJ•moL-1NaOH 溶液混合,温度从298.0K升高到300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J•K-1,溶液密度均为1g•mL-1,生成溶液的比热容c=4.184J•g-1•K-1(己知CH3COOH电离要吸热).
则实验测得CH3COOH的中和热△H=___.
(5)已知:
P4(g)+6Cl2(g)═4PCl3(g),△H=a kJ•moL-1,
P4(g)+10Cl2(g)═4PCl5(g),△H=b kJ•moL-1,
P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ•moL-1,PCl3中P-Cl键的键能为1.2kJ•moL-1,则Cl-Cl键的键能为___kJ•moL-1.

▼优质解答
答案和解析
(1)CH4和CO的燃烧热分别为809kJ/mol和283kJ/mol,其热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2 H2O(l)△H=-809kJ•mol-1
②CO(g)+
O2(g)=CO2(g)△H=-283kJ•mol-1
据盖斯定律,①-②×4得:CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)△H=+323kJ/mol,
故答案为:+323;
(2)N2(g)+O2(g)⇌2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ•mol-1、498kJ•mol-1、632kJ•mol-1,反应焓变△H=(946kJ•mol-1+498kJ•mol-1)-2×632kJ•mol-1=+180kJ/mol,
故答案为:+180;
(3)每生成1.12kg纯硅需吸收akJ热量,则生成1mol纯硅吸收的热量为
kJ=0.025akJ,所以该反应的热化学方程式为2H2(g)+SiCl4(g)
Si(s)+4HCl(g)△H=+0.025akJ•mol-1,
故答案为:2H2(g)+SiCl4(g)
Si(s)+4HCl(g)△H=+0.025akJ•mol-1;
(4)将100mL 0.50mol/L的CH3COOH溶液与100mL 0.55mol/L NaOH溶液混合,完全反应生成0.05mol水放出的热量为:Q=cm△T=[150.5J/K+4.184J/(g•K)×200mL×1g•mL-1]×(300.7-298.0)K=2665.71kJ,则生成1mol水放出的热量为:2665.71kJ×
=53314.2J≈5.33×104J=53.3 kJ,
所以CH3COOH的中和热△H=-53.3 kJ/mol,
故答案为:-53.3kJ/mol;
(5)已知:①P4(g)+6Cl2(g)=4PCl3(g)△H=a kJ∙mol-1;
②P4(g)+10Cl2(g)=4PCl5(g)△H=b kJ∙mol-1;
利用“盖斯定律”,(②-①)×
得:Cl2(g)+PCl3(g)=PCl5(g)△H=
kJ•mol-1,
由Cl2(g)+PCl3(g)=PCl5(g)△H=
kJ•mol-1 可得E(Cl-Cl)+3×1.2c-5c=
,
因此可得:E(Cl-Cl)=
kJ•mol-1=1.4c+0.25b-0.25akJ•mol-1,
故答案为:1.4c+0.25b-0.25a.
①CH4(g)+2O2(g)=CO2(g)+2 H2O(l)△H=-809kJ•mol-1
②CO(g)+
| 1 |
| 2 |
据盖斯定律,①-②×4得:CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)△H=+323kJ/mol,
故答案为:+323;
(2)N2(g)+O2(g)⇌2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ•mol-1、498kJ•mol-1、632kJ•mol-1,反应焓变△H=(946kJ•mol-1+498kJ•mol-1)-2×632kJ•mol-1=+180kJ/mol,
故答案为:+180;
(3)每生成1.12kg纯硅需吸收akJ热量,则生成1mol纯硅吸收的热量为
| 28a |
| 1.12×103 |
| ||
故答案为:2H2(g)+SiCl4(g)
| ||
(4)将100mL 0.50mol/L的CH3COOH溶液与100mL 0.55mol/L NaOH溶液混合,完全反应生成0.05mol水放出的热量为:Q=cm△T=[150.5J/K+4.184J/(g•K)×200mL×1g•mL-1]×(300.7-298.0)K=2665.71kJ,则生成1mol水放出的热量为:2665.71kJ×
| 1mol |
| 0.05mol |
所以CH3COOH的中和热△H=-53.3 kJ/mol,
故答案为:-53.3kJ/mol;
(5)已知:①P4(g)+6Cl2(g)=4PCl3(g)△H=a kJ∙mol-1;
②P4(g)+10Cl2(g)=4PCl5(g)△H=b kJ∙mol-1;
利用“盖斯定律”,(②-①)×
| 1 |
| 4 |
| b-a |
| 4 |
由Cl2(g)+PCl3(g)=PCl5(g)△H=
| b-a |
| 4 |
| b-a |
| 4 |
因此可得:E(Cl-Cl)=
| b-a+5.6c |
| 4 |
故答案为:1.4c+0.25b-0.25a.
看了 化学反应过程中总是伴随着能量...的网友还看了以下:
(2014•崇明县二模)在⊙O中,圆心O在坐标原点上,半径为210,点P的坐标为(4,个),那么点 2020-05-17 …
地铁车站的轨道往往建得高些.如图所示,列车从A到O的进站过程中,在平直轨道的A处关闭发动机,“冲” 2020-07-01 …
(4分)氢气和氧气反应生成1mol水蒸气放热241.8KJ,已知氢气中H-H键能为436kJ/mo 2020-07-19 …
在直角坐标系中,以O(0,0)为圆心,以5为半径画圆,则点A(-3,4)的位置在()A.⊙O内B. 2020-07-26 …
Ⅰ.氮元素可以形成多种化合物.回答以下问题:(1)基态氮原子的价电子排布图是.(2)C、N、O三种 2020-07-28 …
圆的有关概念:(1)圆两种定义方式:(a)在一个平面内线段OA绕它固定的一个端点O旋转一周,另一个 2020-07-31 …
在人类的ABO血型系统中,如果父亲的血型是O型,母亲的血型也是O型,则他们的子女可能出现的血型()A 2020-11-03 …
某人能接受A型血,不能给B型、O型的血液输血,他的血型是()A.A型B.B型C.O型D.AB型 2020-12-24 …
甲常说:“我是万能输血者.”乙却说:“我是万能受血者”.请你分析一下,甲、乙的血型分别是()A.A型 2020-12-24 …
(2002•南昌)如图,正三角形ABC的边长为6厘米,⊙O的半径为r厘米,当圆心O从点A出发,沿着线 2021-01-02 …