早教吧作业答案频道 -->化学-->
根据所给信息填空(1)用0.1mol/L的酸性高锰酸钾溶液测定FeSO4溶液的浓度时,因FeSO4溶液放置时间较长,导致测定结果(填“偏大”、“不变”或“偏小”)(2)过氧化钠的电子式(3)
题目详情
根据所给信息填空
(1)用0.1mol/L的酸性高锰酸钾溶液测定FeSO4溶液的浓度时,因FeSO4溶液放置时间较长,导致测定结果___(填“偏大”、“不变”或“偏小”)
(2)过氧化钠的电子式___
(3)选出下列说法中正确的___
①氧化物都能与酸或碱的溶液反应
②红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐
③由相同元素组成的物质一定是纯净物
④浓氨水滴加到FeCl3溶液中可制取Fe(OH)3胶体
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口
⑥用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
⑦金属Mg的活泼性比Al强,由Al2O3能与NaOH溶液反应推知MgO也能与NaOH溶液反应
⑧SiO2既能和NaOH溶液反应也能和氢氟酸反应,所以是两性氧化物
⑨3mol单质Fe在氧气中完全转变为Fe3O4,失去8NA个电子
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性
(4)浓硝酸久置变黄___
(5)明矾溶液与少量氢氧化钡溶液反应的离子方程式___.根据所给信息填空
(1)用0.1mol/L的酸性高锰酸钾溶液测定FeSO4溶液的浓度时,因FeSO4溶液放置时间较长,导致测定结果___(填“偏大”、“不变”或“偏小”)
(2)过氧化钠的电子式___
(3)选出下列说法中正确的___
①氧化物都能与酸或碱的溶液反应
②红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐
③由相同元素组成的物质一定是纯净物
④浓氨水滴加到FeCl3溶液中可制取Fe(OH)3胶体
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口
⑥用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
⑦金属Mg的活泼性比Al强,由Al2O3能与NaOH溶液反应推知MgO也能与NaOH溶液反应
⑧SiO2既能和NaOH溶液反应也能和氢氟酸反应,所以是两性氧化物
⑨3mol单质Fe在氧气中完全转变为Fe3O4,失去8NA个电子
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性
(4)浓硝酸久置变黄___
(5)明矾溶液与少量氢氧化钡溶液反应的离子方程式___.
44
33
23
2
34A
(1)用0.1mol/L的酸性高锰酸钾溶液测定FeSO4溶液的浓度时,因FeSO4溶液放置时间较长,导致测定结果___(填“偏大”、“不变”或“偏小”)
(2)过氧化钠的电子式___
(3)选出下列说法中正确的___
①氧化物都能与酸或碱的溶液反应
②红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐
③由相同元素组成的物质一定是纯净物
④浓氨水滴加到FeCl3溶液中可制取Fe(OH)3胶体
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口
⑥用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
⑦金属Mg的活泼性比Al强,由Al2O3能与NaOH溶液反应推知MgO也能与NaOH溶液反应
⑧SiO2既能和NaOH溶液反应也能和氢氟酸反应,所以是两性氧化物
⑨3mol单质Fe在氧气中完全转变为Fe3O4,失去8NA个电子
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性
(4)浓硝酸久置变黄___
(5)明矾溶液与少量氢氧化钡溶液反应的离子方程式___.根据所给信息填空
(1)用0.1mol/L的酸性高锰酸钾溶液测定FeSO4溶液的浓度时,因FeSO4溶液放置时间较长,导致测定结果___(填“偏大”、“不变”或“偏小”)
(2)过氧化钠的电子式___
(3)选出下列说法中正确的___
①氧化物都能与酸或碱的溶液反应
②红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐
③由相同元素组成的物质一定是纯净物
④浓氨水滴加到FeCl3溶液中可制取Fe(OH)3胶体
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口
⑥用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
⑦金属Mg的活泼性比Al强,由Al2O3能与NaOH溶液反应推知MgO也能与NaOH溶液反应
⑧SiO2既能和NaOH溶液反应也能和氢氟酸反应,所以是两性氧化物
⑨3mol单质Fe在氧气中完全转变为Fe3O4,失去8NA个电子
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性
(4)浓硝酸久置变黄___
(5)明矾溶液与少量氢氧化钡溶液反应的离子方程式___.
44
33
23
2
34A
▼优质解答
答案和解析
(1)FeSO44具有还原性,可被空气中氧气氧化,如在空气中防止,亚铁离子浓度减小,测定结果偏小,故答案为:偏小;
(2)过氧化钠为离子化合物,电子式为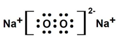 ,故答案为:
,故答案为: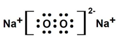 ;
;
(3)①CO等与酸或碱的溶液都不反应,为不成盐氧化物,故错误;
②玛瑙、水晶的主要成分为二氧化硅,钻石的主要成分为C,故错误;
③同素异形体由相同元素组成,可组成混合物,故错误;
④浓氨水滴加到FeCl33溶液中可制取Fe(OH)33沉淀,不能得到胶体,故错误;
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口,防止液体流出,故正确;
⑥焰色反应为元素的性质,不一定为盐溶液,故错误;
⑦MgO与NaOH溶液不反应,故错误;
⑧SiO22氢氟酸反应不生成盐,不是两性氧化物,故错误;
⑨3mol单质Fe在氧气中完全转变为Fe33O44,Fe的化合价变为+2、+3价,失去8NAA个电子,故正确;
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性,可防止食品被氧化,故正确.
故答案为:⑤⑨⑩;
(4)硝酸被稳定,易分解生成二氧化氮,反应的化学方程式为4HNO33=4NO22+O22+2H22O,故答案为:4HNO33=4NO22+O22+2H22O;
(5)明矾溶液与少量氢氧化钡溶液反应可生成氢氧化铝和硫酸钡沉淀,反应的离子方程式为2Al3+3++3SO442-2-+3Ba2+2++6OH--=2Al(OH) 33↓+3BaSO44↓,
故答案为:2Al3+3++3SO442-2-+3Ba2+2++6OH--=2Al(OH) 33↓+3BaSO44↓.
(2)过氧化钠为离子化合物,电子式为
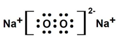 ,故答案为:
,故答案为: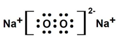 ;
;(3)①CO等与酸或碱的溶液都不反应,为不成盐氧化物,故错误;
②玛瑙、水晶的主要成分为二氧化硅,钻石的主要成分为C,故错误;
③同素异形体由相同元素组成,可组成混合物,故错误;
④浓氨水滴加到FeCl33溶液中可制取Fe(OH)33沉淀,不能得到胶体,故错误;
⑤向容量瓶中转移液体时,玻璃棒不可以接触到容量瓶的瓶口,防止液体流出,故正确;
⑥焰色反应为元素的性质,不一定为盐溶液,故错误;
⑦MgO与NaOH溶液不反应,故错误;
⑧SiO22氢氟酸反应不生成盐,不是两性氧化物,故错误;
⑨3mol单质Fe在氧气中完全转变为Fe33O44,Fe的化合价变为+2、+3价,失去8NAA个电子,故正确;
⑩用含硅胶、铁粉的透气小袋与食品一起密封包装,利用了Fe粉的还原性,可防止食品被氧化,故正确.
故答案为:⑤⑨⑩;
(4)硝酸被稳定,易分解生成二氧化氮,反应的化学方程式为4HNO33=4NO22+O22+2H22O,故答案为:4HNO33=4NO22+O22+2H22O;
(5)明矾溶液与少量氢氧化钡溶液反应可生成氢氧化铝和硫酸钡沉淀,反应的离子方程式为2Al3+3++3SO442-2-+3Ba2+2++6OH--=2Al(OH) 33↓+3BaSO44↓,
故答案为:2Al3+3++3SO442-2-+3Ba2+2++6OH--=2Al(OH) 33↓+3BaSO44↓.
看了 根据所给信息填空(1)用0....的网友还看了以下:
为什么饱和溶液的溶质质量分数=s/100+s×100%求推理过程还有为什么饱和溶液的溶解度=w/1 2020-04-09 …
相对分子质量为M的某物质在室温下的溶解度为S,此时测得饱和溶液的密度为dg•cm-3,则该饱和溶液 2020-04-13 …
将12.6g无水亚硫酸钠固体加入100mL8mol/L的硫酸中的以制取so2气体,反应完全后,有部 2020-04-26 …
25℃时,某物质(无结晶水)溶解度为Sg,其摩尔质量为Mg/mol,饱和溶液密度为dg/cm3.则 2020-05-13 …
物质的量浓度为amol/ml的S溶液(体积不限),要配置成质量分数为b%的S溶液,H毫升(ml), 2020-05-14 …
饱和溶液的溶解度计算公式到底是S/100g=m质/m剂还是S/100g+s=m质/m液? 2020-05-17 …
电池Pb│PbSO4(s)│Na2SO4•10H2O饱和溶液│Hg2SO4(s)│Hg在25oC时 2020-06-07 …
KCl和KNO3的溶解度表及溶解度曲线如图所示,下列说法不正确的是()温度/℃20304050溶解 2020-06-11 …
20.在石灰浆中存在Ca(OH)2(s)——Ca2++2OH-平衡,向室温下的石灰浆中加入一些小块 2020-07-04 …
图1为研究渗透作用的实验装置,请回答下列问题:(1)漏斗内溶液(S1)和漏斗外溶液(S2)为两种不 2020-07-08 …