早教吧作业答案频道 -->化学-->
铝和氢氧化钾都是重要的工业产品,请回答问题:(1)金属铝的生产是以Al2O3为原料,在熔融状态下进行电解,化学方程式为:2Al2O3高温
题目详情
铝和氢氧化钾都是重要的工业产品,请回答问题:
(1)金属铝的生产是以Al2O3为原料,在熔融状态下进行电解,化学方程式为:2Al2O3
4Al+3O2Na3AlF6,电极均由石墨材料做成,电解时不断消耗的电极是___(填“阴极”或“阳极”),原因是___(用化学方程式表示).
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为___.
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为:2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag.则负极的电极反应式为___,正极附近溶液的碱性___(填“增强”、“不变”或“减弱”).
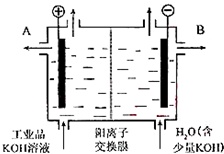
(4)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
①该电解槽的阳极反应式是___.
②阴极区碱性增强的原因是___
③除去杂质后的氢氧化钾溶液从液体出口___(填写“A”或“B”)导出.

(1)金属铝的生产是以Al2O3为原料,在熔融状态下进行电解,化学方程式为:2Al2O3
| ||
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为___.
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为:2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag.则负极的电极反应式为___,正极附近溶液的碱性___(填“增强”、“不变”或“减弱”).
(4)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
①该电解槽的阳极反应式是___.
②阴极区碱性增强的原因是___
③除去杂质后的氢氧化钾溶液从液体出口___(填写“A”或“B”)导出.
▼优质解答
答案和解析
(1)电极均由石墨材料做成,电极过程中阳极生成氧气会和碳反应生成二氧化碳;阳极不断减少,故答案为:阳极;C+O2
CO2;
(2)以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,电解过程中铝做阳极失去电子生成氧化铝,依据原子守恒和电子守恒写出电极反应为:2Al+3H2O-6e-=Al2O3+6H+,故答案为:2Al+3H2O-6e-=Al2O3+6H+;
(3)Al-Ag2O电池可用作水下动力电源,化学反应为2A1+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,反应是原电池反应,依据元素化合价变化判断,铝元素化合价升高失电子的做负极发生氧化反应,电极反应为:Al+4OH--3e-=[Al(OH)4]-;银元素化合价降低得到电子的做电池正极发生还原反应;电极反应为:Ag2O+H2O+2e-=2Ag+2OH-;正极附近生成了氢氧根离子,附近的碱性增强,故答案为:Al+4OH--3e-=[Al(OH)4]-;增强;
(4)①用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质含氧酸根,相当于电解水,故电解时,阳极:4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
②阴极:4H++4e-=2H2↑,其中阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,在阴极和阳极之间有阳离子交换膜,只允许阳离子K+和H+通过,留下的OH-浓度增大,阴极附近溶液pH会增大,
故答案为:通电开始后,水电离产生的H+在阴极放电,留下的OH-又不能通过阳离子交换膜,所以阴极附近溶液pH会增大;
③在阴极区聚集大量的K+和OH-,从而产生纯的氢氧化钾溶液,除杂后的氢氧化钾溶液从出口B导出,故答案为:B.
| ||
(2)以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,电解过程中铝做阳极失去电子生成氧化铝,依据原子守恒和电子守恒写出电极反应为:2Al+3H2O-6e-=Al2O3+6H+,故答案为:2Al+3H2O-6e-=Al2O3+6H+;
(3)Al-Ag2O电池可用作水下动力电源,化学反应为2A1+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,反应是原电池反应,依据元素化合价变化判断,铝元素化合价升高失电子的做负极发生氧化反应,电极反应为:Al+4OH--3e-=[Al(OH)4]-;银元素化合价降低得到电子的做电池正极发生还原反应;电极反应为:Ag2O+H2O+2e-=2Ag+2OH-;正极附近生成了氢氧根离子,附近的碱性增强,故答案为:Al+4OH--3e-=[Al(OH)4]-;增强;
(4)①用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质含氧酸根,相当于电解水,故电解时,阳极:4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
②阴极:4H++4e-=2H2↑,其中阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,在阴极和阳极之间有阳离子交换膜,只允许阳离子K+和H+通过,留下的OH-浓度增大,阴极附近溶液pH会增大,
故答案为:通电开始后,水电离产生的H+在阴极放电,留下的OH-又不能通过阳离子交换膜,所以阴极附近溶液pH会增大;
③在阴极区聚集大量的K+和OH-,从而产生纯的氢氧化钾溶液,除杂后的氢氧化钾溶液从出口B导出,故答案为:B.
看了铝和氢氧化钾都是重要的工业产品...的网友还看了以下:
1.一个多边形的每个外角都相等,如果它的内角与外角的度数之比是13:2,求这个多边形的边数.2.已 2020-04-26 …
高数,积分求立体体积.计算两个圆柱面:x平方+y平方=a方z方+y方=a方老师笔记如下:取积分变量 2020-04-27 …
0为方阵A的特征值是A不可逆的充要条件 2020-05-16 …
长为0.5m质量不计的杆下端固定在O点上,上端连着球A,球A质量为2kg,A绕O在竖直平面做圆周运 2020-05-16 …
已知,a、b、c为△ABC的边长,b、c满足(b-2)2+c−3=0,且a为方程|a-4|=2的解 2020-05-21 …
()世纪,欧美的火灾保险公司大量出现,火灾承保能力大为提高A.18B.17C.19D.20 2020-05-22 …
从高为H的地方A平抛一物体,其水平位移为2S,在A点正上方距地面2H高的B点沿相同方向平抛另一物体 2020-06-06 …
1.e为方阵A的特征值,则矩阵kA,A的平方,aA+bE,A的m次方,A的逆,A的伴随阵分别有特征 2020-06-18 …
0为方阵A的特征值是A不可逆的充要条件 2020-06-23 …
小明家的住宅是一栋7层楼,请你帮他估计一下这栋普通住宅楼约为多高?A.2400cmB.40mC.0 2020-07-11 …